1 . 向某容积固定的密闭容器中加入0.3mol A、0.1mol C和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体的平均相对分子质量没有变化。请回答下列问题:
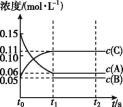
(1)密闭容器的容积是_______ L。
(2)若t1=15时,则t0~t1s内以C物质浓度变化表示的反应速率v(C)=_______ 。
(3)写出反应的化学方程式:_______ 。
(4)t2s时,C在平衡混合气体中的百分含量为_______ ,此时v正(A)_______ v逆(B)(选填“>”“<”或“=”)。
(5)B的起始的物质的量是_______ 。

(1)密闭容器的容积是
(2)若t1=15时,则t0~t1s内以C物质浓度变化表示的反应速率v(C)=
(3)写出反应的化学方程式:
(4)t2s时,C在平衡混合气体中的百分含量为
(5)B的起始的物质的量是
您最近一年使用:0次
2 . 用活性炭还原NO2可防止空气污染,其反应原理为2C(s)+2NO2(g) N2(g)+2CO2(g)。在密闭容器中1mol NO2和足量C发生上述反应,反应相同时间内测得 NO2的生成速率与 N2的生成速率随温度变化的关系如图1所示;维持温度不变,反应相同时间内得 NO2的转化率随压强的变化如图2所示。
N2(g)+2CO2(g)。在密闭容器中1mol NO2和足量C发生上述反应,反应相同时间内测得 NO2的生成速率与 N2的生成速率随温度变化的关系如图1所示;维持温度不变,反应相同时间内得 NO2的转化率随压强的变化如图2所示。
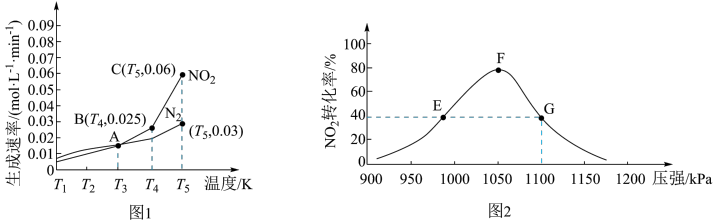
下列说法正确的是
 N2(g)+2CO2(g)。在密闭容器中1mol NO2和足量C发生上述反应,反应相同时间内测得 NO2的生成速率与 N2的生成速率随温度变化的关系如图1所示;维持温度不变,反应相同时间内得 NO2的转化率随压强的变化如图2所示。
N2(g)+2CO2(g)。在密闭容器中1mol NO2和足量C发生上述反应,反应相同时间内测得 NO2的生成速率与 N2的生成速率随温度变化的关系如图1所示;维持温度不变,反应相同时间内得 NO2的转化率随压强的变化如图2所示。 
下列说法正确的是
A.图1中的A、B、C三个点中只有A点的 正= 正= 逆 逆 |
B.图2中E点的 逆大于F点的 逆大于F点的 正 正 |
| C.图2中平衡常数K(E)=K(G),则NO2的平衡浓度c(E)=c(G) |
| D.G点时NO2的分压为550kPa |
您最近一年使用:0次
名校
解题方法
3 . 一定温度下,在容积恒定的密闭容器中,进行如下可逆反应: ,开始时向容器中加入足量的A和
,开始时向容器中加入足量的A和 ,反应到
,反应到 时刻达到平衡状态,下列说法不正确的是
时刻达到平衡状态,下列说法不正确的是
 ,开始时向容器中加入足量的A和
,开始时向容器中加入足量的A和 ,反应到
,反应到 时刻达到平衡状态,下列说法不正确的是
时刻达到平衡状态,下列说法不正确的是A. 时间内,混合气体的密度不发生改变 时间内,混合气体的密度不发生改变 | B. 时间内, 时间内, |
C.达平衡后, | D.容器中压强始终保持不变 |
您最近一年使用:0次
2022-05-24更新
|
179次组卷
|
2卷引用:山西省太原市第五中学2021-2022学年高一下学期5月阶段性检测化学试题
名校
4 . 中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。CO2可转化成有机物实现碳循环。在体积为2L的恒温密闭容器中,充入1molCO2和3molH2,一定条件下反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。

(1)前10min, (CO2)=
(CO2)=____ mol·L-1·min-1。
(2)能说明上述反应达到平衡状态的是____ (填字母)。
a.反应中CO2与CH3OH的物质的量浓度之比为1:1(即图中交叉点)
b.混合气体的压强不随时间的变化而变化
c.单位时间内生成1molH2O,同时生成1molCH3OH
d.混合气体的平均相对分子质量不随时间的变化而变化
e.混合气体的密度不随时间的变化而变化
f.CO2和CH3OH的反应速率之比为1∶1
(3)反应前与平衡时的压强比为____ 。
(4)平衡混合气体中CO2(g)和H2(g)的质量之比是____ 。
(5)平衡时H2的转化率为____ 。

(1)前10min,
 (CO2)=
(CO2)=(2)能说明上述反应达到平衡状态的是
a.反应中CO2与CH3OH的物质的量浓度之比为1:1(即图中交叉点)
b.混合气体的压强不随时间的变化而变化
c.单位时间内生成1molH2O,同时生成1molCH3OH
d.混合气体的平均相对分子质量不随时间的变化而变化
e.混合气体的密度不随时间的变化而变化
f.CO2和CH3OH的反应速率之比为1∶1
(3)反应前与平衡时的压强比为
(4)平衡混合气体中CO2(g)和H2(g)的质量之比是
(5)平衡时H2的转化率为
您最近一年使用:0次
2022-04-29更新
|
163次组卷
|
3卷引用:山西省长治市第二中学校2021-2022学年高一下学期期中考试化学试题
解题方法
5 . 下列方法中可以证明2HI(气) H2(气)+I2(气)已达平衡状态的是
H2(气)+I2(气)已达平衡状态的是
①单位时间内生成nmolH2的同时生成nmolHI
②一个H-H键断裂的同时有两个H-I键断裂
③温度和压强一定时混合气体密度不再变化
④反应速率v(H2)=v(I2)=0.5v(HI)时
⑤c(HI):c(H2):c(I2)=2:1:1
⑥温度和体积一定时,某一生成物浓度不再变化
⑦温度和体积一定时,容器内压强不再变化
⑧条件一定,混合气体的平均相对分子质量不再变化
⑨温度和体积一定时混合气体的颜色不再变化
 H2(气)+I2(气)已达平衡状态的是
H2(气)+I2(气)已达平衡状态的是①单位时间内生成nmolH2的同时生成nmolHI
②一个H-H键断裂的同时有两个H-I键断裂
③温度和压强一定时混合气体密度不再变化
④反应速率v(H2)=v(I2)=0.5v(HI)时
⑤c(HI):c(H2):c(I2)=2:1:1
⑥温度和体积一定时,某一生成物浓度不再变化
⑦温度和体积一定时,容器内压强不再变化
⑧条件一定,混合气体的平均相对分子质量不再变化
⑨温度和体积一定时混合气体的颜色不再变化
| A.②③④⑤⑥ | B.②⑥⑦⑧⑨ | C.①②⑥⑧ | D.②⑥⑨ |
您最近一年使用:0次
2021-11-06更新
|
157次组卷
|
2卷引用:山西省太原市第五十六中学2022-2023学年高二上学期10月联考化学试题
名校
解题方法
6 . 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图所示,下列表述正确的是
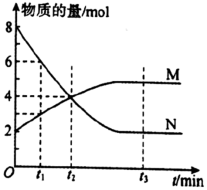

A.化学方程式:2N M M |
| B.t2时,正、逆反应速率相等,达到平衡 |
| C.t3时,正反应速率大于逆反应速率 |
| D.t1时,M的浓度是N的浓度的2倍 |
您最近一年使用:0次
2021-02-19更新
|
970次组卷
|
5卷引用:山西省长治市第一中学校2021-2022学年高一下学期第六次练考化学试题
名校
解题方法
7 . 在一定温度下的恒容容器中,发生反应:2A(g)+B(s) ⇌C(g)+D(g),下列描述中能表明反应已达到平衡状态的是
①混合气体的压强不变
②混合气体的密度不变
③C(g)的物质的量浓度不变
④容器内 A、C、D 三种气体的浓度之比为 2∶1∶1
⑤单位时间内生成 n mol C,同时生成 n mol D
⑥单位时间内生成 n mol D,同时生成 2n mol A
①混合气体的压强不变
②混合气体的密度不变
③C(g)的物质的量浓度不变
④容器内 A、C、D 三种气体的浓度之比为 2∶1∶1
⑤单位时间内生成 n mol C,同时生成 n mol D
⑥单位时间内生成 n mol D,同时生成 2n mol A
| A.①②⑤ | B.②③⑤ | C.②③⑥ | D.①③⑥ |
您最近一年使用:0次
2020-04-03更新
|
583次组卷
|
13卷引用:山西省稷山中学2021-2022学年高一下学期期中考试化学试题
山西省稷山中学2021-2022学年高一下学期期中考试化学试题新疆乌鲁木齐市第四中学2021-2022学年高一下学期期中考试化学试题湖北省黄冈市麻城市第二中学2021-2022学年高一下学期期中考试化学试题吉林省大安市第六中学校2021-2022学年高一下学期期中考试化学试题天津市第二南开学校2019-2020学年高一下学期阶段性检测化学试题鲁科版(2019)高一必修第二册 第2章 化学键 反应规律 第三节 化学反应的快慢和限度 方法帮甘肃省兰州市教育局第四片区2020-2021学年高一下学期期中考试化学试题吉林省延边朝鲜族自治州延边二中北校区2020-2021学年高一下学期第一次月考化学试题辽宁省鞍山市普通高中2022-2023学年高一下学期期中考试化学(A卷)试题新疆维吾尔自治区喀什第二中学2022-2023学年高一下学期期中考试化学试题吉林省长春市绿园区长春市新解放学校2022-2023学年高一下学期6月期中化学试题第2课时 化学反应的限度、化学反应条件的控制江西省横峰中学2023-2024学年高一下学期期中考试化学试题
名校
8 . 一定温度下,在容积为VL的密闭容器中进行反应:aN(g) bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示:
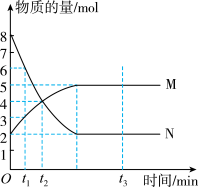
(1)此反应的化学方程式中 =
=____ 。
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为_____ 。
(3)下列叙述能说明上述反应达到平衡状态的是____ (填字母)。
A 反应中M与N的物质的量之比为1∶1
B 混合气体的总质量不随时间的变化而变化
C 混合气体的总物质的量不随时间的变化而变化
D 单位时间内消耗a mol N,同时生成b mol M
E 混合气体的压强不随时间的变化而变化
 bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示:
(1)此反应的化学方程式中
 =
=(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为
(3)下列叙述能说明上述反应达到平衡状态的是
A 反应中M与N的物质的量之比为1∶1
B 混合气体的总质量不随时间的变化而变化
C 混合气体的总物质的量不随时间的变化而变化
D 单位时间内消耗a mol N,同时生成b mol M
E 混合气体的压强不随时间的变化而变化
您最近一年使用:0次
2019-06-27更新
|
371次组卷
|
6卷引用:山西省长治市第一中学校2021-2022学年高一下学期第六次练考化学试题
山西省长治市第一中学校2021-2022学年高一下学期第六次练考化学试题(已下线)09~10年黄冈中学高一下学期期末考试化学卷(已下线)同步君 必修2 第2章 第3节 化学反应的限度高中化学人教版 必修2 第二章 化学反应与能量 第三节 化学反应的速率和限度 化学反应的限度江西省鄱阳县第二中学2018-2019学年高一下学期期中考试化学试题苏教版高一化学必修2专题2《化学反应与能量转化》测试卷



