11-12高三上·上海长宁·期末
解题方法
1 . 25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)  Sn2+(aq)+Pb(s)+ Q,体系中c(Pb2+)和c(Sn2+)变化关系如图所示。
Sn2+(aq)+Pb(s)+ Q,体系中c(Pb2+)和c(Sn2+)变化关系如图所示。

下列判断正确的是
 Sn2+(aq)+Pb(s)+ Q,体系中c(Pb2+)和c(Sn2+)变化关系如图所示。
Sn2+(aq)+Pb(s)+ Q,体系中c(Pb2+)和c(Sn2+)变化关系如图所示。
下列判断正确的是
| A.往平衡体系中加入金属铅后,c(Pb2+)增大 |
| B.往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)不变 |
| C.升高温度,平衡体系中c(Pb2+)增大,说明该反应Q>0 |
| D.c(Pb2+)一线表示正反应快慢, c(Sn2+)一线表示逆反应的快慢 |
您最近一年使用:0次
解题方法
2 . 硅及其化合物广泛应用于太阳能的利用、光导纤维及硅橡胶的制备等.
纯净的硅是从自然界中的石英矿石(主要成分为SiO2)中提取.高温下制取纯硅有如下反应(方法Ⅰ):
①SiO2(s)+2C(s)⇌Si(s)+2CO(g)
②Si(s)+2Cl2(g)⇌SiCl4(g)
③SiCl4(g)+2H2(g)→Si(s)+4HCl(g)
完成下列填空:
(1)硅原子核外有______ 种不同能级的电子,最外层p电子有______ 种自旋方向;SiO2晶体中每个硅原子与______ 个氧原子直接相连.
(2)单质的还原性:碳______ 硅(填写“同于”、“强于”或“弱于”).从平衡的视角而言,反应①能进行的原因是______ .
(3)反应②生成的化合物分子空间构型为;该分子为______ 分子(填写“极性”或“非极性”).
(4)某温度下,反应②在容积为V升的密闭容器中进行,达到平衡时Cl2的浓度为a mol/L.然后迅速缩小容器容积到0.5V升,t秒后重新达到平衡,Cl2的浓度为b mol/L.则:a______ b(填写“大于”、“等于”或“小于”).
(5)在t秒内,反应②中反应速率v(SiCl4)=______ (用含a、b的代数式表示).
(6)工业上还可以通过如下反应制取纯硅(方法Ⅱ):
④Si(粗)+3HCl(g)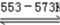 SiHCl3(l)+H2(g)+Q(Q>0)
SiHCl3(l)+H2(g)+Q(Q>0)
⑤SiHCl3(g)+H2(g) Si(纯)+3HCl(g)
Si(纯)+3HCl(g)
提高反应⑤中Si(纯)的产率,可采取的措施有:______ 、______ .
纯净的硅是从自然界中的石英矿石(主要成分为SiO2)中提取.高温下制取纯硅有如下反应(方法Ⅰ):
①SiO2(s)+2C(s)⇌Si(s)+2CO(g)
②Si(s)+2Cl2(g)⇌SiCl4(g)
③SiCl4(g)+2H2(g)→Si(s)+4HCl(g)
完成下列填空:
(1)硅原子核外有
(2)单质的还原性:碳
(3)反应②生成的化合物分子空间构型为;该分子为
(4)某温度下,反应②在容积为V升的密闭容器中进行,达到平衡时Cl2的浓度为a mol/L.然后迅速缩小容器容积到0.5V升,t秒后重新达到平衡,Cl2的浓度为b mol/L.则:a
(5)在t秒内,反应②中反应速率v(SiCl4)=
(6)工业上还可以通过如下反应制取纯硅(方法Ⅱ):
④Si(粗)+3HCl(g)
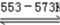 SiHCl3(l)+H2(g)+Q(Q>0)
SiHCl3(l)+H2(g)+Q(Q>0)⑤SiHCl3(g)+H2(g)
 Si(纯)+3HCl(g)
Si(纯)+3HCl(g)提高反应⑤中Si(纯)的产率,可采取的措施有:
您最近一年使用:0次
2020-03-21更新
|
365次组卷
|
3卷引用:上海市长宁区2016届高三12月质量检测化学试题



