1 . 下列事实中,不能用勒夏特列原理解释的是
| A.打开可乐饮料后会产生大量气泡 |
B.“ ”球浸泡在热水中,颜色变深 ”球浸泡在热水中,颜色变深 |
C.工业合成氨时采用500℃的高温(已知该反应 ) ) |
D.加水稀释 溶液,其电离程度增大 溶液,其电离程度增大 |
您最近半年使用:0次
2 . 某小组以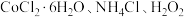 、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X。为测定其组成,进行如下实验。如图为氨的测定装置(已省略加热和夹持装置)
、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X。为测定其组成,进行如下实验。如图为氨的测定装置(已省略加热和夹持装置)
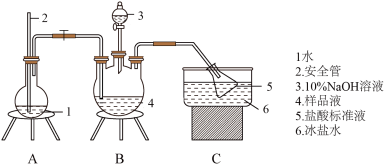
①氨的测定:准确称取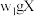 ,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量
,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量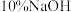 溶液,通入水蒸气,将样品液中的氨全部蒸出,用
溶液,通入水蒸气,将样品液中的氨全部蒸出,用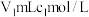 的盐酸标准溶液吸收。蒸氨结束后取下接收瓶,滴加指示剂,用
的盐酸标准溶液吸收。蒸氨结束后取下接收瓶,滴加指示剂,用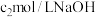 标准溶液滴定过剩的
标准溶液滴定过剩的 ,到终点时消耗
,到终点时消耗 溶液。
溶液。
②氯的测定:准确称取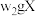 ,配成溶液后移取
,配成溶液后移取 于锥形瓶中,调
于锥形瓶中,调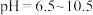 ,滴加指示剂
,滴加指示剂 溶液。在不断摇动下,用
溶液。在不断摇动下,用 标准溶液滴定至终点。(
标准溶液滴定至终点。( 为砖红色)
为砖红色)
回答下列问题:
(1)下列说法不正确 的是___________。
(2)滴定前,有关滴定管的正确操作为___________ (选出正确操作并按序排列)。
检漏→蒸馏水洗涤 开始滴定。
开始滴定。
A.烘干
B.装入滴定液至“0”刻度以上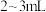 处
处
C.调整滴定液液面至“0”刻度或“0”刻度以下
D.用洗耳球吹出润洗液
E.排除气泡
F.用滴定液润洗2至3次
G.记录起始读数
(3)氯的测定过程中,滴定终点的现象是___________ 。当溶液中的 恰好沉淀完全(浓度等于
恰好沉淀完全(浓度等于 )时,溶液中
)时,溶液中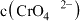 为
为___________  (保留两位有效数字)。已知
(保留两位有效数字)。已知 时,
时, 。
。
(4)测定 过程中,溶液
过程中,溶液 过低会使
过低会使 浓度降低,不能形成沉淀来指示终点。用相关的离子方程式解释
浓度降低,不能形成沉淀来指示终点。用相关的离子方程式解释 过低使
过低使 浓度降低的原因
浓度降低的原因___________ 。
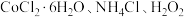 、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X。为测定其组成,进行如下实验。如图为氨的测定装置(已省略加热和夹持装置)
、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X。为测定其组成,进行如下实验。如图为氨的测定装置(已省略加热和夹持装置)
①氨的测定:准确称取
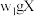 ,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量
,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量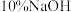 溶液,通入水蒸气,将样品液中的氨全部蒸出,用
溶液,通入水蒸气,将样品液中的氨全部蒸出,用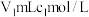 的盐酸标准溶液吸收。蒸氨结束后取下接收瓶,滴加指示剂,用
的盐酸标准溶液吸收。蒸氨结束后取下接收瓶,滴加指示剂,用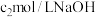 标准溶液滴定过剩的
标准溶液滴定过剩的 ,到终点时消耗
,到终点时消耗 溶液。
溶液。②氯的测定:准确称取
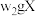 ,配成溶液后移取
,配成溶液后移取 于锥形瓶中,调
于锥形瓶中,调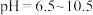 ,滴加指示剂
,滴加指示剂 溶液。在不断摇动下,用
溶液。在不断摇动下,用 标准溶液滴定至终点。(
标准溶液滴定至终点。( 为砖红色)
为砖红色)回答下列问题:
(1)下列说法
| A.安全管的作用是:当A中压力过大时,安全管中液面上升,使A瓶中压力稳定 |
| B.氨的测定过程中,滴定终点时仰视读数,氨的测定含量将偏高 |
| C.氨的测定接近终点时的“半滴操作”是:轻轻挤压玻璃珠下方的橡皮管,使半滴溶液悬于管口,用锥形瓶内壁将半滴溶液沾落,再用洗瓶以少量蒸馏水吹洗锥形瓶内壁 |
| D.氯的测定过程中,使用棕色滴定管的原因是防止硝酸银见光分解 |
(2)滴定前,有关滴定管的正确操作为
检漏→蒸馏水洗涤
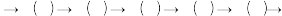 开始滴定。
开始滴定。A.烘干
B.装入滴定液至“0”刻度以上
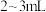 处
处C.调整滴定液液面至“0”刻度或“0”刻度以下
D.用洗耳球吹出润洗液
E.排除气泡
F.用滴定液润洗2至3次
G.记录起始读数
(3)氯的测定过程中,滴定终点的现象是
 恰好沉淀完全(浓度等于
恰好沉淀完全(浓度等于 )时,溶液中
)时,溶液中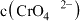 为
为 (保留两位有效数字)。已知
(保留两位有效数字)。已知 时,
时, 。
。(4)测定
 过程中,溶液
过程中,溶液 过低会使
过低会使 浓度降低,不能形成沉淀来指示终点。用相关的离子方程式解释
浓度降低,不能形成沉淀来指示终点。用相关的离子方程式解释 过低使
过低使 浓度降低的原因
浓度降低的原因
您最近半年使用:0次
3 . 在容积不变的密闭容器中进行如下反应: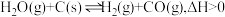 。达到平衡后,改变下列反应条件,相关叙述正确的是
。达到平衡后,改变下列反应条件,相关叙述正确的是
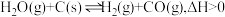 。达到平衡后,改变下列反应条件,相关叙述正确的是
。达到平衡后,改变下列反应条件,相关叙述正确的是A.加入 ,平衡正向移动,体系压强减小 ,平衡正向移动,体系压强减小 |
| B.加入少量C,正反应速率增大 |
| C.降低温度,平衡向正反应方向移动 |
D.加入 ,混合气体的密度增大 ,混合气体的密度增大 |
您最近半年使用:0次
4 . 下列事实不能用勒夏特列原理解释的是
A.用排饱和食盐水法收集 |
| B.在氨水中加入浓的氢氧化钠溶液,有氨气溢出 |
| C.冰镇的啤酒打开后泛起泡沫 |
D.对 平衡体系增加压强使颜色变深 平衡体系增加压强使颜色变深 |
您最近半年使用:0次
解题方法
5 . 在一定体积的密闭容器中,进行化学反应 ,其化学平衡常数K和温度T的关系如表:
,其化学平衡常数K和温度T的关系如表:
(1)该反应的化学平衡常数表达式
______ 。
(2)该反应为______ (填“吸热”或“放热”)反应,判断依据为______ 。
(3)某温度下,各物质的平衡浓度符合下式: ,试判断此时的温度为
,试判断此时的温度为______ 。
(4)若1200℃时,在某时刻平衡体系中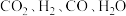 的浓度分别为
的浓度分别为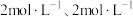 、
、 、
、 ,则此时上述反应的平衡移动方向为
,则此时上述反应的平衡移动方向为______ (填“正反应方向”“逆反应方向”或“不移动”),判断依据为______
 ,其化学平衡常数K和温度T的关系如表:
,其化学平衡常数K和温度T的关系如表:| T/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |

(2)该反应为
(3)某温度下,各物质的平衡浓度符合下式:
 ,试判断此时的温度为
,试判断此时的温度为(4)若1200℃时,在某时刻平衡体系中
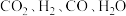 的浓度分别为
的浓度分别为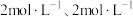 、
、 、
、 ,则此时上述反应的平衡移动方向为
,则此时上述反应的平衡移动方向为
您最近半年使用:0次
6 . 下列操作或事实不能 用勒夏特列原理解释的是
A. ,把充有 ,把充有 的球浸泡在冰水中,气体颜色变浅 的球浸泡在冰水中,气体颜色变浅 |
| B.打开碳酸饮料瓶盖时,会有气泡冒出 |
| C.合成氨工业中,采用高温有利于提高生产效率 |
D.向含有 的红色溶液中加入铁粉,振荡,溶液颜色变浅或褪去 的红色溶液中加入铁粉,振荡,溶液颜色变浅或褪去 |
您最近半年使用:0次
名校
解题方法
7 . 丙烯是一种重要的化工原料,在催化剂作用下,可以由丙烷直接脱氢或氧化脱氢制备。
反应Ⅰ(直接脱氢):

反应Ⅱ(氧化脱氢):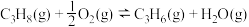

反应Ⅲ(氢气燃烧):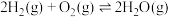
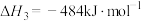
(1)
_____ kJ/mol。
(2)对于反应Ⅰ,总压恒定为100kPa,在密闭容器中通入 和Ar的混合气体。在温度为
和Ar的混合气体。在温度为 时,
时, 的平衡转化率与通入气体中
的平衡转化率与通入气体中 的物质的量分数的关系如图1
的物质的量分数的关系如图1
①结合图1,从平衡移动的角度分析,“通入Ar”的作用是_____ 。
②若要将 的平衡转化率提高到60%,则
的平衡转化率提高到60%,则
_____ 。
(3)恒温条件下,测得反应Ⅰ平衡时 的物质的量浓度与平衡总压的关系如图2.请在图上画出平衡时
的物质的量浓度与平衡总压的关系如图2.请在图上画出平衡时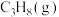 的物质的量浓度随平衡总压变化的曲线
的物质的量浓度随平衡总压变化的曲线_____ 。(在图中C点平衡总压为10Mpa时,丙烷和丙烯的物质的浓度相等)。
(4)①关于反应Ⅲ,下列说法正确的是_____ 。
A.该反应在任何温度下都能自发进行
B.升高温度,反应Ⅱ的平衡常数增大
C.通入的氧气越多,越有利于丙烷的氧化脱氢
D.将水液化分离出来,既可以加快反应速率,又能提高 的转化率
的转化率
②与直接脱氢反应相比,氧化脱氢制备丙烯的优点是_____ 。
(5)研究表明, 可催化氧化
可催化氧化 脱氢制丙烯。在p=0.1MPa,
脱氢制丙烯。在p=0.1MPa, ,催化剂X的催化下,气体按一定流速通过反应器,丙烷转化率和产物选择性(丙烯的选择性=丙烯的产率÷丙烷的转化率×100%)随温度变化如下表:
,催化剂X的催化下,气体按一定流速通过反应器,丙烷转化率和产物选择性(丙烯的选择性=丙烯的产率÷丙烷的转化率×100%)随温度变化如下表:
下列说法不正确的是_____。
反应Ⅰ(直接脱氢):


反应Ⅱ(氧化脱氢):
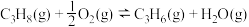

反应Ⅲ(氢气燃烧):
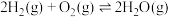
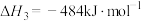
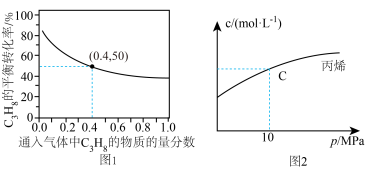
(1)

(2)对于反应Ⅰ,总压恒定为100kPa,在密闭容器中通入
 和Ar的混合气体。在温度为
和Ar的混合气体。在温度为 时,
时, 的平衡转化率与通入气体中
的平衡转化率与通入气体中 的物质的量分数的关系如图1
的物质的量分数的关系如图1①结合图1,从平衡移动的角度分析,“通入Ar”的作用是
②若要将
 的平衡转化率提高到60%,则
的平衡转化率提高到60%,则
(3)恒温条件下,测得反应Ⅰ平衡时
 的物质的量浓度与平衡总压的关系如图2.请在图上画出平衡时
的物质的量浓度与平衡总压的关系如图2.请在图上画出平衡时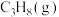 的物质的量浓度随平衡总压变化的曲线
的物质的量浓度随平衡总压变化的曲线(4)①关于反应Ⅲ,下列说法正确的是
A.该反应在任何温度下都能自发进行
B.升高温度,反应Ⅱ的平衡常数增大
C.通入的氧气越多,越有利于丙烷的氧化脱氢
D.将水液化分离出来,既可以加快反应速率,又能提高
 的转化率
的转化率②与直接脱氢反应相比,氧化脱氢制备丙烯的优点是
(5)研究表明,
 可催化氧化
可催化氧化 脱氢制丙烯。在p=0.1MPa,
脱氢制丙烯。在p=0.1MPa, ,催化剂X的催化下,气体按一定流速通过反应器,丙烷转化率和产物选择性(丙烯的选择性=丙烯的产率÷丙烷的转化率×100%)随温度变化如下表:
,催化剂X的催化下,气体按一定流速通过反应器,丙烷转化率和产物选择性(丙烯的选择性=丙烯的产率÷丙烷的转化率×100%)随温度变化如下表:| t℃ | 丙烷转化率 | 产物的选择性 | ||
 |  | CO | ||
| 400 | 4.06 | 93.12 | 2.20 | 4.68 |
| 500 | 12.32 | 91.23 | 3.16 | 5.61 |
| 600 | 35.22 | 85.44 | 7.73 | 6.83 |
| A.在较高温度下,催化剂X可提高产生丙烯反应的速率 |
B. 催化氧化 催化氧化 脱氢制丙烯的反应是放热反应 脱氢制丙烯的反应是放热反应 |
| C.相同条件下,使用不同的催化剂,丙烷的平衡转化率相同 |
| D.温度升高,催化剂X的活性下降,丙烯的产率降低 |
您最近半年使用:0次
2023-12-05更新
|
208次组卷
|
4卷引用:浙江省宁波市2023-2024学年高二上学期九校联考化学试题
浙江省宁波市2023-2024学年高二上学期九校联考化学试题浙江省稽阳联谊学校2023-2024学年高三上学期联考化学试题河南省焦作市博爱县第一中学2023-2024学年高二上学期1月期末化学试题(已下线)专题10 化学反应原理综合题(浙江专用)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)
名校
解题方法
8 . 在一密闭容器中,反应 达到平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的60%,则下列说法正确的是
达到平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的60%,则下列说法正确的是
 达到平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的60%,则下列说法正确的是
达到平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的60%,则下列说法正确的是| A.平衡向逆反应方向移动了 | B.物质A的转化率减小了 |
| C.物质B的质量分数增大了 | D. |
您最近半年使用:0次
2023-11-14更新
|
357次组卷
|
25卷引用:浙江省金华第一中学2022-2023学年高一下学期6月期末化学试题
浙江省金华第一中学2022-2023学年高一下学期6月期末化学试题(已下线)【浙江新东方】双师118黑龙江省绥化市第一中学2021-2022学年高二上学期期末考试化学试题吉林省长春希望高中2021-2022学年高二上学期期末考试化学试题浙江省浙东北联盟(ZDB)2023-2024学年高二上学期期中考试化学试题安徽省阜阳市临泉第一中学(高铁分校)2023-2024学年高二上学期期末考试化学试题黑龙江省伊春市伊美区第二中学2018-2019学年高二上学期阶段考试(12月)化学试题安徽省淮北市树人高级中学2020-2021学年高二上学期第一次联考化学试题天津市武清区梅厂中学2021-2022学年高二上学期阶段性练习化学试题广西百色中学2021-2022学年高二上学期第一次月考化学试题黑龙江省哈尔滨市依兰县高级中学2021-2022学年高二上学期第一次月考化学试题天津市外国语大学附属外国语学校2021-2022学年高二上学期期中阶段性检测化学试题黑龙江省大庆市东风中学2021-2022学年高二下学期开学考试化学试题广西桂林市第十八中学2021-2022学年高二下学期开学考试化学试题天津市第二南开学校2022-2023学年高二上学期9月阶段性线上练习化学试题 天津市宁河区芦台第一中学2022-2023学年高二上学期第一次学习诊断化学试题宁夏回族自治区中宁县第一中学2022-2023学年高二上学期10月月考化学试题山西省太原市第五中学校2023-2024学年高二上学期10月月考化学试题北京师范大学附属实验中学2023-2024学年高二上学期期中考试化学试题 北京师范大学附属实验中学2023-2024学年高二上学期期中考试化学试题(已下线)寒假作业03 化学平衡-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)新疆石河子第一中学2023-2024学年高二上学期11月月考化学试题北京师范大学附属实验中学2023-2024学年高二上学期期中考试化学试题河北省石家庄市第十五中学2023-2024学年高二上学期12月阶段考试化学试题广东省汕头市潮阳区河溪中学2023-2024学年高二上学期月考化学试题
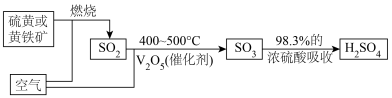
9 . 工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤:2SO2(g)+O2(g) 2SO3(g)。工业制硫酸的原理示意图:
2SO3(g)。工业制硫酸的原理示意图:
SO2的平衡转化率(%)随温度和压强的变化情况见下表:
下列说法不正确 的是
 2SO3(g)。工业制硫酸的原理示意图:
2SO3(g)。工业制硫酸的原理示意图:
SO2的平衡转化率(%)随温度和压强的变化情况见下表:
温度/℃ | 平衡时SO2的转化率/% | ||||
0.1MPa | 0.5MPa | 1MPa | 5MPa | 10MPa | |
450 | 97.5 | 98.9 | 99.2 | 99.6 | 99.7 |
550 | 85.6 | 92.9 | 94.9 | 97.7 | 98.3 |
| A.使用催化剂可以缩短反应达到平衡所需的时间 |
| B.通常不采取加压措施是因为常压下SO2的转化率已相当高 |
| C.工业生产中通入过量的空气可以提高SO2的平衡转化率 |
| D.反应选择在400~500 ℃,主要是让V2O5的活性最大、SO2的平衡转化率提高 |
您最近半年使用:0次
2023-07-29更新
|
277次组卷
|
3卷引用:浙江省丽水市2022-2023学年高二上学期期末考试化学试题
浙江省丽水市2022-2023学年高二上学期期末考试化学试题浙江省浙东北联盟(ZDB)2023-2024学年高二上学期期中考试化学试题(已下线)专题04 化学平衡-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)
名校
10 . 下列事实不能 用勒夏特列原理解释的是
| A.甲基橙滴加到pH=2的溶液中呈红色,滴加到pH=6的溶液中呈黄色 |
B.由NO2和N2O4组成的平衡体系:2NO2(g) N2O4(g),恒温缩小容积,平衡后气体颜色比原平衡深 N2O4(g),恒温缩小容积,平衡后气体颜色比原平衡深 |
C.Na(l) + KCl(l) 2NaCl(l)+K(g),工业上将钾蒸气从反应混合体系中分离出来,以制备金属钾 2NaCl(l)+K(g),工业上将钾蒸气从反应混合体系中分离出来,以制备金属钾 |
| D.实验室配制氯化铁溶液时,先将FeCl3晶体溶解在较浓的盐酸中,然后加水稀释到需要的浓度 |
您最近半年使用:0次
2023-07-29更新
|
503次组卷
|
2卷引用:浙江省丽水市2022-2023学年高二上学期期末考试化学试题



