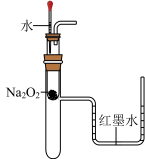
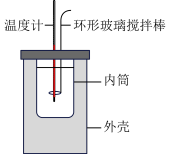
在容积不变的密闭容器中进行如下反应: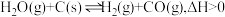 。达到平衡后,改变下列反应条件,相关叙述正确的是
。达到平衡后,改变下列反应条件,相关叙述正确的是
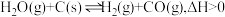 。达到平衡后,改变下列反应条件,相关叙述正确的是
。达到平衡后,改变下列反应条件,相关叙述正确的是A.加入 ,平衡正向移动,体系压强减小 ,平衡正向移动,体系压强减小 |
| B.加入少量C,正反应速率增大 |
| C.降低温度,平衡向正反应方向移动 |
D.加入 ,混合气体的密度增大 ,混合气体的密度增大 |
更新时间:2024-03-05 15:51:15
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】由反应物X转化为Y和Z的能量变化如图所示。下列说法错误的是( )


A.由 反应的ΔH >0 反应的ΔH >0 |
B.由 反应的ΔH = (E2-E1) kJ/mol 反应的ΔH = (E2-E1) kJ/mol |
| C.降低压强有利于提高Y的产率 |
| D.降低温度有利于提高Z的产率 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列事实中不能用勒·夏特列原理解释的是
| A.光照新制的氯水时,溶液的酸性逐渐增强 |
| B.向含有[Fe(SCN)]2+的红色溶液中加铁粉,振荡,溶液颜色变浅或退去 |
| C.加入催化剂有利于氨的氧化反应 |
| D.用排饱和食盐水法除去Cl2中的HCl |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】下列叙述中,不能用勒夏特列原理解释的是
| A.工业制取金属钾的反应为Na(l)+KCl(l)⇌NaCl(l)+K(g),选取适宜的温度,使K变成.蒸气从反应混合物中分离出来,有利于反应向右进行 |
| B.将铜粉和锌粉混合后放入稀硫酸中,产生气体的速率比不加铜粉快 |
| C.工业上SO2催化氧化生成SO3,常通入过量的空气来提高SO2的平衡转化率 |
| D.常温下,将pH=2的一元弱酸HA加水稀释100倍后,所得溶液的pH小于4 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】在一定温度下,对已达到平衡的反应:Fe3++3SCN- Fe(SCN)3,向其平衡后的 溶液中做如下处理,将导致平衡向左移动的是
Fe(SCN)3,向其平衡后的 溶液中做如下处理,将导致平衡向左移动的是
 Fe(SCN)3,向其平衡后的 溶液中做如下处理,将导致平衡向左移动的是
Fe(SCN)3,向其平衡后的 溶液中做如下处理,将导致平衡向左移动的是| A.加入少量氯化钾固体 | B.加水稀释 |
| C.加入少量 FeCl3固体 | D.加入少量 KSCN 固体 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】由下列实验操作及现象能得出相应结论的是
| 选项 | 操作 | 现象 | 结论 |
| A | 向 溶液中缓慢滴加稀硫酸 溶液中缓慢滴加稀硫酸 | 溶液由黄色变为橙色 | 增大 ,平衡向生成 ,平衡向生成 的方向移动 的方向移动 |
| B | 将蘸有某溶液的玻璃棒在酒精灯火焰上灼烧 | 火焰呈黄色 | 该溶液中一定含钠元素 |
| C | 用pH计测定 溶液和 溶液和 溶液的pH 溶液的pH |  溶液的pH较大 溶液的pH较大 |  酸性弱于 酸性弱于 |
| D | 将少量 加入稀硫酸中 加入稀硫酸中 | 溶液由无色变为蓝色,并有红色固体生成 | 反应中 只作还原剂 只作还原剂 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】在一密闭烧瓶中充满NO2,在25℃时NO2与N2O4达到平衡:2NO2 N2O4ΔH﹤0,把烧瓶置于100℃沸水中,又建立新的平衡状态,前后两平衡比较,不变的是
N2O4ΔH﹤0,把烧瓶置于100℃沸水中,又建立新的平衡状态,前后两平衡比较,不变的是
 N2O4ΔH﹤0,把烧瓶置于100℃沸水中,又建立新的平衡状态,前后两平衡比较,不变的是
N2O4ΔH﹤0,把烧瓶置于100℃沸水中,又建立新的平衡状态,前后两平衡比较,不变的是| A.颜色 | B.平均分子量 | C.物质的量 | D.密度 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】实验是学习化学的基础。下列装置和操作不能达到实验目的的是
|
|
| A.探究温度对化学平衡的影响 | B.探究浓度对反应速率的影响 |
|
|
| C.探究过氧化钠与水反应的热效应 | D.测定中和反应反应热 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列事实,不能用勒夏特列原理解释的是
A.2HI H2(g) + I2(g)的平衡体系,增大压强可是颜色加深 H2(g) + I2(g)的平衡体系,增大压强可是颜色加深 |
B.氯水中存在下列平衡:Cl2 + H2  HCl + HClO,当加入AgNO3溶液后,溶液的颜色变浅 HCl + HClO,当加入AgNO3溶液后,溶液的颜色变浅 |
| C.在合成氨的工业生产中要及时将生成的氨气分离出去 |
| D.可用浓氨水和氢氧化钠固体快速制取氨气 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列平衡移动方向和现象判断正确的是
A.Cr2O + H2O + H2O  2CrO 2CrO + 2H+,加水增大了水的浓度,平衡正向移动 + 2H+,加水增大了水的浓度,平衡正向移动 |
B.2NO2 N2O4,压缩容器体积,平衡正向移动,气体颜色变浅 N2O4,压缩容器体积,平衡正向移动,气体颜色变浅 |
C.Fe3+ + 3SCN- 3Fe(SCN)3,加入 KSCN 浓溶液,混合溶液颜色变浅 3Fe(SCN)3,加入 KSCN 浓溶液,混合溶液颜色变浅 |
D.[Cu(H2O)4]2+ + 4Cl- [CuCl4]2- + 4H2O ΔH>0,升高温度,溶液由蓝绿色变为黄绿色 [CuCl4]2- + 4H2O ΔH>0,升高温度,溶液由蓝绿色变为黄绿色 |
您最近一年使用:0次

 的值增大
的值增大