1 . CH3CHO在NaOH溶液作用下制取2-丁烯醛的历程如下:
下列说法不正确 的是

下列说法
| A.OH-是该反应的催化剂 |
B.CH3CHO分子中甲基上的“ ”比 ”比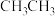 中的“ 中的“ ”更易电离出H+ ”更易电离出H+ |
| C.反应(4)加热失水有利于反应(3)平衡正向移动 |
| D.CH3CHO与CH3CH2CHO的混合液在NaOH溶液作用下最多可得到2种羟基醛 |
您最近半年使用:0次
2 . 硝酸盐型熔盐(含 )在太阳能光热发电领域被广泛应用.高纯
)在太阳能光热发电领域被广泛应用.高纯 的制备、性质与应用是目前研究的热点,部分生产方法及性质研究如下:
的制备、性质与应用是目前研究的热点,部分生产方法及性质研究如下: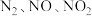 .
.
请回答:
(1)写出溶液A中的所有离子_________ ;方法Ⅱ中,“氧化吸收液”的目的是__________ .
(2)下列说法正确的是_________.
(3)方法Ⅰ中,用 代替
代替 ,得到副产品
,得到副产品 .工业上用
.工业上用 溶液浸取菱镁矿的煅烧粉(含
溶液浸取菱镁矿的煅烧粉(含 ),不断加热蒸出氨气,以获得较高浓度的
),不断加热蒸出氨气,以获得较高浓度的 溶液,其原理是
溶液,其原理是_________ .
(4)在某温度下, 分解得到的
分解得到的 可用于制备新型高效多功能水处理剂
可用于制备新型高效多功能水处理剂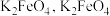 水溶液放置过程中会放出无色无味气体、产生沉淀、溶液呈强碱性.请依据上述信息,设计实验检验无色无味气体成分和沉淀中的金属元素
水溶液放置过程中会放出无色无味气体、产生沉淀、溶液呈强碱性.请依据上述信息,设计实验检验无色无味气体成分和沉淀中的金属元素_________ .写出 与
与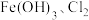 共热制取
共热制取 的化学方程式:
的化学方程式:_________ .
 )在太阳能光热发电领域被广泛应用.高纯
)在太阳能光热发电领域被广泛应用.高纯 的制备、性质与应用是目前研究的热点,部分生产方法及性质研究如下:
的制备、性质与应用是目前研究的热点,部分生产方法及性质研究如下: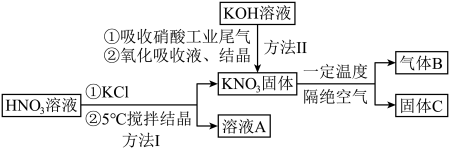
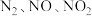 .
.请回答:
(1)写出溶液A中的所有离子
(2)下列说法正确的是_________.
A.方法Ⅰ说明:该条件下,酸性 |
B.方法Ⅱ中,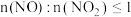 ,氮氧化物才能被足量的 ,氮氧化物才能被足量的 溶液充分吸收 溶液充分吸收 |
C. 固体与浓硫酸共热,可产生红棕色气体 固体与浓硫酸共热,可产生红棕色气体 |
| D.若气体B是一种单质,则所得固体C中不能含有三种元素 |
(3)方法Ⅰ中,用
 代替
代替 ,得到副产品
,得到副产品 .工业上用
.工业上用 溶液浸取菱镁矿的煅烧粉(含
溶液浸取菱镁矿的煅烧粉(含 ),不断加热蒸出氨气,以获得较高浓度的
),不断加热蒸出氨气,以获得较高浓度的 溶液,其原理是
溶液,其原理是(4)在某温度下,
 分解得到的
分解得到的 可用于制备新型高效多功能水处理剂
可用于制备新型高效多功能水处理剂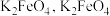 水溶液放置过程中会放出无色无味气体、产生沉淀、溶液呈强碱性.请依据上述信息,设计实验检验无色无味气体成分和沉淀中的金属元素
水溶液放置过程中会放出无色无味气体、产生沉淀、溶液呈强碱性.请依据上述信息,设计实验检验无色无味气体成分和沉淀中的金属元素 与
与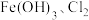 共热制取
共热制取 的化学方程式:
的化学方程式:
您最近半年使用:0次
2024-04-01更新
|
303次组卷
|
3卷引用:2024届浙江省温州市高三下学期第二次适应性考试(二模)化学试题
名校
解题方法
3 . 已知难溶性化合物 的化学式为
的化学式为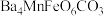 ,对
,对 进行如下实验,部分产物已经略去。
进行如下实验,部分产物已经略去。 中的金属元素在该实验条件下不能与
中的金属元素在该实验条件下不能与 产生配合物。
产生配合物。
(1) 高温下在
高温下在 气流中的反应
气流中的反应________ 氧化还原反应(填“属于”或“不属于”), 中钡元素的化合价为
中钡元素的化合价为________ 。
(2)步骤Ⅳ可以进行的原因除了生成 降低体系的能量之外,从化学平衡的角度解释能够发生的原因
降低体系的能量之外,从化学平衡的角度解释能够发生的原因________ 。
(3)下列说法正确的是________。
(4)固体 在一定条件下也可以与
在一定条件下也可以与 溶液反应,写出反应的离子方程式
溶液反应,写出反应的离子方程式________ 。
(5)设计实验检验混合气体A(除 外)的成份
外)的成份________ 。
 的化学式为
的化学式为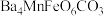 ,对
,对 进行如下实验,部分产物已经略去。
进行如下实验,部分产物已经略去。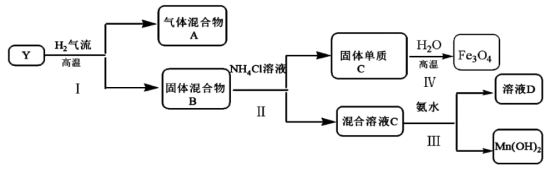
 中的金属元素在该实验条件下不能与
中的金属元素在该实验条件下不能与 产生配合物。
产生配合物。(1)
 高温下在
高温下在 气流中的反应
气流中的反应 中钡元素的化合价为
中钡元素的化合价为(2)步骤Ⅳ可以进行的原因除了生成
 降低体系的能量之外,从化学平衡的角度解释能够发生的原因
降低体系的能量之外,从化学平衡的角度解释能够发生的原因(3)下列说法正确的是________。
A.溶液D中阳离子只有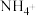 |
| B.若磁铁能吸引反应Ⅳ的剩余固体,则证明铁有剩余 |
| C.步骤Ⅱ中的氯化铵溶液也可以用盐酸代替 |
D.依据步骤Ⅲ可知碱性强弱 |
 在一定条件下也可以与
在一定条件下也可以与 溶液反应,写出反应的离子方程式
溶液反应,写出反应的离子方程式(5)设计实验检验混合气体A(除
 外)的成份
外)的成份
您最近半年使用:0次
解题方法
4 . 将二氧化碳转化为高附加值化学品是目前研究的热点之一,甲醇是重要的化工原料和优良的替代燃料,因此加氢制甲醇被广泛关注。在催化剂作用下主要发生以下反应。
Ⅰ.

Ⅱ.
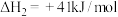
Ⅲ.

(1)反应Ⅲ自发进行的条件是______ 。
(2)恒温恒容条件下,原料气 、
、 以物质的量浓度1:3投料时,控制合适条件(不考虑反应Ⅲ),甲醇的选择性为
以物质的量浓度1:3投料时,控制合适条件(不考虑反应Ⅲ),甲醇的选择性为 。已知初始压强为
。已知初始压强为 ,
, ,
, 平衡转化率为
平衡转化率为 ,则该条件下反应Ⅱ
,则该条件下反应Ⅱ
______ 。(对于气相反应,用组分B的平衡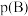 代替
代替 ,记作
,记作 。
。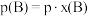 ,p为平衡压强,
,p为平衡压强,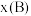 为平衡系统中
为平衡系统中 的物质的量分数。)
的物质的量分数。)
在 ,
, ,
, 、
、 以物质的量浓度1:3投料,以一定流速通过不同
以物质的量浓度1:3投料,以一定流速通过不同 与
与 催化剂,图a和b为催化反应
催化剂,图a和b为催化反应 转化率、甲醇选择性、甲醇收率随温度的变化,反应的产物只有甲醇、
转化率、甲醇选择性、甲醇收率随温度的变化,反应的产物只有甲醇、 和
和 。
。
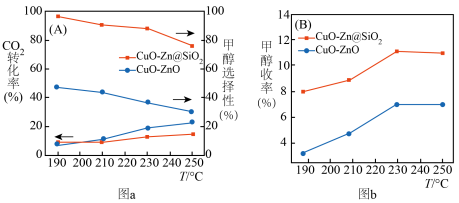
(3)分析在该压强下的最适合反应条件为______ 。
(4)推测在一定温度范围内,随着反应温度的升高, 转化率增大,但甲醇选择性降低的原因是
转化率增大,但甲醇选择性降低的原因是______ 。
(5)催化加氢的反应机理如下图所示。

下列说法正确的是_______
(6)在 催化剂条件下,保持流速与反应物投料比不变,增加反应物用量,请在图b上画出甲醇收率随温度变化曲线
催化剂条件下,保持流速与反应物投料比不变,增加反应物用量,请在图b上画出甲醇收率随温度变化曲线__________ 。
Ⅰ.


Ⅱ.

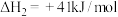
Ⅲ.


(1)反应Ⅲ自发进行的条件是
(2)恒温恒容条件下,原料气
 、
、 以物质的量浓度1:3投料时,控制合适条件(不考虑反应Ⅲ),甲醇的选择性为
以物质的量浓度1:3投料时,控制合适条件(不考虑反应Ⅲ),甲醇的选择性为 。已知初始压强为
。已知初始压强为 ,
, ,
, 平衡转化率为
平衡转化率为 ,则该条件下反应Ⅱ
,则该条件下反应Ⅱ
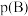 代替
代替 ,记作
,记作 。
。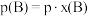 ,p为平衡压强,
,p为平衡压强,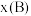 为平衡系统中
为平衡系统中 的物质的量分数。)
的物质的量分数。) 在
 ,
, ,
, 、
、 以物质的量浓度1:3投料,以一定流速通过不同
以物质的量浓度1:3投料,以一定流速通过不同 与
与 催化剂,图a和b为催化反应
催化剂,图a和b为催化反应 转化率、甲醇选择性、甲醇收率随温度的变化,反应的产物只有甲醇、
转化率、甲醇选择性、甲醇收率随温度的变化,反应的产物只有甲醇、 和
和 。
。
(3)分析在该压强下的最适合反应条件为
(4)推测在一定温度范围内,随着反应温度的升高,
 转化率增大,但甲醇选择性降低的原因是
转化率增大,但甲醇选择性降低的原因是(5)催化加氢的反应机理如下图所示。

下列说法正确的是_______
A. 催化剂中 催化剂中 抑制了 抑制了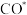 的解吸附,从而抑制 的解吸附,从而抑制 的生成。 的生成。 |
B. 催化剂上主要通过甲酸盐路径加氢生成甲醇。 催化剂上主要通过甲酸盐路径加氢生成甲醇。 |
| C.增大流速,原料气与催化剂碰撞机会多,甲醇产率一定增加。 |
D.随着温度升高,有利于 在催化剂表面反应,平衡转化率增大。 在催化剂表面反应,平衡转化率增大。 |
(6)在
 催化剂条件下,保持流速与反应物投料比不变,增加反应物用量,请在图b上画出甲醇收率随温度变化曲线
催化剂条件下,保持流速与反应物投料比不变,增加反应物用量,请在图b上画出甲醇收率随温度变化曲线
您最近半年使用:0次
23-24高三上·浙江绍兴·阶段练习
5 . 氯化钠应用广泛,下列说法正确的是
A.侯氏制碱法是将足量 通入氨化的氯化钠饱和溶液中,析出 通入氨化的氯化钠饱和溶液中,析出 晶体 晶体 |
| B.氯碱工业采用阴离子交换膜电解槽电解饱和食盐水获得氯气和氢氧化钠 |
| C.用洗净的铂丝蘸取某样品在酒精灯上灼烧,火焰呈黄色,该样品一定是钠盐 |
| D.向饱和氯化钠溶液中滴加浓盐酸能观察到固体析出 |
您最近半年使用:0次
23-24高三上·浙江·阶段练习
6 .  是一种重要的盐,其水溶液中存在平衡:
是一种重要的盐,其水溶液中存在平衡: 。下列说法
。下列说法不正确 的是
 是一种重要的盐,其水溶液中存在平衡:
是一种重要的盐,其水溶液中存在平衡: 。下列说法
。下列说法A. 溶液中加入淀粉溶液,溶液显蓝色 溶液中加入淀粉溶液,溶液显蓝色 |
B. 溶液呈棕褐色溶液,加入 溶液呈棕褐色溶液,加入 后,振荡,上层溶液显紫红色 后,振荡,上层溶液显紫红色 |
C. 溶液中滴加少量 溶液中滴加少量 溶液,溶液酸性增强 溶液,溶液酸性增强 |
D.利用 溶液可以除去硫粉中的少量碘单质 溶液可以除去硫粉中的少量碘单质 |
您最近半年使用:0次
23-24高三上·浙江·阶段练习
名校
解题方法
7 . 丙烯是一种重要的化工原料,在催化剂作用下,可以由丙烷直接脱氢或氧化脱氢制备。
反应Ⅰ(直接脱氢):

反应Ⅱ(氧化脱氢):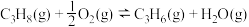

反应Ⅲ(氢气燃烧):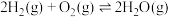
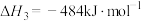
(1)
_____ kJ/mol。
(2)对于反应Ⅰ,总压恒定为100kPa,在密闭容器中通入 和Ar的混合气体。在温度为
和Ar的混合气体。在温度为 时,
时, 的平衡转化率与通入气体中
的平衡转化率与通入气体中 的物质的量分数的关系如图1
的物质的量分数的关系如图1
①结合图1,从平衡移动的角度分析,“通入Ar”的作用是_____ 。
②若要将 的平衡转化率提高到60%,则
的平衡转化率提高到60%,则
_____ 。
(3)恒温条件下,测得反应Ⅰ平衡时 的物质的量浓度与平衡总压的关系如图2.请在图上画出平衡时
的物质的量浓度与平衡总压的关系如图2.请在图上画出平衡时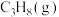 的物质的量浓度随平衡总压变化的曲线
的物质的量浓度随平衡总压变化的曲线_____ 。(在图中C点平衡总压为10Mpa时,丙烷和丙烯的物质的浓度相等)。
(4)①关于反应Ⅲ,下列说法正确的是_____ 。
A.该反应在任何温度下都能自发进行
B.升高温度,反应Ⅱ的平衡常数增大
C.通入的氧气越多,越有利于丙烷的氧化脱氢
D.将水液化分离出来,既可以加快反应速率,又能提高 的转化率
的转化率
②与直接脱氢反应相比,氧化脱氢制备丙烯的优点是_____ 。
(5)研究表明, 可催化氧化
可催化氧化 脱氢制丙烯。在p=0.1MPa,
脱氢制丙烯。在p=0.1MPa, ,催化剂X的催化下,气体按一定流速通过反应器,丙烷转化率和产物选择性(丙烯的选择性=丙烯的产率÷丙烷的转化率×100%)随温度变化如下表:
,催化剂X的催化下,气体按一定流速通过反应器,丙烷转化率和产物选择性(丙烯的选择性=丙烯的产率÷丙烷的转化率×100%)随温度变化如下表:
下列说法不正确的是_____。
反应Ⅰ(直接脱氢):


反应Ⅱ(氧化脱氢):
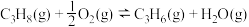

反应Ⅲ(氢气燃烧):
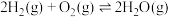
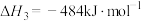
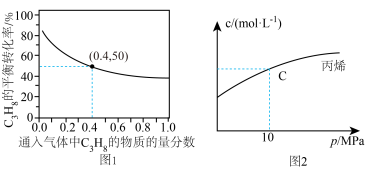
(1)

(2)对于反应Ⅰ,总压恒定为100kPa,在密闭容器中通入
 和Ar的混合气体。在温度为
和Ar的混合气体。在温度为 时,
时, 的平衡转化率与通入气体中
的平衡转化率与通入气体中 的物质的量分数的关系如图1
的物质的量分数的关系如图1①结合图1,从平衡移动的角度分析,“通入Ar”的作用是
②若要将
 的平衡转化率提高到60%,则
的平衡转化率提高到60%,则
(3)恒温条件下,测得反应Ⅰ平衡时
 的物质的量浓度与平衡总压的关系如图2.请在图上画出平衡时
的物质的量浓度与平衡总压的关系如图2.请在图上画出平衡时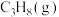 的物质的量浓度随平衡总压变化的曲线
的物质的量浓度随平衡总压变化的曲线(4)①关于反应Ⅲ,下列说法正确的是
A.该反应在任何温度下都能自发进行
B.升高温度,反应Ⅱ的平衡常数增大
C.通入的氧气越多,越有利于丙烷的氧化脱氢
D.将水液化分离出来,既可以加快反应速率,又能提高
 的转化率
的转化率②与直接脱氢反应相比,氧化脱氢制备丙烯的优点是
(5)研究表明,
 可催化氧化
可催化氧化 脱氢制丙烯。在p=0.1MPa,
脱氢制丙烯。在p=0.1MPa, ,催化剂X的催化下,气体按一定流速通过反应器,丙烷转化率和产物选择性(丙烯的选择性=丙烯的产率÷丙烷的转化率×100%)随温度变化如下表:
,催化剂X的催化下,气体按一定流速通过反应器,丙烷转化率和产物选择性(丙烯的选择性=丙烯的产率÷丙烷的转化率×100%)随温度变化如下表:| t℃ | 丙烷转化率 | 产物的选择性 | ||
 |  | CO | ||
| 400 | 4.06 | 93.12 | 2.20 | 4.68 |
| 500 | 12.32 | 91.23 | 3.16 | 5.61 |
| 600 | 35.22 | 85.44 | 7.73 | 6.83 |
| A.在较高温度下,催化剂X可提高产生丙烯反应的速率 |
B. 催化氧化 催化氧化 脱氢制丙烯的反应是放热反应 脱氢制丙烯的反应是放热反应 |
| C.相同条件下,使用不同的催化剂,丙烷的平衡转化率相同 |
| D.温度升高,催化剂X的活性下降,丙烯的产率降低 |
您最近半年使用:0次
2023-12-05更新
|
208次组卷
|
4卷引用:专题10 化学反应原理综合题(浙江专用)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)
(已下线)专题10 化学反应原理综合题(浙江专用)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)浙江省稽阳联谊学校2023-2024学年高三上学期联考化学试题浙江省宁波市2023-2024学年高二上学期九校联考化学试题河南省焦作市博爱县第一中学2023-2024学年高二上学期1月期末化学试题
23-24高三上·浙江·开学考试
解题方法
8 . 下列实验装置,可以达到实验目的的是
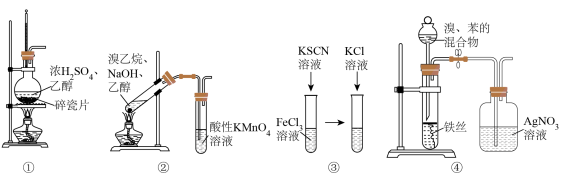

| A.用装置①在实验室制备乙烯 |
| B.用装置②证明溴乙烷消去反应有乙烯生成 |
C.用装置③探究KCl浓度是否对FeCl3+3KSCN Fe(SCN)3+3KCl的平衡移动有影响 Fe(SCN)3+3KCl的平衡移动有影响 |
| D.用装置④证明溴和苯发生的是取代反应而不是加成反应 |
您最近半年使用:0次
23-24高三上·浙江·阶段练习
9 . 某兴趣小组用淀粉水解液和浓 为原料制取草酸晶体
为原料制取草酸晶体 ,进而制备纳米草酸钙
,进而制备纳米草酸钙 ,按如下流程开展了实验(夹持仪器已省略):
,按如下流程开展了实验(夹持仪器已省略):
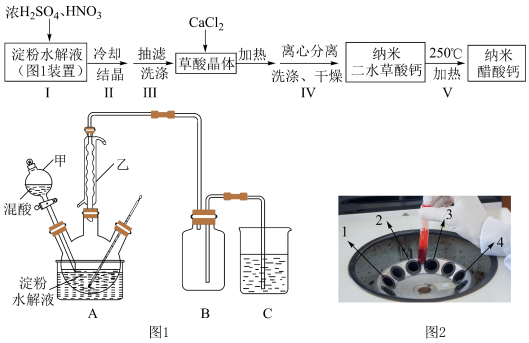
已知:①草酸能溶于水,易溶于乙醇;
②纳米草酸钙难溶于水,高温易分解;
③淀粉水解液与混酸反应的方程式: (
( 作催化剂)。
作催化剂)。
请回答:
(1)图1装置中仪器乙的名称___________ 。若C烧杯中盛放足量氢氧化钠溶液,写出C中发生反应的离子方程式___________ (假设气体全部被吸收),除了氢氧化钠溶液,还可以选用___________ (至少写出两种溶液)。
(2)下列有关操作说法不正确 的是___________。
(3)步骤Ⅳ中离心分离后得到的滤液中加入氨水还会析出产品沉淀,请结合离子方程式和平衡移动原理加以解释___________ 。
(4)草酸晶体 含有结晶水,某同学通过如下实验测定其组成:
含有结晶水,某同学通过如下实验测定其组成:
①配制标准氢氧化钠溶液:称取一定质量氢氧化钠固体,用适量水溶解后,选择合适的操作并排序(步骤可重复使用),配制溶液:___________
a→b→(___________)→(___________)→f→d→(___________)→(___________)→h
a.检查容量瓶玻璃塞处是否漏水b.将烧杯中的液体全部转移到容量瓶中
c.用蒸馏水洗涤烧杯和玻璃棒2-3次d.加蒸馏水至容量瓶接近标线
e.盖好瓶塞,反复上下颠倒容量瓶f.轻轻摇动容量瓶
g.离刻度线 时,改用胶头滴管加水至凹液面与刻度线相切h.装瓶贴标签
时,改用胶头滴管加水至凹液面与刻度线相切h.装瓶贴标签
②标定氢氧化钠溶液的浓度。
③滴定:准确称取一定质量草酸晶体于锥形瓶中,用蒸馏水溶解,以酚酞作指示剂,用上述 标准溶液滴定。若草酸晶体中混有
标准溶液滴定。若草酸晶体中混有 ,则该滴定法测得产品中
,则该滴定法测得产品中 的值
的值___________ (填“偏大”“偏小”“无影响”)。
 为原料制取草酸晶体
为原料制取草酸晶体 ,进而制备纳米草酸钙
,进而制备纳米草酸钙 ,按如下流程开展了实验(夹持仪器已省略):
,按如下流程开展了实验(夹持仪器已省略):
已知:①草酸能溶于水,易溶于乙醇;
②纳米草酸钙难溶于水,高温易分解;
③淀粉水解液与混酸反应的方程式:
 (
( 作催化剂)。
作催化剂)。请回答:
(1)图1装置中仪器乙的名称
(2)下列有关操作说法
| A.步骤Ⅱ采取冷却结晶,以防止草酸晶体失水 |
| B.步骤Ⅲ洗涤可用乙醇水溶液,步骤IV洗涤可用蒸馏水洗涤 |
C.步骤Ⅴ采用 加热,为提高反应速率,也可采用更高温度加热 加热,为提高反应速率,也可采用更高温度加热 |
| D.步骤Ⅳ采用离心分离,装置如图2所示,操作时应将两支离心管放置于1、4处 |
(3)步骤Ⅳ中离心分离后得到的滤液中加入氨水还会析出产品沉淀,请结合离子方程式和平衡移动原理加以解释
(4)草酸晶体
 含有结晶水,某同学通过如下实验测定其组成:
含有结晶水,某同学通过如下实验测定其组成:①配制标准氢氧化钠溶液:称取一定质量氢氧化钠固体,用适量水溶解后,选择合适的操作并排序(步骤可重复使用),配制溶液:
a→b→(___________)→(___________)→f→d→(___________)→(___________)→h
a.检查容量瓶玻璃塞处是否漏水b.将烧杯中的液体全部转移到容量瓶中
c.用蒸馏水洗涤烧杯和玻璃棒2-3次d.加蒸馏水至容量瓶接近标线
e.盖好瓶塞,反复上下颠倒容量瓶f.轻轻摇动容量瓶
g.离刻度线
 时,改用胶头滴管加水至凹液面与刻度线相切h.装瓶贴标签
时,改用胶头滴管加水至凹液面与刻度线相切h.装瓶贴标签②标定氢氧化钠溶液的浓度。
③滴定:准确称取一定质量草酸晶体于锥形瓶中,用蒸馏水溶解,以酚酞作指示剂,用上述
 标准溶液滴定。若草酸晶体中混有
标准溶液滴定。若草酸晶体中混有 ,则该滴定法测得产品中
,则该滴定法测得产品中 的值
的值
您最近半年使用:0次
2023-10-09更新
|
209次组卷
|
3卷引用:专题09 化学实验综合题(浙江专用)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)
(已下线)专题09 化学实验综合题(浙江专用)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)浙江省强基联盟2023-2024学年高三上学期10月联考化学试题浙江强基联盟2023-2024学年第一学期高三年级10月联考 化学
23-24高三上·浙江·阶段练习
解题方法
10 . 某小组设计实验探究铜被碘氧化的产物及铜元素的价态。
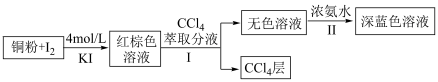
已知:① 易溶于
易溶于 溶液,发生反应
溶液,发生反应 (红棕色);
(红棕色);
②铜元素被氧化可能存在的形式有 (蓝色)、
(蓝色)、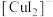 (无色);
(无色);
③ (无色),易被空气氧化。
(无色),易被空气氧化。
请回答:
(1)步骤Ⅰ中加入 萃取分液的目的是
萃取分液的目的是___________ 。
(2)用离子方程式表示步骤Ⅱ中发生的反应___________ 。
(3)已知 为白色不溶于水的固体,向
为白色不溶于水的固体,向 中加入浓
中加入浓 溶液,现象为
溶液,现象为___________ 。
(4)向深蓝色溶液中滴加浓盐酸,溶液呈黄绿色,写出该转化能进行的可能原因___________ 。
(已知: 稳定性远大于
稳定性远大于 (黄色),
(黄色), 稳定指的是不易发生解离反应
稳定指的是不易发生解离反应 )
)
(5) 层呈
层呈___________ 色。如何设计实验将 层中的碘元素分离得到碘单质,请补充完具体实验操作步骤:将
层中的碘元素分离得到碘单质,请补充完具体实验操作步骤:将 层溶液转移入分液漏斗中,加入足量浓氢氧化钠溶液,
层溶液转移入分液漏斗中,加入足量浓氢氧化钠溶液,___________ 。请补充完实验操作中涉及的离子方程式: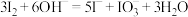 ,
,___________ 。

已知:①
 易溶于
易溶于 溶液,发生反应
溶液,发生反应 (红棕色);
(红棕色);②铜元素被氧化可能存在的形式有
 (蓝色)、
(蓝色)、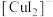 (无色);
(无色);③
 (无色),易被空气氧化。
(无色),易被空气氧化。请回答:
(1)步骤Ⅰ中加入
 萃取分液的目的是
萃取分液的目的是(2)用离子方程式表示步骤Ⅱ中发生的反应
(3)已知
 为白色不溶于水的固体,向
为白色不溶于水的固体,向 中加入浓
中加入浓 溶液,现象为
溶液,现象为(4)向深蓝色溶液中滴加浓盐酸,溶液呈黄绿色,写出该转化能进行的可能原因
(已知:
 稳定性远大于
稳定性远大于 (黄色),
(黄色), 稳定指的是不易发生解离反应
稳定指的是不易发生解离反应 )
)(5)
 层呈
层呈 层中的碘元素分离得到碘单质,请补充完具体实验操作步骤:将
层中的碘元素分离得到碘单质,请补充完具体实验操作步骤:将 层溶液转移入分液漏斗中,加入足量浓氢氧化钠溶液,
层溶液转移入分液漏斗中,加入足量浓氢氧化钠溶液,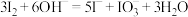 ,
,
您最近半年使用:0次
2023-10-09更新
|
208次组卷
|
3卷引用:专题08 工艺流程综合题(浙江专用)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)
(已下线)专题08 工艺流程综合题(浙江专用)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)浙江省强基联盟2023-2024学年高三上学期10月联考化学试题浙江强基联盟2023-2024学年第一学期高三年级10月联考 化学



