1 . 利用含钴废料(主要成分为 、
、 、
、 、
、 以及
以及 、
、 等)制备碳酸钴和硫酸镍晶体的一种工艺流程如图所示:
等)制备碳酸钴和硫酸镍晶体的一种工艺流程如图所示: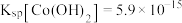 ;
;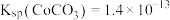 。
。
请回答下列问题:
(1)“碱浸”时所得滤液中溶质的主要成分为 和
和___________ 。“酸浸”时 发生反应的总离子方程式为
发生反应的总离子方程式为___________ 。
(2)“萃取”时 萃取的反应原理如下:
萃取的反应原理如下: (有机层)
(有机层)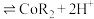 ,若萃取剂的量一定时,
,若萃取剂的量一定时,___________ (填“一次萃取”或“少量多次萃取”)的萃取效率更高。若“酸浸”后浸出液的 ,
, ,萃取完成后水相中
,萃取完成后水相中 为
为 ,则钴的萃取率为
,则钴的萃取率为___________ (结果保留一位小数,溶液体积变化忽略不计)。
(3)“沉锰”时, 转化为
转化为 ,则“沉锰”时发生反应的离子方程式为
,则“沉锰”时发生反应的离子方程式为___________ 。
(4)可以通过电解 溶液获得单质
溶液获得单质 和较浓的盐酸,其工作原理如图所示,其中膜a和膜b中,属于阳离子交换膜的是
和较浓的盐酸,其工作原理如图所示,其中膜a和膜b中,属于阳离子交换膜的是___________ 。若Ⅱ室溶液中溶质的质量增加了 ,则理论上获得的单质
,则理论上获得的单质 的质量为
的质量为___________ 。
 、
、 、
、 、
、 以及
以及 、
、 等)制备碳酸钴和硫酸镍晶体的一种工艺流程如图所示:
等)制备碳酸钴和硫酸镍晶体的一种工艺流程如图所示: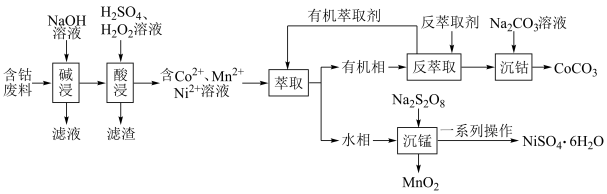
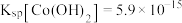 ;
;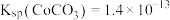 。
。请回答下列问题:
(1)“碱浸”时所得滤液中溶质的主要成分为
 和
和 发生反应的总离子方程式为
发生反应的总离子方程式为(2)“萃取”时
 萃取的反应原理如下:
萃取的反应原理如下: (有机层)
(有机层)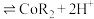 ,若萃取剂的量一定时,
,若萃取剂的量一定时, ,
, ,萃取完成后水相中
,萃取完成后水相中 为
为 ,则钴的萃取率为
,则钴的萃取率为(3)“沉锰”时,
 转化为
转化为 ,则“沉锰”时发生反应的离子方程式为
,则“沉锰”时发生反应的离子方程式为(4)可以通过电解
 溶液获得单质
溶液获得单质 和较浓的盐酸,其工作原理如图所示,其中膜a和膜b中,属于阳离子交换膜的是
和较浓的盐酸,其工作原理如图所示,其中膜a和膜b中,属于阳离子交换膜的是 ,则理论上获得的单质
,则理论上获得的单质 的质量为
的质量为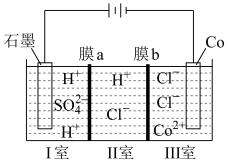
您最近一年使用:0次
2 . 抗击“疫情”期间,过氧乙酸是常用的消毒剂之一,实验室拟合成过氧乙酸并测定其含量。
(1)浓缩H2O2
在图示装置(加热装置已省略)中,由分液漏斗向冷凝管1中滴加30%H2O2溶液,最终得到质量分数约68%的H2O2溶液。
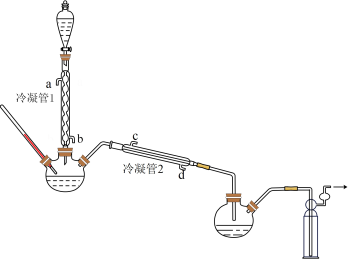
①冷凝管1、冷凝管2中进水接口依次为、___________ (填字母)。
②加热温度不宜超过60℃的原因是___________ 。
(2)合成过氧乙酸
向带有搅拌装置及温度计的500mL三口烧瓶中先加入16g冰醋酸,在搅拌下滴加90g68%H2O2溶液,最后加入4.1mL浓硫酸,搅拌5h,静置20h。(已知CH3COOH+H2O2= +H2O)
+H2O)
①用浓缩的68%H2O2溶液代替常见的30%H2O2溶液的目的是___________ 。
②充分搅拌的目的是___________ 。
(3)过氧乙酸含量的测定
步骤a:称取5.0g过氧乙酸试样(液体),配制成100mL溶液A。
步骤b:在碘量瓶中加入5.0mL 溶液、3滴
溶液、3滴 溶液、5.0mL溶液A,摇匀,用0.01mol/L的
溶液、5.0mL溶液A,摇匀,用0.01mol/L的 溶液滴定至溶液呈微红色。
溶液滴定至溶液呈微红色。
步骤c:向滴定后的溶液中再加1.0gKI(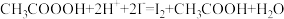 ),摇匀,置于暗处5min,用蒸馏水冲洗瓶盖及四周,加钼酸铵催化剂20mL,摇匀,用淀粉溶液作指示剂,用0.05mol/L的
),摇匀,置于暗处5min,用蒸馏水冲洗瓶盖及四周,加钼酸铵催化剂20mL,摇匀,用淀粉溶液作指示剂,用0.05mol/L的 标准溶液滴定至蓝色刚好褪去(
标准溶液滴定至蓝色刚好褪去( )。重复步骤b,步骤c三次,测得平均消耗
)。重复步骤b,步骤c三次,测得平均消耗 标准溶液的体积为20.00mL。
标准溶液的体积为20.00mL。
①步骤a中配制溶液A时,需要用到的玻璃仪器除烧杯、胶头滴管、玻璃棒和量筒外,还需要______ 。
②设计步骤b的目的是___________ 。
③过氧乙酸的质量分数为___________ %。
(1)浓缩H2O2
在图示装置(加热装置已省略)中,由分液漏斗向冷凝管1中滴加30%H2O2溶液,最终得到质量分数约68%的H2O2溶液。

①冷凝管1、冷凝管2中进水接口依次为、
②加热温度不宜超过60℃的原因是
(2)合成过氧乙酸
向带有搅拌装置及温度计的500mL三口烧瓶中先加入16g冰醋酸,在搅拌下滴加90g68%H2O2溶液,最后加入4.1mL浓硫酸,搅拌5h,静置20h。(已知CH3COOH+H2O2=
 +H2O)
+H2O)①用浓缩的68%H2O2溶液代替常见的30%H2O2溶液的目的是
②充分搅拌的目的是
(3)过氧乙酸含量的测定
步骤a:称取5.0g过氧乙酸试样(液体),配制成100mL溶液A。
步骤b:在碘量瓶中加入5.0mL
 溶液、3滴
溶液、3滴 溶液、5.0mL溶液A,摇匀,用0.01mol/L的
溶液、5.0mL溶液A,摇匀,用0.01mol/L的 溶液滴定至溶液呈微红色。
溶液滴定至溶液呈微红色。步骤c:向滴定后的溶液中再加1.0gKI(
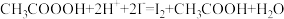 ),摇匀,置于暗处5min,用蒸馏水冲洗瓶盖及四周,加钼酸铵催化剂20mL,摇匀,用淀粉溶液作指示剂,用0.05mol/L的
),摇匀,置于暗处5min,用蒸馏水冲洗瓶盖及四周,加钼酸铵催化剂20mL,摇匀,用淀粉溶液作指示剂,用0.05mol/L的 标准溶液滴定至蓝色刚好褪去(
标准溶液滴定至蓝色刚好褪去( )。重复步骤b,步骤c三次,测得平均消耗
)。重复步骤b,步骤c三次,测得平均消耗 标准溶液的体积为20.00mL。
标准溶液的体积为20.00mL。①步骤a中配制溶液A时,需要用到的玻璃仪器除烧杯、胶头滴管、玻璃棒和量筒外,还需要
②设计步骤b的目的是
③过氧乙酸的质量分数为
您最近一年使用:0次
名校
3 . 向密闭容器中充入 ,发生反应:
,发生反应: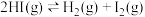
 ,达到平衡状态。该反应经过以下两步基元反应完成:
,达到平衡状态。该反应经过以下两步基元反应完成:
i.

ii.

下列分析不正确 的是
 ,发生反应:
,发生反应: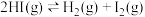
 ,达到平衡状态。该反应经过以下两步基元反应完成:
,达到平衡状态。该反应经过以下两步基元反应完成:i.


ii.


下列分析
A. 、 、 |
B.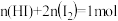 |
| C.恒温时,缩小体积,气体颜色变深,是平衡正向移动导致的 |
| D.恒容时,升高温度,气体颜色加深,同时电子发生了转移 |
您最近一年使用:0次
2021-11-08更新
|
1719次组卷
|
17卷引用:陕西省渭南市2022届高考第一次模拟考试化学试题
陕西省渭南市2022届高考第一次模拟考试化学试题陕西省渭南市2021-2022学年高三下学期第一次模拟考试化学试题北京市和平街第一中学2021-2022学年高三下学期5月检测(三模)化学试题北京市朝阳区2021-2022学年高三上学期期中考试化学试题浙江省湖州市2021-2022学年高二上学期期末考试化学试题浙江省湖州市2021-2022学年高二上学期期末调研测试化学试题(已下线)专题09反应速率、化学平衡-2022年高考真题+模拟题汇编(全国卷)(已下线)专题09反应速率、化学平衡-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题09反应速率、化学平衡-五年(2018~2022)高考真题汇编(全国卷)河南省洛阳市2021-2022学年高三上学期第一次统一考试化学试题河北省衡水中学2022届高三上学期六调考试化学试题安徽省太和县第八中学2021-2022学年高二上学期期中考试化学试题黑龙江省牡丹江市第一高级中学2022-2023学年高二上学期期中考试化学试题北京市东城区一六六中学2022-2023学年高三上学期期中考试化学试题北京交通大学附属中学2023-2024学年高二上学期期中考试化学试题北京市第一○一中学2023-2024学年高二上学期统练一化学试题广东省佛山市顺德区第一中学2023-2024学年高二上学期11月期中考试化学试题
4 . 下列说法正确的是
A.向 的液体平衡体系中加入少量KCl固体,由于生成物浓度增加,平衡逆向移动,所以液体血红色变浅 的液体平衡体系中加入少量KCl固体,由于生成物浓度增加,平衡逆向移动,所以液体血红色变浅 |
B.∆H>0、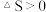 或∆H<0、∆S<0的化学反应都可能自发进行 或∆H<0、∆S<0的化学反应都可能自发进行 |
C.以铜为电极,电解KI溶液 含有少量淀粉 含有少量淀粉 ,阳极附近溶液呈现蓝色 ,阳极附近溶液呈现蓝色 |
D.向稀 中滴加 中滴加 溶液,反应的离子方程式为 溶液,反应的离子方程式为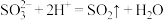 |
您最近一年使用:0次
5 . T K时,向2.0L恒容密闭容器中充入0.10mol COCl2,发生反应COCl2(g)  Cl2(g)+ CO(g),经过一段时间后反应达到平衡。反应过程中测得的部分数据见下表,下列说法正确的是
Cl2(g)+ CO(g),经过一段时间后反应达到平衡。反应过程中测得的部分数据见下表,下列说法正确的是
 Cl2(g)+ CO(g),经过一段时间后反应达到平衡。反应过程中测得的部分数据见下表,下列说法正确的是
Cl2(g)+ CO(g),经过一段时间后反应达到平衡。反应过程中测得的部分数据见下表,下列说法正确的是| t/s | 0 | 2 | 4 | 6 | 8 |
| n(Cl2)/mol | 0 | 0.030 | 0.039 | 0.040 | 0.040 |
| A.反应在前2s的平均速率v(COCl2)=0.015mol·L-1·s-1 |
| B.平衡后,温度不变再充入一定量COCl2,该反应的化学平衡常数减小 |
| C.保持其他条件不变,升高温度,若新平衡时c(Cl2)=0.038 mol·L-1,则反应的△H<0 |
| D.平衡后向上述容器中再充入0.10 mol COCl2,平衡正向移动,COCl2的转化率减小 |
您最近一年使用:0次
2020-12-16更新
|
1228次组卷
|
7卷引用:陕西省汉中市2021届高三第一次模拟化学试题
陕西省汉中市2021届高三第一次模拟化学试题陕西省汉中市2021届高三教学质量第一次检测考试化学试卷河南省新蔡县第一高级中学2021-2022学年高二10月月考化学试题(已下线)专题09反应速率、化学平衡-2022年高考真题+模拟题汇编(全国卷)(已下线)专题09反应速率、化学平衡-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题09反应速率、化学平衡-五年(2018~2022)高考真题汇编(全国卷)江西省瑞金市第二中学2022-2023学年高三上学期开学考试化学试题
11-12高二·河南鹤壁·阶段练习
名校
6 . 在相同容积的4个密闭器中进行同一种可逆反应,2A(g)+B(g) 3C(g)+2D(g),起始时4个容器所盛A、B的量如表所示各容器所盛物质的量:
3C(g)+2D(g),起始时4个容器所盛A、B的量如表所示各容器所盛物质的量:
在相同温度下,建立平衡时,4个容器中A或B的转化率的大小关系是
 3C(g)+2D(g),起始时4个容器所盛A、B的量如表所示各容器所盛物质的量:
3C(g)+2D(g),起始时4个容器所盛A、B的量如表所示各容器所盛物质的量:| 容器 | 甲 | 乙 | 丙 | 丁 |
| A | 2mol | 1mol | 2mol | 1mol |
| B | 1mol | 1mol | 2mol | 2mol |
| A.A的转化率为:甲<丙<乙<丁 | B.A的转化率为:甲<乙<丙<丁 |
| C.B的转化率为:甲>丙>乙>丁 | D.B的转化率为:丁>乙>丙>甲 |
您最近一年使用:0次
2019-10-29更新
|
276次组卷
|
8卷引用:2014陕西省西安中学高三上学期第四次质量检测化学试卷
(已下线)2014陕西省西安中学高三上学期第四次质量检测化学试卷(已下线)2014届陕西省西安市西安中学高三第四次质量检测化学试卷(已下线)2012-2013学年河南省淇县一中高二第一次月考化学试卷(已下线)2013-2014学年江西省赣州市十二县高二上学期期中考试化学试卷浙江省诸暨中学2019-2020学年高二上学期10月阶段性考试化学试题(已下线)【南昌新东方】2019 进贤二中 高二上 期中.河南省鹤壁市高级中学2020-2021学年高二上学期阶段性检测(二)化学试题河北省张家口市宣化区宣化第一中学2020-2021学年高二上学期10月月考化学试题
名校
7 . 已知通过乙醇制取氢气通常有如下两条途径:
a.CH3CH2OH(g)+H2O(g)⇌4H2(g)+2CO(g) △H1=+256.6kJ·mol-1
b.2CH3CH2OH(g)+O2(g)⇌6H2(g)+4CO(g) △H2=+27.6kJ·mol-1
则下列说法正确的是
a.CH3CH2OH(g)+H2O(g)⇌4H2(g)+2CO(g) △H1=+256.6kJ·mol-1
b.2CH3CH2OH(g)+O2(g)⇌6H2(g)+4CO(g) △H2=+27.6kJ·mol-1
则下列说法正确的是
| A.升高a的反应温度,乙醇的转化率增大 |
| B.由b可知:乙醇的燃烧热为13.8 kJ·mol-1 |
| C.对反应b来说,增大O2浓度可使△H2的值增大 |
| D.以上两种途径,制取等量的氢气,无论哪种途径,消耗的能量均相同 |
您最近一年使用:0次
2017-04-09更新
|
524次组卷
|
8卷引用:陕西省咸阳市2021届高三上学期高考模拟检测(一)化学试题
陕西省咸阳市2021届高三上学期高考模拟检测(一)化学试题2017届河北省保定市高三下学期第一次模拟考试理科综合化学试卷宁夏银川一中2018届高三第五次月考理综化学试题(已下线)2019高考备考二轮复习精品资料-专题8 化学反应中与能量变化(押题专练)【懂做原理题】2020届高三化学选修4二轮专题练——燃烧热【选择精编25题】(已下线)专题09反应速率、化学平衡-2022年高考真题+模拟题汇编(全国卷)(已下线)专题09反应速率、化学平衡-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题09反应速率、化学平衡-五年(2018~2022)高考真题汇编(全国卷)
8 . 下列事实能用勒沙特列原理解释的是
①由H2、I2蒸气、HI组成的平衡体系加压后颜色变深
②实验室中用氯化钠固体与浓硫酸共热制取氯化氢气体
③用排饱和食盐水法收集Cl2
④温度控制在500℃有利于合成氨反应
⑤工业制取金属钾Na(l)+ KCl(l) NaCl(l)+ K(g)选适宜的温度,使K成蒸气从反应混合物中分离出来
NaCl(l)+ K(g)选适宜的温度,使K成蒸气从反应混合物中分离出来
①由H2、I2蒸气、HI组成的平衡体系加压后颜色变深
②实验室中用氯化钠固体与浓硫酸共热制取氯化氢气体
③用排饱和食盐水法收集Cl2
④温度控制在500℃有利于合成氨反应
⑤工业制取金属钾Na(l)+ KCl(l)
 NaCl(l)+ K(g)选适宜的温度,使K成蒸气从反应混合物中分离出来
NaCl(l)+ K(g)选适宜的温度,使K成蒸气从反应混合物中分离出来| A.②③⑤ | B.①③⑤ | C.②③④⑤ | D.①②③⑤ |
您最近一年使用:0次



