下列操作或事实不能 用勒夏特列原理解释的是
A. ,把充有 ,把充有 的球浸泡在冰水中,气体颜色变浅 的球浸泡在冰水中,气体颜色变浅 |
| B.打开碳酸饮料瓶盖时,会有气泡冒出 |
| C.合成氨工业中,采用高温有利于提高生产效率 |
D.向含有 的红色溶液中加入铁粉,振荡,溶液颜色变浅或褪去 的红色溶液中加入铁粉,振荡,溶液颜色变浅或褪去 |
更新时间:2024-02-05 22:02:36
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】下列实验操作、现象、结论或解释不对应 的是
| 选项 | 操作 | 现象 | 结论或解释 |
| A | 常温下,向物质的量浓度均为 的 的 和 和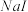 混合溶液中逐滴滴入 混合溶液中逐滴滴入 液 液 | 先出现黄色沉淀 | 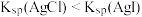 |
| B | 常温下,用 试纸测定相同浓度的 试纸测定相同浓度的 溶液和 溶液和 溶液的 溶液的 | 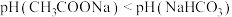 | 酸性: |
| C | 常温下,同浓度同体积的醋酸溶液和盐酸分别与相同大小的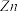 片反应 片反应 | 醋酸溶液中放出 的速率较慢 的速率较慢 | 醋酸是弱电解质 |
| D | 滴有酚酞的 ,溶液中加入少量 ,溶液中加入少量 固体 固体 | 溶液红色变浅 |  溶液中存在水解平衡 溶液中存在水解平衡 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】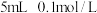 的KI溶液与
的KI溶液与 的
的 溶液发生反应:
溶液发生反应: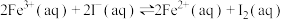 ,达到平衡。下列说法中正确的是
,达到平衡。下列说法中正确的是
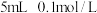 的KI溶液与
的KI溶液与 的
的 溶液发生反应:
溶液发生反应: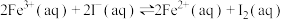 ,达到平衡。下列说法中正确的是
,达到平衡。下列说法中正确的是A.该反应的平衡常数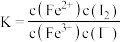 |
| B.加入少量KC1固体,平衡正向移动,溶液颜色变深 |
C.加入 萃取后,上层溶液呈紫红色,下层溶液呈浅绿色 萃取后,上层溶液呈紫红色,下层溶液呈浅绿色 |
D.经 萃取后,向水层溶液中滴入KSCN溶液,呈血红色 萃取后,向水层溶液中滴入KSCN溶液,呈血红色 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】对于工业合成氨反应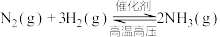 ,以下分析错误的是
,以下分析错误的是
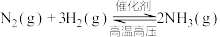 ,以下分析错误的是
,以下分析错误的是| A.可以通过改变温度、压强控制合成氨的反应限度 |
| B.高压比常压条件更有利于合成氨的反应,提高氨气的产率 |
| C.500℃左右比室温更有利于合成氨的反应,提高氨气的产率 |
| D.合成氨工业采用高压,不仅能提高转化率,还能缩短到达平衡的时间 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列事实不能用平衡移动原理解释的是
| A | B | C | D |
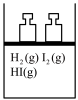 |  |  |  |
| 向H2(g)、I2(g)、HI(g)的平衡体系加压后颜色变深 | 开启啤酒瓶后,瓶中马上泛起大量泡沫 | 实验室制取乙酸乙酯时,将乙酸乙酯不断蒸出 | 石灰岩受地下水长期溶蚀形成溶洞 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】由下列实验事实所得出的结论正确的是
| 选项 | 实验事实 | 结论 |
| A | 某温度下,向容积可变的密闭容器中加入足量CaCO3,发生反应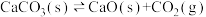 ,并达到平衡,将容器容积增大为原来的2倍 ,并达到平衡,将容器容积增大为原来的2倍 | 当体系再次达到平衡时,气体密度不变 |
| B | 恒温恒容条件下, ,增加 ,增加 的物质的量 的物质的量 | H2O的平衡转化率提高,且增大其反应速率 |
| C | 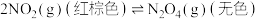  ,在反应达到平衡后,对平衡体系采取缩小容积、增大压强的措施, ,在反应达到平衡后,对平衡体系采取缩小容积、增大压强的措施, | 因为平衡向正反应方向移动,故体系颜色变浅 |
| D | 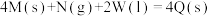 常温下,自发进行 常温下,自发进行 | 则ΔH>0 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】1100℃,在恒容密闭容器中加入一定量FeO(s)与CO(g),发生反应 ,一段时间后达到平衡。下列说法
,一段时间后达到平衡。下列说法不正确 的是
 ,一段时间后达到平衡。下列说法
,一段时间后达到平衡。下列说法A.升高温度,若 减小,则 减小,则 |
B.加入一定量CO(g),平衡正向移动, 的体积分数增大 的体积分数增大 |
C.改变浓度使 ,平衡将逆向移动 ,平衡将逆向移动 |
| D.若减小容器体积,平衡不移动 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐2】反应:aX(g)+bY(g) cZ(g),达到平衡时测得X气体的浓度为3mol/L,在恒温下将该容器体积扩大一倍,再次达到平衡时,测得X气体的浓度为1.4mol/L,则下列叙述不正确的是
cZ(g),达到平衡时测得X气体的浓度为3mol/L,在恒温下将该容器体积扩大一倍,再次达到平衡时,测得X气体的浓度为1.4mol/L,则下列叙述不正确的是
 cZ(g),达到平衡时测得X气体的浓度为3mol/L,在恒温下将该容器体积扩大一倍,再次达到平衡时,测得X气体的浓度为1.4mol/L,则下列叙述不正确的是
cZ(g),达到平衡时测得X气体的浓度为3mol/L,在恒温下将该容器体积扩大一倍,再次达到平衡时,测得X气体的浓度为1.4mol/L,则下列叙述不正确的是| A.a+b<c | B.平衡向生成Z的方向移动 |
| C.Z的体积分数降低 | D.Y的转化率升高 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列不能用勒沙特列原理解释的是
| A.用NH4Cl溶液除铁锈,增大NH4Cl溶液浓度,除铁锈速率加快 |
| B.氯水宜保存在低温、避光条件下 |
| C.NaF溶液不能盛放在玻璃瓶中 |
| D.KMnO4溶液通常用稀H2SO4酸化 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列事实能用勒夏特列原理解释的是
A.加压后,由 、 、 、HI组成的平衡体系颜色加深 、HI组成的平衡体系颜色加深 |
B.氯水中加入 粉末以提高氯水中HClO的浓度 粉末以提高氯水中HClO的浓度 |
C.在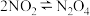 平衡体系中,加压后颜色加深 平衡体系中,加压后颜色加深 |
| D.合成氨工业,采取高温有利于合成氨 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】反应2X(g)+Y(g) 2Z(g)在不同温度下(T1和T2)产物Z的物质的量n(Z)与反应时间t的关系如图所示。下列判断正确的是
2Z(g)在不同温度下(T1和T2)产物Z的物质的量n(Z)与反应时间t的关系如图所示。下列判断正确的是
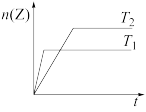
 2Z(g)在不同温度下(T1和T2)产物Z的物质的量n(Z)与反应时间t的关系如图所示。下列判断正确的是
2Z(g)在不同温度下(T1和T2)产物Z的物质的量n(Z)与反应时间t的关系如图所示。下列判断正确的是
| A.T1<T2,正反应为放热反应 |
| B.T1>T2,正反应为吸热反应 |
| C.T1>T2,逆反应为吸热反应 |
| D.T1<T2,逆反应为放热反应 |
您最近半年使用:0次


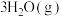 。反应的Arrhenius经验公式的实验数据如图所示,Arrhenius经验公式为
。反应的Arrhenius经验公式的实验数据如图所示,Arrhenius经验公式为 (
( 为活化能,k为速率常数,R和C为常数)。下列有关说法正确的是
为活化能,k为速率常数,R和C为常数)。下列有关说法正确的是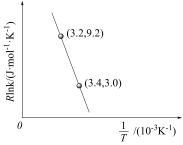
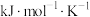
 物质的量平衡正向移动,
物质的量平衡正向移动,

