下列事实能用勒夏特列原理解释的是
A.加压后,由 、 、 、HI组成的平衡体系颜色加深 、HI组成的平衡体系颜色加深 |
B.氯水中加入 粉末以提高氯水中HClO的浓度 粉末以提高氯水中HClO的浓度 |
C.在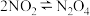 平衡体系中,加压后颜色加深 平衡体系中,加压后颜色加深 |
| D.合成氨工业,采取高温有利于合成氨 |
更新时间:2023-10-02 19:55:54
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】对可逆反应:2C(g) A(g) + 3B(g),(正反应吸热);下列说法正确的是( )
A(g) + 3B(g),(正反应吸热);下列说法正确的是( )
 A(g) + 3B(g),(正反应吸热);下列说法正确的是( )
A(g) + 3B(g),(正反应吸热);下列说法正确的是( )| A.升高温度,正反应速率减小,逆反应速率增大, |
| B.降低压强,反应速率减慢,平衡逆向移动 |
| C.达平衡后,升温或加压都有利于平衡正向移动 |
| D.达平衡后保持体积不变,增加C的物质的量,则C的转化率降低 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】已知在K2Cr2O7溶液中存在着如下平衡: 。加入下列物质能使溶液显橙色的是( )
。加入下列物质能使溶液显橙色的是( )
 。加入下列物质能使溶液显橙色的是( )
。加入下列物质能使溶液显橙色的是( )| A.氨水 | B.稀硫酸 | C.碳酸氢钠溶液 | D.水 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列反应达到平衡后,升高温度可以使混合气体平均相对分子质量增大的是( )
A.H2(g)+I2(g) 2HI(g)ΔH<0 2HI(g)ΔH<0 |
B.4NH3(g)+5O2(g) 4NO(g)+6H2O(g)ΔH<0 4NO(g)+6H2O(g)ΔH<0 |
C.N2(g)+3H2(g) 2NH3(g)ΔH<0 2NH3(g)ΔH<0 |
D.2SO3(g) 2SO2(g)+O2(g)ΔH>0 2SO2(g)+O2(g)ΔH>0 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列实验操作或做法不能达到目的的是
| 选项 | 操作或做法 | 目的 |
| A | 将 丙酮加入到适量碘水中,振荡,静置 丙酮加入到适量碘水中,振荡,静置 | 萃取碘水中的 |
| B | 向盐碱地(含有较多 、 、 )中施加适量石膏 )中施加适量石膏 | 降低土壤的碱性 |
| C | 将两支盛有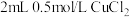 溶液的试管分别置于热水和冷水中 溶液的试管分别置于热水和冷水中 | 探究温度对化学平衡的影响 |
| D | 在薄钢板表面镀上一层锌 | 在金属表面覆盖保护层保护金属不被腐蚀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】通过以下两步反应可实现NH4Cl分解产物的分离。
NH4Cl(s)+MgO(s)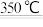 NH3(g)+Mg(OH)Cl(s)ΔH=+61.34kJ·mol-1
NH3(g)+Mg(OH)Cl(s)ΔH=+61.34kJ·mol-1
Mg(OH)Cl(s)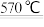 HCl(g)+MgO(s)ΔH=+97.50kJ·mol-1
HCl(g)+MgO(s)ΔH=+97.50kJ·mol-1
下列说法正确的是
NH4Cl(s)+MgO(s)
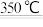 NH3(g)+Mg(OH)Cl(s)ΔH=+61.34kJ·mol-1
NH3(g)+Mg(OH)Cl(s)ΔH=+61.34kJ·mol-1Mg(OH)Cl(s)
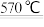 HCl(g)+MgO(s)ΔH=+97.50kJ·mol-1
HCl(g)+MgO(s)ΔH=+97.50kJ·mol-1下列说法正确的是
A.反应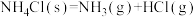 的ΔH=+158.84kJ·mol-1 的ΔH=+158.84kJ·mol-1 |
| B.上述两步反应的ΔS均小于0 |
| C.增大压强可以加快上述两步反应的速率 |
| D.5.35gNH4Cl完全分解理论上可获得标准状况下HCl约2.24L |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列平衡体系中,当条件改变时,不能用勒夏特列原理来解释的事实是( )
| A.N2(g)+3H2(g) ⇌ 2NH3(g),高压有利于合成氨 |
| B.2NO2(g) ⇌N2O4(g)ΔH<0,升高温度颜色加深 |
| C.Cl2+H2O⇌HCl+HClO,氯水中当加入AgNO3溶液后,溶液颜色变浅 |
| D.2SO2(g)+O2(g) ⇌ 2SO3(g),加催化剂可以提高生产效率 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列不能用勒夏特列原理解释的是( )
| A.实验室常用排饱和食盐水的方法收集Cl2 |
| B.将收集NO2气体的烧瓶密闭后,放在装有热水的烧杯中,发生颜色变化 |
| C.对2HI(g)⇌H2(g)+I2(g)平衡体系加压,颜色变深 |
| D.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列图示与对应的叙述不相符的是
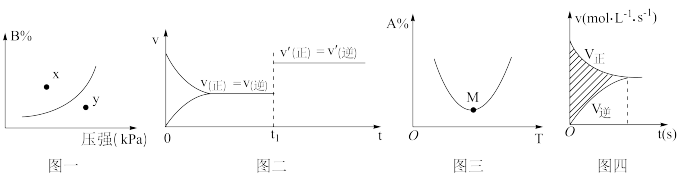

A.图一表示反应: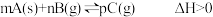 ,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系,则x点时 ,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系,则x点时 正> 正> 逆 逆 |
B.图二是可逆反应: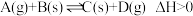 的速率时间图象,则在t1时刻改变条件可能是加入催化剂 的速率时间图象,则在t1时刻改变条件可能是加入催化剂 |
C.图三表示对于化学反应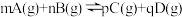 ,A的百分含量与温度(T)的变化情况,则该反应的 ,A的百分含量与温度(T)的变化情况,则该反应的 |
| D.图四所示图中的阴影部分面积的含义是反应物的物质的量减少量 |
您最近一年使用:0次

 ,当加入
,当加入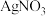 固体后,溶液颜色变浅
固体后,溶液颜色变浅 平衡体系,增大压强可使颜色变深
平衡体系,增大压强可使颜色变深 中的HCl
中的HCl 的反应,为提高
的反应,为提高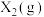 和
和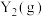 ,发生反应:
,发生反应: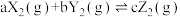
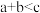
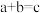
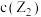 不变
不变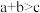
 2NH3的反应,使用铁触媒可以加快合成氨反应的速率
2NH3的反应,使用铁触媒可以加快合成氨反应的速率

