下列平衡体系中,当条件改变时,不能用勒夏特列原理来解释的事实是( )
| A.N2(g)+3H2(g) ⇌ 2NH3(g),高压有利于合成氨 |
| B.2NO2(g) ⇌N2O4(g)ΔH<0,升高温度颜色加深 |
| C.Cl2+H2O⇌HCl+HClO,氯水中当加入AgNO3溶液后,溶液颜色变浅 |
| D.2SO2(g)+O2(g) ⇌ 2SO3(g),加催化剂可以提高生产效率 |
更新时间:2020-08-15 09:47:57
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】已知: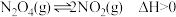 。向一恒温恒容的密闭容器中充入一定量的
。向一恒温恒容的密闭容器中充入一定量的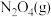 发生反应,
发生反应, 时达到平衡状态I,在
时达到平衡状态I,在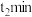 时改变某一条件,
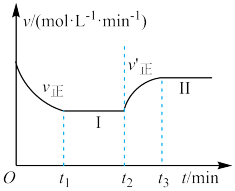
时改变某一条件, 时达到平衡状态II,正反应速率随时间的变化如图所示。下列说法正确的是
时达到平衡状态II,正反应速率随时间的变化如图所示。下列说法正确的是
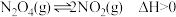 。向一恒温恒容的密闭容器中充入一定量的
。向一恒温恒容的密闭容器中充入一定量的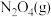 发生反应,
发生反应, 时达到平衡状态I,在
时达到平衡状态I,在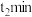 时改变某一条件,
时改变某一条件, 时达到平衡状态II,正反应速率随时间的变化如图所示。下列说法正确的是
时达到平衡状态II,正反应速率随时间的变化如图所示。下列说法正确的是
A.平衡状态下混合气体中 和 和 的体积比始终为 的体积比始终为 |
B.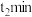 时改变的条件:向容器中通入 时改变的条件:向容器中通入 气体 气体 |
| C.恒温时,缩小容积,平衡正向移动,最终气体颜色变深 |
D.平衡常数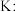 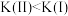 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】在K2Cr2O7溶液中,存在平衡:Cr2O (橙色)+H2O
(橙色)+H2O 2CrO
2CrO (黄色)+2H⁺。向一支试管中加入2mL 0.1mol/L K2Cr2O7溶液,向其中先滴入5滴6mol/LNaOH溶液,再滴入5滴6mol/LH2SO4溶液。下列说法正确的是
(黄色)+2H⁺。向一支试管中加入2mL 0.1mol/L K2Cr2O7溶液,向其中先滴入5滴6mol/LNaOH溶液,再滴入5滴6mol/LH2SO4溶液。下列说法正确的是
 (橙色)+H2O
(橙色)+H2O 2CrO
2CrO (黄色)+2H⁺。向一支试管中加入2mL 0.1mol/L K2Cr2O7溶液,向其中先滴入5滴6mol/LNaOH溶液,再滴入5滴6mol/LH2SO4溶液。下列说法正确的是
(黄色)+2H⁺。向一支试管中加入2mL 0.1mol/L K2Cr2O7溶液,向其中先滴入5滴6mol/LNaOH溶液,再滴入5滴6mol/LH2SO4溶液。下列说法正确的是| A.元素Cr属于短周期元素 |
| B.该反应属于氧化还原反应 |
| C.滴入碱液后,溶液颜色变浅至黄色,平衡正向移动 |
| D.再滴入酸液时,体系c(H⁺)增大,平衡正向移动 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】将 装入带活塞的密闭容器中,反应
装入带活塞的密闭容器中,反应 达到平衡状态,改变一个条件,下列叙述正确的是
达到平衡状态,改变一个条件,下列叙述正确的是
 装入带活塞的密闭容器中,反应
装入带活塞的密闭容器中,反应 达到平衡状态,改变一个条件,下列叙述正确的是
达到平衡状态,改变一个条件,下列叙述正确的是| A.慢慢压缩气体体积,若体积减小一半,压强增大,但小于原来的两倍 |
| B.慢慢压缩气体体积,平衡正向移动,混合气体颜色变浅 |
| C.体积不变,升高温度气体颜色加深,则此反应为吸热 |
| D.恒温、恒容时,充入惰性气体,压强增大,平衡正向移动,混合气体的颜色变浅 |
您最近一年使用:0次
【推荐2】科学家已经成功地利用二氧化碳催化氢化获得甲酸,利用化合物1催化氢化二氧化碳的反应过程如图甲所示,其中化合物2与水反应变成化合物3,化合物3与 的反应历程如图乙所示,其中TS表示过渡态,Ⅰ表示中间体。下列说法错误的是
的反应历程如图乙所示,其中TS表示过渡态,Ⅰ表示中间体。下列说法错误的是
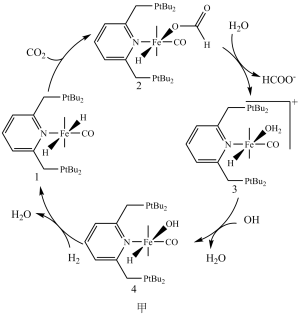
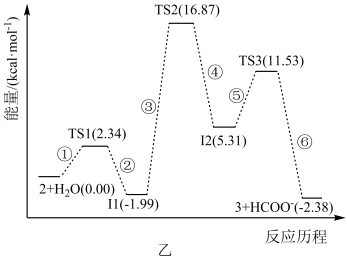
 的反应历程如图乙所示,其中TS表示过渡态,Ⅰ表示中间体。下列说法错误的是
的反应历程如图乙所示,其中TS表示过渡态,Ⅰ表示中间体。下列说法错误的是

A.从平衡移动的角度看,降低温度可促进化合物2与水反应变成化合物3与 |
| B.使用更高效的催化剂可以降低反应所需的活化能,最终提高二氧化碳的转化率 |
| C.该历程中最大能垒(活化能)E(正)=18.86Kcal/mol |
| D.化合物1到化合物2的过程中存在碳氧键的断裂和碳氢键的形成 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
下列说法错误的是( )
 CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
A.反应的化学平衡常数表达式为K=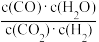 |
| B.该反应为吸热反应 |
| C.某温度下,各物质的平衡浓度符合如下关系:3c(CO2)·c(H2)=5c(CO)·c(H2O),此时的温度为830℃ |
| D.830℃时,容器中的化学反应已达到平衡。在其他条件不变的情况下,扩大容器的体积,平衡不移动 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】一定条件下,某可逆反应aA(g)  bB(s)+cC(g)自发进行并达到平衡状态后,A的转化率α(A)与温度(T)、压强(p)的关系如图所示。下列判断正确的是
bB(s)+cC(g)自发进行并达到平衡状态后,A的转化率α(A)与温度(T)、压强(p)的关系如图所示。下列判断正确的是
 bB(s)+cC(g)自发进行并达到平衡状态后,A的转化率α(A)与温度(T)、压强(p)的关系如图所示。下列判断正确的是
bB(s)+cC(g)自发进行并达到平衡状态后,A的转化率α(A)与温度(T)、压强(p)的关系如图所示。下列判断正确的是 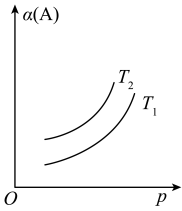
| A.a>b+c |
| B.该反应的平衡常数随温度的升高而增大 |
| C.T1﹤T2 |
| D.该反应自发进行的温度是低温 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列叙述中,不能用平衡移动原理解释的是( )
| A.红棕色的NO2,加压后颜色先变深后变浅 |
| B.高压比常压有利于合成SO3的反应 |
| C.加入催化剂有利于氨的合成 |
| D.工业制取金属钾:Na(l)+KCl(l)⇌NaCl(l)+K(g)选取适宜的温度,使K成蒸汽从反应混合物中分离出来 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列反应能用勒夏特列原理解释的是
| A.加入催化剂有利于氨的合成 |
| B.煅烧粉碎的黄铁矿矿石有利于SO2的生成 |
| C.硫酸生产中用98%的硫酸吸收SO3,而不用H2O或稀硫酸吸收SO3 |
D.工业制取金属钾Na(l)+KCl(l)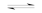 NaCl(l)+K(g)选取适宜的温度,使K变成蒸气从反应混合物中分离出 NaCl(l)+K(g)选取适宜的温度,使K变成蒸气从反应混合物中分离出 |
您最近一年使用:0次

 溶液中滴加无色的
溶液中滴加无色的 溶液后,有以下可逆反应存在:
溶液后,有以下可逆反应存在: 。已知
。已知 呈红色,在该平衡体系中加入少量
呈红色,在该平衡体系中加入少量 晶体后(忽略溶液体积的变化),红色将
晶体后(忽略溶液体积的变化),红色将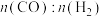 分别为1:1、1:2、1:3投料,发生反应为
分别为1:1、1:2、1:3投料,发生反应为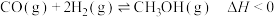 。测得不同压强下,CO平衡转化率如图所示。下列叙述正确的是
。测得不同压强下,CO平衡转化率如图所示。下列叙述正确的是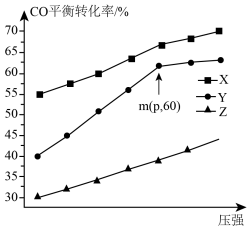
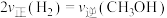 ,该反应达到平衡状态
,该反应达到平衡状态 的平衡转化率为60%
的平衡转化率为60%
 ,在一定条件下达到平衡,下列有关叙述正确的是
,在一定条件下达到平衡,下列有关叙述正确的是 的浓度不变
的浓度不变 的浓度,v(正)增大,v(逆)减小,平衡正向移动
的浓度,v(正)增大,v(逆)减小,平衡正向移动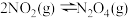 ,达平衡后,若将气体体积压缩到原来的
,达平衡后,若将气体体积压缩到原来的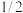 。当再达平衡时,则下列叙述
。当再达平衡时,则下列叙述 的体积分数增大
的体积分数增大 的转化率升高
的转化率升高

