名校
1 . 硫酰氯(SO2Cl2)可用于有机合成和药物制造等。实验室利用SO2和Cl2在活性炭作用下制取SO2Cl2[SO2(g)+Cl2(g) SO2Cl2(l) ΔH=-97.3kJ/mol],装置如图所示(部分装置省略)。已知SO2Cl2的熔点为-54.1℃,沸点为69.1℃,有强腐蚀性,不宜接触碱、醇、纤维素等许多无机物和有机物,遇水能发生剧烈反应并产生白雾。回答下列问题:
SO2Cl2(l) ΔH=-97.3kJ/mol],装置如图所示(部分装置省略)。已知SO2Cl2的熔点为-54.1℃,沸点为69.1℃,有强腐蚀性,不宜接触碱、醇、纤维素等许多无机物和有机物,遇水能发生剧烈反应并产生白雾。回答下列问题:
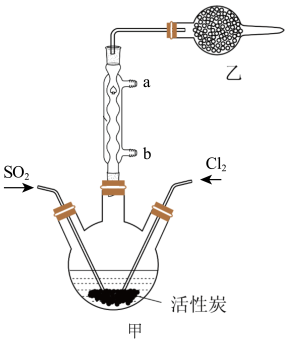
I.SO2Cl2的制备
(1)水应从___ (选填“a”或“b”)口进入。
(2)制取SO2的最佳组合是___ (填标号)。
①Fe+18.4mol/LH2SO4
②Na2SO3+70%H2SO4
③Na2SO3+3mo/LHNO3
(3)乙装置中盛放的试剂是___ 。
(4)制备过程中需要将装置甲置于冰水浴中,原因是___ 。
(5)反应结束后,分离甲中混合物的最佳实验操作是___ 。
II.测定产品中SO2Cl2的含量,实验步骤如下:
①取1.5g产品加入足量Ba(OH)2溶液,充分振荡、过滤、洗涤,将所得溶液均放入锥形瓶中;
②向锥形瓶中加入硝酸酸化,再加入0.2000mol·L-1的AgNO3溶液l00.00mL;
③向其中加入2mL硝基苯,用力摇动,使沉淀表面被有机物覆盖;
④加入NH4Fe(SO4)2指示剂,用0.1000mol·L-1NH4SCN溶液滴定过量Ag+,终点所用体积为10.00mL。
已知:Ksp(AgCl)=3.2×10-10 Ksp(AgSCN)=2×10-12
(6)滴定终点的现象为___ 。
(7)产品中SO2Cl2的质量分数为___ %,若步骤③不加入硝基苯则所测SO2Cl2含量将___ (填“偏高”、“偏低”或“无影响”)。
 SO2Cl2(l) ΔH=-97.3kJ/mol],装置如图所示(部分装置省略)。已知SO2Cl2的熔点为-54.1℃,沸点为69.1℃,有强腐蚀性,不宜接触碱、醇、纤维素等许多无机物和有机物,遇水能发生剧烈反应并产生白雾。回答下列问题:
SO2Cl2(l) ΔH=-97.3kJ/mol],装置如图所示(部分装置省略)。已知SO2Cl2的熔点为-54.1℃,沸点为69.1℃,有强腐蚀性,不宜接触碱、醇、纤维素等许多无机物和有机物,遇水能发生剧烈反应并产生白雾。回答下列问题:
I.SO2Cl2的制备
(1)水应从
(2)制取SO2的最佳组合是
①Fe+18.4mol/LH2SO4
②Na2SO3+70%H2SO4
③Na2SO3+3mo/LHNO3
(3)乙装置中盛放的试剂是
(4)制备过程中需要将装置甲置于冰水浴中,原因是
(5)反应结束后,分离甲中混合物的最佳实验操作是
II.测定产品中SO2Cl2的含量,实验步骤如下:
①取1.5g产品加入足量Ba(OH)2溶液,充分振荡、过滤、洗涤,将所得溶液均放入锥形瓶中;
②向锥形瓶中加入硝酸酸化,再加入0.2000mol·L-1的AgNO3溶液l00.00mL;
③向其中加入2mL硝基苯,用力摇动,使沉淀表面被有机物覆盖;
④加入NH4Fe(SO4)2指示剂,用0.1000mol·L-1NH4SCN溶液滴定过量Ag+,终点所用体积为10.00mL。
已知:Ksp(AgCl)=3.2×10-10 Ksp(AgSCN)=2×10-12
(6)滴定终点的现象为
(7)产品中SO2Cl2的质量分数为
您最近一年使用:0次
2019-12-10更新
|
482次组卷
|
3卷引用:陕西省西安市长安区第一中学2020-2021学年高三第七次质量检测理综化学试题
解题方法
2 . 研究人员从处理废旧线路板后的固体残渣(含SnO2、PbO2等)中进一步回收金属锡(Sn),一种回收流程如下。

已知:i.50Sn、82Pb为ⅣA族元素;
ii.SnO2、PbO2与强碱反应生成盐和水。
iii.+2价Sn不稳定,与空气接触容易氧化为+4价锡
(1)SnO2与稀NaOH反应的离子方程式为_______ 。
(2)滤液1中加入Na2S的目的是除铅,将相关方程式补充完整:____
Na2PbO3+□Na2S+□ =PbS↓+S↓+□
(3)不同溶剂中Na2SnO3的溶解度随温度变化如图。

①相同温度下,Na2SnO3的溶解度随NaOH浓度增大而减小,结合平衡移动原理解释原因:_______ 。
②操作Ⅲ的具体方法为_______ 。
(4)测定粗锡中Sn的纯度:在强酸性环境中将a g粗锡样品溶解(此时Sn全部转化成Sn2+),迅速加入过量NH4Fe(SO4)2溶液,以二苯胺磺酸钠为指示剂,用0.1000mol/L K2Cr2O7标准溶液滴定至终点。消耗K2Cr2O7溶液的体积如图所示,计算Sn的纯度。
已知: Sn2++2Fe3+=Sn4++2Fe2+;Cr2O +6Fe2++14H+=2Cr3++6Fe3++7H2O
+6Fe2++14H+=2Cr3++6Fe3++7H2O

①溶解粗锡时不宜选用浓盐酸,理由是_______ 。
②二苯胺磺酸钠是一种氧化还原指示剂,滴定终点时因发生_______ 反应而变色。(填写“氧化”或“还原”)
③滴定终点时消耗K2Cr2O7标准溶液体积_______ mL,粗锡样品中Sn的纯度为_______ (用质量分数表示)。
④下列操作会导致样品中Sn的测定结果偏高的是_______ (填选项字母)。
a.上述实验中若缓慢加入NH4Fe(SO4)2溶液
b.盛标准K2Cr2O7标准溶液的滴定管尖嘴部分有气泡未排除就开始滴定
c.实验用的酸式滴定管、锥形瓶水洗后均未润洗

已知:i.50Sn、82Pb为ⅣA族元素;
ii.SnO2、PbO2与强碱反应生成盐和水。
iii.+2价Sn不稳定,与空气接触容易氧化为+4价锡
(1)SnO2与稀NaOH反应的离子方程式为
(2)滤液1中加入Na2S的目的是除铅,将相关方程式补充完整:
Na2PbO3+□Na2S+□ =PbS↓+S↓+□
(3)不同溶剂中Na2SnO3的溶解度随温度变化如图。

①相同温度下,Na2SnO3的溶解度随NaOH浓度增大而减小,结合平衡移动原理解释原因:
②操作Ⅲ的具体方法为
(4)测定粗锡中Sn的纯度:在强酸性环境中将a g粗锡样品溶解(此时Sn全部转化成Sn2+),迅速加入过量NH4Fe(SO4)2溶液,以二苯胺磺酸钠为指示剂,用0.1000mol/L K2Cr2O7标准溶液滴定至终点。消耗K2Cr2O7溶液的体积如图所示,计算Sn的纯度。
已知: Sn2++2Fe3+=Sn4++2Fe2+;Cr2O
 +6Fe2++14H+=2Cr3++6Fe3++7H2O
+6Fe2++14H+=2Cr3++6Fe3++7H2O
①溶解粗锡时不宜选用浓盐酸,理由是
②二苯胺磺酸钠是一种氧化还原指示剂,滴定终点时因发生
③滴定终点时消耗K2Cr2O7标准溶液体积
④下列操作会导致样品中Sn的测定结果偏高的是
a.上述实验中若缓慢加入NH4Fe(SO4)2溶液
b.盛标准K2Cr2O7标准溶液的滴定管尖嘴部分有气泡未排除就开始滴定
c.实验用的酸式滴定管、锥形瓶水洗后均未润洗
您最近一年使用:0次
名校
解题方法
3 . 钴是元素周期表第四周期第Ⅷ族元素,其化合物用途广泛。如: 作锂电池的正极材料。
作锂电池的正极材料。
I.(1)基态Co原子的价层电子排布式为_______ 。
II.利用原钴矿 (含
(含 、NiS等杂质)制备
、NiS等杂质)制备 的工艺流程如下:
的工艺流程如下:
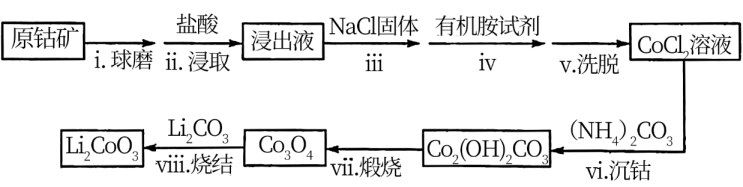
资料:①在含一定量 的溶液中:
的溶液中: 。
。
②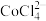 溶于有机胺试剂,有机胺不溶于水。
溶于有机胺试剂,有机胺不溶于水。
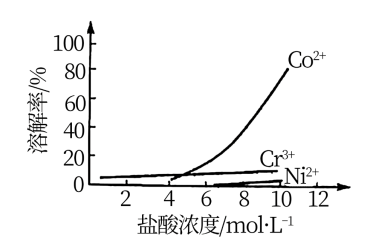
③盐酸溶液中,有机胺试剂对金属离子的溶解率随盐酸浓度变化如图所示:
(2)步骤i的目的是_______ 。
(3)步骤ii中出现了淡黄色沉淀,写出发生该反应的离子方程式:_______ 。
(4)从平衡移动角度解释步骤iii中加入NaCl固体的目的是_______ 。
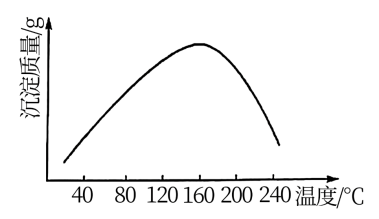
(5)步骤vi用 作沉钴剂,在一定条件下得到碱式碳酸钴
作沉钴剂,在一定条件下得到碱式碳酸钴 。实验测得在一段时间内加入等量
。实验测得在一段时间内加入等量 所得沉淀质量随反应温度的变化如图所示,分析曲线下降的原因
所得沉淀质量随反应温度的变化如图所示,分析曲线下降的原因___ 。
(6)步骤vi沉钴中(常温下进行),若滤液中 含量为
含量为 ,此时溶液的pH为
,此时溶液的pH为___ 。
(7)步骤viii中 和
和 混合后,鼓入空气,经高温烧结得到
混合后,鼓入空气,经高温烧结得到 。该反应的化学方程式是
。该反应的化学方程式是_______ 。
 作锂电池的正极材料。
作锂电池的正极材料。I.(1)基态Co原子的价层电子排布式为
II.利用原钴矿
 (含
(含 、NiS等杂质)制备
、NiS等杂质)制备 的工艺流程如下:
的工艺流程如下:
资料:①在含一定量
 的溶液中:
的溶液中: 。
。②
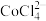 溶于有机胺试剂,有机胺不溶于水。
溶于有机胺试剂,有机胺不溶于水。③盐酸溶液中,有机胺试剂对金属离子的溶解率随盐酸浓度变化如图所示:

(2)步骤i的目的是
(3)步骤ii中出现了淡黄色沉淀,写出发生该反应的离子方程式:
(4)从平衡移动角度解释步骤iii中加入NaCl固体的目的是
(5)步骤vi用
 作沉钴剂,在一定条件下得到碱式碳酸钴
作沉钴剂,在一定条件下得到碱式碳酸钴 。实验测得在一段时间内加入等量
。实验测得在一段时间内加入等量 所得沉淀质量随反应温度的变化如图所示,分析曲线下降的原因
所得沉淀质量随反应温度的变化如图所示,分析曲线下降的原因
(6)步骤vi沉钴中(常温下进行),若滤液中
 含量为
含量为 ,此时溶液的pH为
,此时溶液的pH为
(7)步骤viii中
 和
和 混合后,鼓入空气,经高温烧结得到
混合后,鼓入空气,经高温烧结得到 。该反应的化学方程式是
。该反应的化学方程式是
您最近一年使用:0次
2021-03-04更新
|
253次组卷
|
2卷引用:辽宁省名校联盟2021届高三3月联合考试化学试题



