解题方法
1 . 三甲基镓 是一种重要的半导体材料前驱体。实验室以镓镁合金
是一种重要的半导体材料前驱体。实验室以镓镁合金 、碘甲烷
、碘甲烷 为原料制备
为原料制备 ,实验步骤及装置如图:
,实验步骤及装置如图:
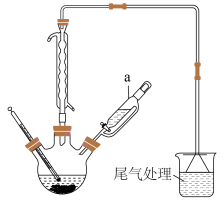
向三颈烧瓶中加入镓镁合金、碘甲烷和乙醚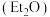 ,加热(55℃)并搅拌
,加热(55℃)并搅拌 。蒸出低沸点有机物后减压蒸馏,收集
。蒸出低沸点有机物后减压蒸馏,收集 。向
。向 中逐滴滴加
中逐滴滴加 (三正辛胺),室温下搅拌
(三正辛胺),室温下搅拌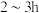 ,并用真空泵不断抽出
,并用真空泵不断抽出 蒸气,制得
蒸气,制得 。将
。将 置于真空中加热,蒸出
置于真空中加热,蒸出 。
。
已知:①常温下, 为无色透明的液体,易水解,在空气中易自燃。
为无色透明的液体,易水解,在空气中易自燃。
②相关物质的沸点信息如表:
回答下列问题:
(1)仪器a的名称是_______ ;制备 时,需在真空中加热的原因是
时,需在真空中加热的原因是_______ 。
(2)三颈烧瓶中除生成 外,还有
外,还有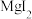 和
和 生成,该反应的化学方程式为
生成,该反应的化学方程式为_______ 。
(3)用真空泵不断抽出 蒸气,有利于
蒸气,有利于 生成的理由是
生成的理由是_______ (用平衡移动原理解释);与直接分解 制备
制备 相比,采用“
相比,采用“ 配体交换”工艺制备的产品纯度更高的原因是
配体交换”工艺制备的产品纯度更高的原因是_______ 。
(4)测定 产品的纯度。取
产品的纯度。取 样品于锥形瓶中,加入
样品于锥形瓶中,加入 盐酸,至不再产生气泡,加入2滴甲基橙,用
盐酸,至不再产生气泡,加入2滴甲基橙,用 溶液滴定剩余盐酸,消耗
溶液滴定剩余盐酸,消耗 溶液的体积为
溶液的体积为 ,则
,则 的质量分数为
的质量分数为_______ (用含m、V、 、c、
、c、 的代数式表示);若滴定达终点时发现滴定管尖嘴内有气泡生成,则测定结果
的代数式表示);若滴定达终点时发现滴定管尖嘴内有气泡生成,则测定结果_______ (填“偏高”“偏低”或“无影响”)。
 是一种重要的半导体材料前驱体。实验室以镓镁合金
是一种重要的半导体材料前驱体。实验室以镓镁合金 、碘甲烷
、碘甲烷 为原料制备
为原料制备 ,实验步骤及装置如图:
,实验步骤及装置如图:
向三颈烧瓶中加入镓镁合金、碘甲烷和乙醚
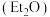 ,加热(55℃)并搅拌
,加热(55℃)并搅拌 。蒸出低沸点有机物后减压蒸馏,收集
。蒸出低沸点有机物后减压蒸馏,收集 。向
。向 中逐滴滴加
中逐滴滴加 (三正辛胺),室温下搅拌
(三正辛胺),室温下搅拌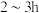 ,并用真空泵不断抽出
,并用真空泵不断抽出 蒸气,制得
蒸气,制得 。将
。将 置于真空中加热,蒸出
置于真空中加热,蒸出 。
。已知:①常温下,
 为无色透明的液体,易水解,在空气中易自燃。
为无色透明的液体,易水解,在空气中易自燃。②相关物质的沸点信息如表:
| 物质 |  |  |  |  |
| 沸点/℃ | 55.8 | 40.3 | 34.5 | 365.8 |
(1)仪器a的名称是
 时,需在真空中加热的原因是
时,需在真空中加热的原因是(2)三颈烧瓶中除生成
 外,还有
外,还有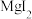 和
和 生成,该反应的化学方程式为
生成,该反应的化学方程式为(3)用真空泵不断抽出
 蒸气,有利于
蒸气,有利于 生成的理由是
生成的理由是 制备
制备 相比,采用“
相比,采用“ 配体交换”工艺制备的产品纯度更高的原因是
配体交换”工艺制备的产品纯度更高的原因是(4)测定
 产品的纯度。取
产品的纯度。取 样品于锥形瓶中,加入
样品于锥形瓶中,加入 盐酸,至不再产生气泡,加入2滴甲基橙,用
盐酸,至不再产生气泡,加入2滴甲基橙,用 溶液滴定剩余盐酸,消耗
溶液滴定剩余盐酸,消耗 溶液的体积为
溶液的体积为 ,则
,则 的质量分数为
的质量分数为 、c、
、c、 的代数式表示);若滴定达终点时发现滴定管尖嘴内有气泡生成,则测定结果
的代数式表示);若滴定达终点时发现滴定管尖嘴内有气泡生成,则测定结果
您最近一年使用:0次
名校
解题方法
2 . 我国冶铅工艺迅猛发展,底吹炉烟灰中除含有主金属铅外,还含有锌、镉(Cd)等有价金属元素,一种对该烟灰中有价金属综合回收工艺研究如下:

已知:Ⅰ.
①As元素以砷酸盐( )形式存在;
)形式存在;
②Pb元素主要以PbO和PbSO4形式存在,不溶于水;
③Cd元素主要以CdSO4形式存在,CdSO4易溶于水。
Ⅱ.水浸液初始pH=2~3;滤渣①返回冶铅系统;滤渣②主要成分为FeAsO4。
回答下列问题:
(1)为提高“水浸”效率,可以采取的措施有_______ (任写一条)。
(2)为提高铅和镉的回收率,需综合分析浸出率、渣含金属、渣率。
根据以上实验数据选择合适的液固比和温度:_______ ,理由:_______ 。
(3)“中和除砷”阶段主要反应的离子方程式为_______ 。该工序最终需加入试剂①调节溶液pH=5,下列最合适的是_______ (填序号)。
A.NaOH B.NH3·H2O C.Zn2O D.H2SO4
(4)“电解”过程中阴极的电极反应式为_______ 。

已知:Ⅰ.
| 底吹炉含镉烟灰的主要化学成分 |  |  |  |  |  |  |
| 质量分数/% | 37.40 | 15.88 | 2.51 | 0.15 | 0.28 | 0.15 |
 )形式存在;
)形式存在;②Pb元素主要以PbO和PbSO4形式存在,不溶于水;
③Cd元素主要以CdSO4形式存在,CdSO4易溶于水。
Ⅱ.水浸液初始pH=2~3;滤渣①返回冶铅系统;滤渣②主要成分为FeAsO4。
回答下列问题:
(1)为提高“水浸”效率,可以采取的措施有
(2)为提高铅和镉的回收率,需综合分析浸出率、渣含金属、渣率。
| 温度/℃ | 浸出率/% | 渣含金属 | 渣率/℃ | |||
 |  |  |  |  | ||
| 25 | 86.06 | 65.48 | 55.48 | 3.27 | 1.28 | 67.69 |
| 45 | 84.19 | 63.95 | 54.63 | 3.69 | 1.33 | 68.04 |
| 65 | 85.51 | 62.45 | 55.63 | 3.37 | 1.38 | 68.30 |
| 85 | 84.15 | 65.08 | 54.70 | 3.82 | 1.33 | 65.90 |
| 液固比 | 浸出率/% | 渣含金属 | 渣率/℃ | |||
 |  |  |  |  | ||
| 1:1 | 75.22 | 54.65 | 51.26 | 5.29 | 1.53 | 74.39 |
| 2:1 | 80.59 | 58.62 | 53.98 | 4.28 | 1.47 | 70.66 |
| 3:1 | 85.51 | 62.45 | 55.63 | 3.37 | 1.38 | 68.30 |
| 4:1 | 86.82 | 65.02 | 57.06 | 3.14 | 1.32 | 66.52 |
(3)“中和除砷”阶段主要反应的离子方程式为
A.NaOH B.NH3·H2O C.Zn2O D.H2SO4
(4)“电解”过程中阴极的电极反应式为
您最近一年使用:0次
名校
3 . 下列关于化学反应速率和化学平衡的说法正确的是
| A.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加单位体积内活化分子百分数,从而使反应速率增大 |
B.已知反应: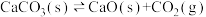 ,在密闭的反应炉内达到平衡后,若其他条件均不改变,将反应炉体积缩小一半,则达到新平衡时 ,在密闭的反应炉内达到平衡后,若其他条件均不改变,将反应炉体积缩小一半,则达到新平衡时 的浓度将升高 的浓度将升高 |
C.在一定温度下,容积一定的密闭容器中的反应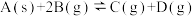 ,当混合气体的压强不变时,则表明该反应已达平衡 ,当混合气体的压强不变时,则表明该反应已达平衡 |
D.在一定条件下,可逆反应  达到平衡后。保持容器温度和容积不变,再通入一定量 达到平衡后。保持容器温度和容积不变,再通入一定量 ,则再次达到平衡时 ,则再次达到平衡时 的百分含量减小 的百分含量减小 |
您最近一年使用:0次
2022-12-09更新
|
685次组卷
|
5卷引用:山东省济南市历城第二中学2022-2023学年高二上学期期末线上测试化学试题



