解题方法
1 . 三甲基镓 是一种重要的半导体材料前驱体。实验室以镓镁合金
是一种重要的半导体材料前驱体。实验室以镓镁合金 、碘甲烷
、碘甲烷 为原料制备
为原料制备 ,实验步骤及装置如图:
,实验步骤及装置如图:
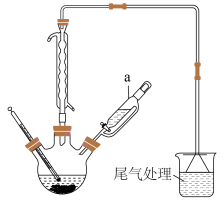
向三颈烧瓶中加入镓镁合金、碘甲烷和乙醚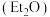 ,加热(55℃)并搅拌
,加热(55℃)并搅拌 。蒸出低沸点有机物后减压蒸馏,收集
。蒸出低沸点有机物后减压蒸馏,收集 。向
。向 中逐滴滴加
中逐滴滴加 (三正辛胺),室温下搅拌
(三正辛胺),室温下搅拌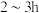 ,并用真空泵不断抽出
,并用真空泵不断抽出 蒸气,制得
蒸气,制得 。将
。将 置于真空中加热,蒸出
置于真空中加热,蒸出 。
。
已知:①常温下, 为无色透明的液体,易水解,在空气中易自燃。
为无色透明的液体,易水解,在空气中易自燃。
②相关物质的沸点信息如表:
回答下列问题:
(1)仪器a的名称是_______ ;制备 时,需在真空中加热的原因是
时,需在真空中加热的原因是_______ 。
(2)三颈烧瓶中除生成 外,还有
外,还有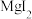 和
和 生成,该反应的化学方程式为
生成,该反应的化学方程式为_______ 。
(3)用真空泵不断抽出 蒸气,有利于
蒸气,有利于 生成的理由是
生成的理由是_______ (用平衡移动原理解释);与直接分解 制备
制备 相比,采用“
相比,采用“ 配体交换”工艺制备的产品纯度更高的原因是
配体交换”工艺制备的产品纯度更高的原因是_______ 。
(4)测定 产品的纯度。取
产品的纯度。取 样品于锥形瓶中,加入
样品于锥形瓶中,加入 盐酸,至不再产生气泡,加入2滴甲基橙,用
盐酸,至不再产生气泡,加入2滴甲基橙,用 溶液滴定剩余盐酸,消耗
溶液滴定剩余盐酸,消耗 溶液的体积为
溶液的体积为 ,则
,则 的质量分数为
的质量分数为_______ (用含m、V、 、c、
、c、 的代数式表示);若滴定达终点时发现滴定管尖嘴内有气泡生成,则测定结果
的代数式表示);若滴定达终点时发现滴定管尖嘴内有气泡生成,则测定结果_______ (填“偏高”“偏低”或“无影响”)。
 是一种重要的半导体材料前驱体。实验室以镓镁合金
是一种重要的半导体材料前驱体。实验室以镓镁合金 、碘甲烷
、碘甲烷 为原料制备
为原料制备 ,实验步骤及装置如图:
,实验步骤及装置如图:
向三颈烧瓶中加入镓镁合金、碘甲烷和乙醚
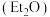 ,加热(55℃)并搅拌
,加热(55℃)并搅拌 。蒸出低沸点有机物后减压蒸馏,收集
。蒸出低沸点有机物后减压蒸馏,收集 。向
。向 中逐滴滴加
中逐滴滴加 (三正辛胺),室温下搅拌
(三正辛胺),室温下搅拌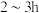 ,并用真空泵不断抽出
,并用真空泵不断抽出 蒸气,制得
蒸气,制得 。将
。将 置于真空中加热,蒸出
置于真空中加热,蒸出 。
。已知:①常温下,
 为无色透明的液体,易水解,在空气中易自燃。
为无色透明的液体,易水解,在空气中易自燃。②相关物质的沸点信息如表:
| 物质 |  |  |  |  |
| 沸点/℃ | 55.8 | 40.3 | 34.5 | 365.8 |
(1)仪器a的名称是
 时,需在真空中加热的原因是
时,需在真空中加热的原因是(2)三颈烧瓶中除生成
 外,还有
外,还有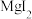 和
和 生成,该反应的化学方程式为
生成,该反应的化学方程式为(3)用真空泵不断抽出
 蒸气,有利于
蒸气,有利于 生成的理由是
生成的理由是 制备
制备 相比,采用“
相比,采用“ 配体交换”工艺制备的产品纯度更高的原因是
配体交换”工艺制备的产品纯度更高的原因是(4)测定
 产品的纯度。取
产品的纯度。取 样品于锥形瓶中,加入
样品于锥形瓶中,加入 盐酸,至不再产生气泡,加入2滴甲基橙,用
盐酸,至不再产生气泡,加入2滴甲基橙,用 溶液滴定剩余盐酸,消耗
溶液滴定剩余盐酸,消耗 溶液的体积为
溶液的体积为 ,则
,则 的质量分数为
的质量分数为 、c、
、c、 的代数式表示);若滴定达终点时发现滴定管尖嘴内有气泡生成,则测定结果
的代数式表示);若滴定达终点时发现滴定管尖嘴内有气泡生成,则测定结果
您最近半年使用:0次
名校
解题方法
2 . 我国冶铅工艺迅猛发展,底吹炉烟灰中除含有主金属铅外,还含有锌、镉(Cd)等有价金属元素,一种对该烟灰中有价金属综合回收工艺研究如下:

已知:Ⅰ.
①As元素以砷酸盐( )形式存在;
)形式存在;
②Pb元素主要以PbO和PbSO4形式存在,不溶于水;
③Cd元素主要以CdSO4形式存在,CdSO4易溶于水。
Ⅱ.水浸液初始pH=2~3;滤渣①返回冶铅系统;滤渣②主要成分为FeAsO4。
回答下列问题:
(1)为提高“水浸”效率,可以采取的措施有_______ (任写一条)。
(2)为提高铅和镉的回收率,需综合分析浸出率、渣含金属、渣率。
根据以上实验数据选择合适的液固比和温度:_______ ,理由:_______ 。
(3)“中和除砷”阶段主要反应的离子方程式为_______ 。该工序最终需加入试剂①调节溶液pH=5,下列最合适的是_______ (填序号)。
A.NaOH B.NH3·H2O C.Zn2O D.H2SO4
(4)“电解”过程中阴极的电极反应式为_______ 。

已知:Ⅰ.
| 底吹炉含镉烟灰的主要化学成分 |  |  |  |  |  |  |
| 质量分数/% | 37.40 | 15.88 | 2.51 | 0.15 | 0.28 | 0.15 |
 )形式存在;
)形式存在;②Pb元素主要以PbO和PbSO4形式存在,不溶于水;
③Cd元素主要以CdSO4形式存在,CdSO4易溶于水。
Ⅱ.水浸液初始pH=2~3;滤渣①返回冶铅系统;滤渣②主要成分为FeAsO4。
回答下列问题:
(1)为提高“水浸”效率,可以采取的措施有
(2)为提高铅和镉的回收率,需综合分析浸出率、渣含金属、渣率。
| 温度/℃ | 浸出率/% | 渣含金属 | 渣率/℃ | |||
 |  |  |  |  | ||
| 25 | 86.06 | 65.48 | 55.48 | 3.27 | 1.28 | 67.69 |
| 45 | 84.19 | 63.95 | 54.63 | 3.69 | 1.33 | 68.04 |
| 65 | 85.51 | 62.45 | 55.63 | 3.37 | 1.38 | 68.30 |
| 85 | 84.15 | 65.08 | 54.70 | 3.82 | 1.33 | 65.90 |
| 液固比 | 浸出率/% | 渣含金属 | 渣率/℃ | |||
 |  |  |  |  | ||
| 1:1 | 75.22 | 54.65 | 51.26 | 5.29 | 1.53 | 74.39 |
| 2:1 | 80.59 | 58.62 | 53.98 | 4.28 | 1.47 | 70.66 |
| 3:1 | 85.51 | 62.45 | 55.63 | 3.37 | 1.38 | 68.30 |
| 4:1 | 86.82 | 65.02 | 57.06 | 3.14 | 1.32 | 66.52 |
(3)“中和除砷”阶段主要反应的离子方程式为
A.NaOH B.NH3·H2O C.Zn2O D.H2SO4
(4)“电解”过程中阴极的电极反应式为
您最近半年使用:0次
名校
3 . KSCN是实验室常用的化学试剂。
(1)探究KCl浓度对Fe3+与SCN-显色反应的影响
将25mL0.005mol•L-1FeCl3与25mL0.01mol•L-1KSCN溶液混合得红色溶液,各取3mL溶液分别加KCl晶体进行透光实验,结果如图所示。
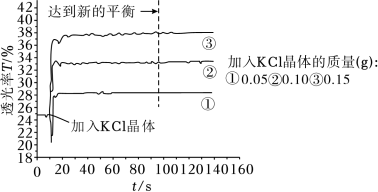
已知:i.溶液颜色越浅,透光率(T)越高;
ii.FeCl3溶液中存在Fe3++4Cl- [FeCl4]-(黄色)。
[FeCl4]-(黄色)。
①采用FeCl3稀溶液是为了避免_______ (填离子符号)的颜色对实验干扰。
②由实验结果分析,随着KCl浓度增大,Fe(SCN)3的浓度_______ (填“增大”“减小”或“不变”),从平衡移动的角度分析可能的原因_______ 。
(2)探究KSCN在铜含量测定过程中的作用
步骤如下:取1.0g铜盐样品溶于稀盐酸配成250mL溶液,取10.00mL加入过量KI充分反应,用0.0100mol•L-1的Na2S2O3标准液滴定至终点。
已知:i.2Cu2++4I-=2CuI↓+I2;2S2O +I2=S4O
+I2=S4O +2I-;
+2I-;
ii.I2+I- I
I ,CuI沉淀强烈吸附I
,CuI沉淀强烈吸附I ;
;
iii.Ksp(CuI)=1.0×10-12;Ksp(CuSCN)=4.8×10-15
①以淀粉为指示剂,滴定终点的颜色变化为_______ ;根据信息预测最终测定的结果将_______ (填“偏大”“偏小”或“无影响”)。
②通过实验探究,在滴定过程中加入KSCN可使测定结果更准确,写出发生反应的离子方程式_______ ;到达滴定终点时消耗标准液20.00mL,样品中铜元素质量分数为_______ ,滴定后仍存在少量CuI沉淀,测得溶液中c(I-)=0.2mol•L-1,则c(SCN-)=_______ 。
(1)探究KCl浓度对Fe3+与SCN-显色反应的影响
将25mL0.005mol•L-1FeCl3与25mL0.01mol•L-1KSCN溶液混合得红色溶液,各取3mL溶液分别加KCl晶体进行透光实验,结果如图所示。

已知:i.溶液颜色越浅,透光率(T)越高;
ii.FeCl3溶液中存在Fe3++4Cl-
 [FeCl4]-(黄色)。
[FeCl4]-(黄色)。①采用FeCl3稀溶液是为了避免
②由实验结果分析,随着KCl浓度增大,Fe(SCN)3的浓度
(2)探究KSCN在铜含量测定过程中的作用
步骤如下:取1.0g铜盐样品溶于稀盐酸配成250mL溶液,取10.00mL加入过量KI充分反应,用0.0100mol•L-1的Na2S2O3标准液滴定至终点。
已知:i.2Cu2++4I-=2CuI↓+I2;2S2O
 +I2=S4O
+I2=S4O +2I-;
+2I-;ii.I2+I-
 I
I ,CuI沉淀强烈吸附I
,CuI沉淀强烈吸附I ;
;iii.Ksp(CuI)=1.0×10-12;Ksp(CuSCN)=4.8×10-15
①以淀粉为指示剂,滴定终点的颜色变化为
②通过实验探究,在滴定过程中加入KSCN可使测定结果更准确,写出发生反应的离子方程式
您最近半年使用:0次
2024-04-05更新
|
51次组卷
|
3卷引用:山东省青岛第十五中学2023-2024学年高二下学期期初考试化学试卷
4 . 以硅藻土为载体的五氧化二钒(V2O5)是接触法生产硫酸的催化剂。从废矾催化剂中回收V2O5既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为
如图是一种废钒催化剂回收工艺路线:
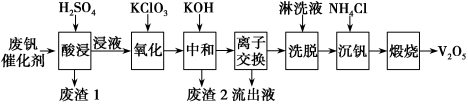
回答下列问题:
(1)已知“酸浸”时,V2O5转化为VO ,V2O4转化成VO2+,请写出废钒催化剂“酸浸”时V2O5发生反应的离子方程式
,V2O4转化成VO2+,请写出废钒催化剂“酸浸”时V2O5发生反应的离子方程式___________ 。
(2)工艺中“氧化”步骤使VO2+变为VO 反应的离子方程式
反应的离子方程式___________ 。
(3)“离子交换”和“洗脱”可简单表示为4ROH+V4O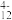
 R4V4O12+4OH-(ROH为强碱性阴离子交换树脂)。为了提高“洗脱”效率,“淋洗液”应该呈
R4V4O12+4OH-(ROH为强碱性阴离子交换树脂)。为了提高“洗脱”效率,“淋洗液”应该呈___________ (填“酸”“碱”或“中”)性。
(4)“流出液”中阳离子最多的是___________ 。
| 物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
| 质量分数/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |
如图是一种废钒催化剂回收工艺路线:

回答下列问题:
(1)已知“酸浸”时,V2O5转化为VO
 ,V2O4转化成VO2+,请写出废钒催化剂“酸浸”时V2O5发生反应的离子方程式
,V2O4转化成VO2+,请写出废钒催化剂“酸浸”时V2O5发生反应的离子方程式(2)工艺中“氧化”步骤使VO2+变为VO
 反应的离子方程式
反应的离子方程式(3)“离子交换”和“洗脱”可简单表示为4ROH+V4O
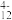
 R4V4O12+4OH-(ROH为强碱性阴离子交换树脂)。为了提高“洗脱”效率,“淋洗液”应该呈
R4V4O12+4OH-(ROH为强碱性阴离子交换树脂)。为了提高“洗脱”效率,“淋洗液”应该呈(4)“流出液”中阳离子最多的是
您最近半年使用:0次
名校
5 . 下列关于化学反应速率和化学平衡的说法正确的是
| A.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加单位体积内活化分子百分数,从而使反应速率增大 |
B.已知反应: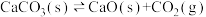 ,在密闭的反应炉内达到平衡后,若其他条件均不改变,将反应炉体积缩小一半,则达到新平衡时 ,在密闭的反应炉内达到平衡后,若其他条件均不改变,将反应炉体积缩小一半,则达到新平衡时 的浓度将升高 的浓度将升高 |
C.在一定温度下,容积一定的密闭容器中的反应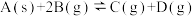 ,当混合气体的压强不变时,则表明该反应已达平衡 ,当混合气体的压强不变时,则表明该反应已达平衡 |
D.在一定条件下,可逆反应  达到平衡后。保持容器温度和容积不变,再通入一定量 达到平衡后。保持容器温度和容积不变,再通入一定量 ,则再次达到平衡时 ,则再次达到平衡时 的百分含量减小 的百分含量减小 |
您最近半年使用:0次
2022-12-09更新
|
678次组卷
|
5卷引用:山东省青岛第二中学2020-2021学年高二上学期期末化学试题
6 . 一定温度下,某气态平衡体系的平衡常数表达式为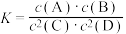 ,有关该平衡体系的说法正确的是
,有关该平衡体系的说法正确的是
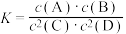 ,有关该平衡体系的说法正确的是
,有关该平衡体系的说法正确的是A.升高温度,平衡常数 一定增大 一定增大 | B.增大 浓度,平衡向正反应方向移动 浓度,平衡向正反应方向移动 |
C.增大压强, 体积分数增加 体积分数增加 | D.升高温度,若 的百分含量减少,则正反应是放热反应 的百分含量减少,则正反应是放热反应 |
您最近半年使用:0次
2021-10-15更新
|
133次组卷
|
3卷引用:山东省烟台市招远市第二中学2021-2022学年高二10月月考化学试题
山东省烟台市招远市第二中学2021-2022学年高二10月月考化学试题(已下线)必考点03 化学平衡-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版)四川省广安市育才学校2022-2023学年高二上学期11月期中考试化学试题
2022·河北石家庄·一模
解题方法
7 . 镁条投入盐酸时,快速溶解并产生大量气泡;投入热水时,其表面会附着微量气泡。受此启发,某兴趣小组对Mg与NaHCO3溶液的反应进行了如下探究:
I.探究反应产生的气体成分。
(1)经检验反应产生的气体有H2,实验室检验H2的方法为_______ 。
(2)小组成员认为反应产生的气体中可能有CO2,并对此进行了如下实验(图1、图2中曲线②均为对应加入镁条的数据):
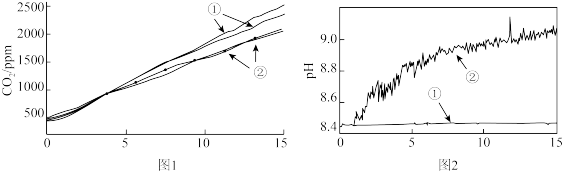
图1中曲线②对应的CO2含量逐渐增大的原因为_______ (用化学方程式表示);结合实验3解释,随着时间推移,图1中曲线②的数值低于曲线①的原因为_______ 。
II.探究Mg与NaHCO3溶液反应比与热水反应快的原因。
小组成员推测可能是溶液中的Na+或HCO 加快了该反应的发生,对比实验1设计实验如下:
加快了该反应的发生,对比实验1设计实验如下:
(3)结合实验1和4,可知溶液中的HCO 加快了反应的发生。
加快了反应的发生。
①实验4中横线处内容为_______ 。
②查阅文献可知,Mg(OH)2质地致密,MgCO3质地疏松,请结合必要的文字和化学用语解释HCO 能加快该反应的原因为
能加快该反应的原因为_______ 。
III.探究固体浑浊物的组成。
文献显示,固体浑浊物为Mg(OH)2和MgCO3的混合物。甲、乙两位同学设计不同方案,测定混合物组成。
(4)甲同学借助下图装置(可重复选用),通过测定固体热分解产物水及二氧化碳的质量,测定其组成。按照该方案,装置的连接顺序为_______ (填字母编号)。

(5)乙同学只测定了固体浑浊物在热分解前后的质量分别为3.42 g和2.00g,据此计算出固体浑浊物中n[Mg(OH)2]:n[MgCO3]=_______ 。
| 实验序号 | 实验操作 | 实验现象 |
| 1 | 向7.5 mL1mol·L-1NaHCO3溶液中加入长3cm的镁条 | 持续快速产生大量气泡,溶液略显浑浊 |
(1)经检验反应产生的气体有H2,实验室检验H2的方法为
(2)小组成员认为反应产生的气体中可能有CO2,并对此进行了如下实验(图1、图2中曲线②均为对应加入镁条的数据):
| 实验序号 | 实验操作 |
| 2 | 分别称取两份6.0 mL 1 mol·L-1NaHCO3溶液于两个相同塑料瓶中(其中一个加入0.1g镁条),塞紧CO2气体传感器,采集数据,各重复实验1次,得到图1所示曲线 |
| 3 | 分别称取两份30.0 mL 1 mol·L-1NaHCO3溶液于两个相同烧杯中(其中一个加入1.1g镁条),插入pH传感器,搅拌并采集数据,得到图2所示曲线 |

图1中曲线②对应的CO2含量逐渐增大的原因为
II.探究Mg与NaHCO3溶液反应比与热水反应快的原因。
小组成员推测可能是溶液中的Na+或HCO
 加快了该反应的发生,对比实验1设计实验如下:
加快了该反应的发生,对比实验1设计实验如下:| 实验序号 | 实验操作 | 实验现象 |
| 4 | 向_______溶液中加入长3 cm的镁条 | 持续快速产生大量气泡,溶液略显浑浊 |
 加快了反应的发生。
加快了反应的发生。①实验4中横线处内容为
②查阅文献可知,Mg(OH)2质地致密,MgCO3质地疏松,请结合必要的文字和化学用语解释HCO
 能加快该反应的原因为
能加快该反应的原因为III.探究固体浑浊物的组成。
文献显示,固体浑浊物为Mg(OH)2和MgCO3的混合物。甲、乙两位同学设计不同方案,测定混合物组成。
(4)甲同学借助下图装置(可重复选用),通过测定固体热分解产物水及二氧化碳的质量,测定其组成。按照该方案,装置的连接顺序为

(5)乙同学只测定了固体浑浊物在热分解前后的质量分别为3.42 g和2.00g,据此计算出固体浑浊物中n[Mg(OH)2]:n[MgCO3]=
您最近半年使用:0次
2022-04-09更新
|
1130次组卷
|
7卷引用:化学-2022年高考押题预测卷03(山东卷)
(已下线)化学-2022年高考押题预测卷03(山东卷)河北省石家庄市2022届高三毕业班教学质量检测二(一模)化学试题(已下线)专项14 化学实验综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)(已下线)秘籍21 性质探究实验-备战2022年高考化学抢分秘籍(全国通用)(已下线)化学-2022年高考押题预测卷01(福建卷)(已下线)押江苏卷第17题 化学实验综合题 -备战2022年高考化学临考题号押题(江苏卷)(已下线)河北省石家庄市2022届高三毕业班教学质量检测二(一模)(实验探究题)
8 . 工业合成氨是人工固研究的重要领域。回答下列问题:
(1)如图所示是电解法合成氨反应装置示意图
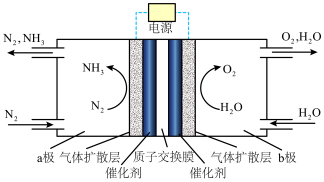
则b极为___________ (填“阴”或“阳”)极,a极的电极反应式为___________ ,电解装置中质子交换膜的作用为___________ ;若b极产生的O2在一定条件下的体积为336L,a极中通入相同条件下N2的总体积为672L,则N2的转化率为___________ %(保留两位有效数字)。
(2)合成氨反应的一种反应机理的相对能量—反应进程如下图所示,其中标有“*”的微粒为吸附态(图中“*H”均未标出)。
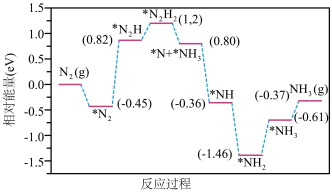
则各步反应中决定合成氨反应速率的反应方程式为___________
(3)当氮气和氢气的比例为1:3时,工业合成氨所得混合气体中,氨气的含量与温度、压强的关系如下
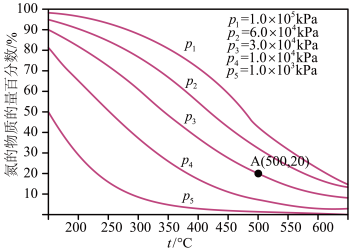
①平衡曲线上A点的平衡常数
___________ (用含 的式子表示)
的式子表示)
②工业实际生产投料时,氮气与氢气的体积比为1:2.8,适当增加氮气的比重的目的是___________ 。
(1)如图所示是电解法合成氨反应装置示意图

则b极为
(2)合成氨反应的一种反应机理的相对能量—反应进程如下图所示,其中标有“*”的微粒为吸附态(图中“*H”均未标出)。

则各步反应中决定合成氨反应速率的反应方程式为
(3)当氮气和氢气的比例为1:3时,工业合成氨所得混合气体中,氨气的含量与温度、压强的关系如下

①平衡曲线上A点的平衡常数

 的式子表示)
的式子表示)②工业实际生产投料时,氮气与氢气的体积比为1:2.8,适当增加氮气的比重的目的是
您最近半年使用:0次
9 . 一定温度下,在带活塞的密闭容器中,反应H2(g) +I2(g) 2HI(g)(△H〈0)达到平衡后,下列说法不正确的是
2HI(g)(△H〈0)达到平衡后,下列说法不正确的是
 2HI(g)(△H〈0)达到平衡后,下列说法不正确的是
2HI(g)(△H〈0)达到平衡后,下列说法不正确的是 | A.恒容时,升高温度,平衡向逆反应方向移动,正反应速率减小 |
| B.恒温时,减小容积平衡不移动,但气体颜色加深 |
| C.恒容时,通入H2,I2的质量分数减小 |
| D.恒压时,通入HI气体,刚开始时正反应速率会减小 |
您最近半年使用:0次
名校
解题方法
10 . 在催化剂作用下,向刚性容器中按物质的量比1︰1充入甲醇和异丁烯(用R表示),分别在T1和T2两个温度下发生反应生成有机物W:CH3OH(g)+R(g)⇌W(g) ΔH。异丁烯的转化率随时间的变化关系如图所示。下列说法正确的是
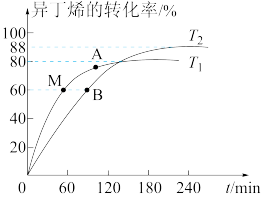

| A.T1>T2,ΔH>0 |
| B.vM正=vB正>vA逆 |
| C.维持T2不变,再向容器中充入1 mol W,新平衡时W的百分含量减小 |
D.T1时,容器内起始总压为p0 kPa,则用分压表示的该反应的平衡常数Kp= kPa-1 kPa-1 |
您最近半年使用:0次
2021-03-07更新
|
1331次组卷
|
8卷引用:山东省济南市平阴县第一中学2021届高三下学期3月月考化学试题
山东省济南市平阴县第一中学2021届高三下学期3月月考化学试题重庆市强基联合体2021届高三下学期质量检测化学试题河南省鹤壁市高中2020-2021学年高二下学期第三次段考化学试题(已下线)考点17 化学反应速率及其影响因素-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点17 化学反应速率及其影响因素-备战2022年高考化学一轮复习考点帮(浙江专用)安徽省马鞍山市第二中学2021-2022学年高二上学期期中考试化学试题(已下线)专题10 化学反应速率与平衡-2023年高考化学一轮复习小题多维练(全国通用)重庆市第一中学校2020-2021学年高二下学期期末考试化学试题



