名校
1 . 下列实验目的对应的方案设计、现象和结论都正确的是
| 选项 | 实验目的 | 方案设计 | 现象和结论 |
| A | 比较 和 和 的 的 相对大小 相对大小 | 向等体积饱和 溶液和饱和 溶液和饱和 溶液中分别滴加等量的浓 溶液中分别滴加等量的浓 溶液 溶液 | 得到沉淀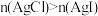 ,则 ,则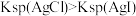 |
| B | 探究压强对平衡移动的影响 | 密闭容器中盛装 ,一段时间后反应达平衡,压缩体积至原来的一半 ,一段时间后反应达平衡,压缩体积至原来的一半 | 气体颜色加深,说明平衡向生成 的方向移动 的方向移动 |
| C | 比较 与 与 的酸性 的酸性 | 用 计测定 计测定 :① :① 溶液② 溶液② 溶液 溶液 |  :①>②,证明 :①>②,证明 的酸性弱于 的酸性弱于 |
| D | 比较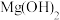 和 和 的 的 相对大小 相对大小 | 向 的 的 溶液中滴加2滴 溶液中滴加2滴 的 的 溶液,再滴加2滴 溶液,再滴加2滴 的 的 溶液 溶液 | 先生成白色沉淀,后生成红褐色沉淀,证明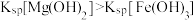 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2 . 下列实验能达到预期目的的实验个数是
| 编号 | 实验内容 | 实验目的 |
| ① | 室温下,用pH试纸分别测定浓度相等的NaClO溶液和NaHCO3溶液的pH | 比较HClO与H2CO3的酸性强弱 |
| ② | 往含有酚酞的Na2CO3溶液中,加入少量CaCl2晶体,现象溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| ③ | 配制FeCl2溶液时,先将FeCl2溶于适量浓盐酸中,再用蒸馏水稀释到所需浓度,最后在试剂瓶中加入少量铁粉 | 抑制Fe2+水解,并防止Fe2+被氧化 |
| ④ | 快速压缩装有NO2、N2O4平衡混合气体的针筒活塞,平衡后气体颜色变深 | 探究压强对化学平衡的影响 |
| A.1 | B.2 | C.3 | D.4 |
您最近半年使用:0次
3 . 下列实验装置或操作不能达到实验目的的是
|
|
| A.蒸干AlCl3溶液制备AlCl3固体 | B.测定中和反应的反应热 |
|
|
| C.探究压强对平衡的影响 | D.分离碘和氯化钠固体 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
4 . 下列实验中,对现象的解释不正确 的是
| 选项 | A | B |
| 装置及操作 |  向右轻轻推动活塞压缩体积 | 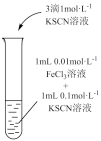 |
| 现象 | 气体红棕色先变深再变浅 | 溶液血红色加深 |
| 解释 | 压强增大, 平衡先逆向移动,再正向移动 平衡先逆向移动,再正向移动 | 增大反应物浓度,  平衡正向移动 平衡正向移动 |
| 选项 | C | D |
| 装置及操作 |  分别测定20℃和80℃蒸馏水的电导率 |  |
| 现象 | 80℃蒸馏水的电导率大于20℃的 | 加入 粉末后电导率增大 粉末后电导率增大 |
| 解释 | 温度升高,水的电离平衡正向移动 |  在水中存在 在水中存在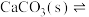  |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
5 . 下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象与结论 | |
| A | 验证压强对化学平衡的影响 | 先将注射器充满NO2气体,然后将活塞往里推压缩体积 | 观察到注射器内气体颜色加深,证明加压平衡朝生成NO2气体的方向移动 |
| B | 铜的电解精炼 | 待精炼的铜和纯铜连接外加直流电源的阳极和阴极,用硫酸铜溶液作电解质电解 | 阳极上铜逐渐溶解,阴极上铜逐渐析出,硫酸铜溶液浓度保持不变 |
| C | 制备[Cu(NH3)4]SO4·H2O晶体 | 向4mL 0.1mol/LCuSO4溶液中滴加氨水,先形成难溶物,并继续滴加沉淀溶解,然后蒸发溶剂析出晶体 | 反应过程中,NH3的N给出孤对电子,Cu2+接受电子对,形成了稳定的配位键[Cu(NH3)4]2+ |
| D | 除去锅炉水垢中的CaSO4 | 先用碳酸钠溶液浸泡水垢,然后再用盐酸除去 | 利用Ksp(CaSO4)> Ksp(CaCO3),实现沉淀的转化 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2022-01-21更新
|
404次组卷
|
4卷引用:河北鸡泽县第一中学2021-2022学年高二下学期开学考试化学试题
河北鸡泽县第一中学2021-2022学年高二下学期开学考试化学试题浙江省温州市2021-2022学年高二上学期期末教学质量统一检测化学试题(已下线)3.4 配合物与超分子-2021-2022学年高二化学课后培优练(人教版2019选择性必修2)浙江省富阳区第二中学2021-2022学年高二下学期(3月)检测化学试题
名校
解题方法
6 . NH3经如图所示一系列反应可以得到HNO3。
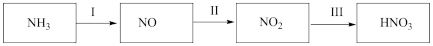
(1)步骤I中,NH3和O2在催化剂作用下反应,其化学方程式是___________ 。
(2)步骤II中,2NO(g)+O2(g) 2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强( p1、p2)下随温度变化的曲线(如图)。
2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强( p1、p2)下随温度变化的曲线(如图)。

①比较p1、p2的大小关系:___________ 。
②随温度升高,该反应平衡常数变化的趋势是___________ 。
(3)步骤III中,先降低温度,将NO2(g)转化为N2O4(l),再制备浓硝酸。
①已知:2NO2(g) N2O4(g) △H1
N2O4(g) △H1
2NO2(g) N2O4(l) △H2
N2O4(l) △H2
下列能量变化示意图中,正确的是___________ (填字母)。
A.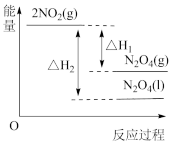 B.
B. 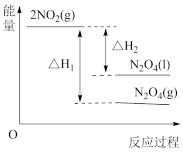 C.
C. 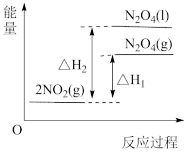
②N2O4与O2、H2O化合的化学方程式是___________ 。
(4)一种利用垃圾渗滤液中NH3、NH 发电的原理如图所示。
发电的原理如图所示。

①X为该装置的___________ 极。
②该装置工作时, Y电极周围溶液的pH___________ (填“ 升高”或“降低”。)
③写出该装置工作时的电池反应式:___________ 。

(1)步骤I中,NH3和O2在催化剂作用下反应,其化学方程式是
(2)步骤II中,2NO(g)+O2(g)
 2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强( p1、p2)下随温度变化的曲线(如图)。
2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强( p1、p2)下随温度变化的曲线(如图)。
①比较p1、p2的大小关系:
②随温度升高,该反应平衡常数变化的趋势是
(3)步骤III中,先降低温度,将NO2(g)转化为N2O4(l),再制备浓硝酸。
①已知:2NO2(g)
 N2O4(g) △H1
N2O4(g) △H12NO2(g)
 N2O4(l) △H2
N2O4(l) △H2下列能量变化示意图中,正确的是
A.
 B.
B.  C.
C. 
②N2O4与O2、H2O化合的化学方程式是
(4)一种利用垃圾渗滤液中NH3、NH
 发电的原理如图所示。
发电的原理如图所示。
①X为该装置的
②该装置工作时, Y电极周围溶液的pH
③写出该装置工作时的电池反应式:
您最近半年使用:0次