名校
1 . 在一密闭容器中,放入镍粉并充入一定量的 CO 气体,一定条件下发生可逆反应 Ni(s)+4CO(g) Ni(CO)4(g),已知该反应在 25℃、80℃时的平衡常数分别为 5×104 和 2,下列说法正确的是
Ni(CO)4(g),已知该反应在 25℃、80℃时的平衡常数分别为 5×104 和 2,下列说法正确的是
 Ni(CO)4(g),已知该反应在 25℃、80℃时的平衡常数分别为 5×104 和 2,下列说法正确的是
Ni(CO)4(g),已知该反应在 25℃、80℃时的平衡常数分别为 5×104 和 2,下列说法正确的是| A.上述生成Ni(CO)4(g)的反应为吸热反应 |
| B.80℃时,测得某时刻 Ni(CO)4(g)、CO(g)浓度均为 0.5 mol·L-1,则此时 v(正)<v(逆) |
| C.恒温恒压下,向容器中再充入少量的Ar,上述平衡将正向移动 |
| D.恒温恒容下,向容器中再加入少量的 Ni(s),CO 的百分含量将增大 |
您最近一年使用:0次
名校
2 . 在一定温度下,向容积固定不变的密闭容器中充入a mol A,发生反应:2A(g)  B(g) ΔH<0。达平衡后再向容器中充入a mol A,再次达到平衡后,与原平衡比较,下列叙述不正确的是( )
B(g) ΔH<0。达平衡后再向容器中充入a mol A,再次达到平衡后,与原平衡比较,下列叙述不正确的是( )
 B(g) ΔH<0。达平衡后再向容器中充入a mol A,再次达到平衡后,与原平衡比较,下列叙述不正确的是( )
B(g) ΔH<0。达平衡后再向容器中充入a mol A,再次达到平衡后,与原平衡比较,下列叙述不正确的是( )| A.平均相对分子质量增大 |
| B.A的转化率提高 |
| C.A的质量分数增大 |
| D.反应放出的总热量大于原来的2倍 |
您最近一年使用:0次
2019-04-04更新
|
279次组卷
|
2卷引用:【全国百强校】福建省厦门外国语学校2018-2019学年高二下学期第一次月考化学试题
名校
3 . 一定条件下,下列反应中水蒸气含量随温度升高而下降,随压强增大而增大的是
A.CO2(g)+2NH3(g) CO(NH2)2(s)+H2O(g) ΔH<0 CO(NH2)2(s)+H2O(g) ΔH<0 |
B.CO2(g)+H2(g) CO(g)+H2O(g) ΔH>0 CO(g)+H2O(g) ΔH>0 |
C.CH3CH2OH(g) CH2=CH2(g)+H2O(g) ΔH>0 CH2=CH2(g)+H2O(g) ΔH>0 |
D.2C6H5CH2CH3(g)+O2(g) 2C6H5CH=CH2(g)+2H2O(g) ΔH<0 2C6H5CH=CH2(g)+2H2O(g) ΔH<0 |
您最近一年使用:0次
名校
4 . 现有反应aA(g)+bB(g) pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则
(1)该反应的逆反应是____ 反应(填“吸热或放热),且a+b___ p(填“>”“<”或“=”)。
(2)减压时,A的质量分数______ (填“增大”“减小”或“不变”,下同)。
(3)若加入B(体积不变),则A的转化率________ ,B的转化率________ 。
(4)若升高温度,则平衡时,B、C的浓度之比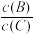 将
将________ 。
(5)若B是有色物质,A、C均为无色物质,则加入C(体积不变)时混合物的颜色________ (填“变浅”“变深”或“不变”,下同),而维持容器内气体的压强不变,充入氖气时,混合物的颜色________ 。
 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则(1)该反应的逆反应是
(2)减压时,A的质量分数
(3)若加入B(体积不变),则A的转化率
(4)若升高温度,则平衡时,B、C的浓度之比
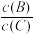 将
将(5)若B是有色物质,A、C均为无色物质,则加入C(体积不变)时混合物的颜色
您最近一年使用:0次
2018-10-22更新
|
296次组卷
|
2卷引用:河南省安阳市第三十六中学2018-2019学年高二上学期第一次月考化学试题
5 . 在一密闭容器中发生反应

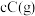 。反应过程中,物质A和C的物质的量随某物理量(x)的变化曲线如图所示。下列说法正确的是
。反应过程中,物质A和C的物质的量随某物理量(x)的变化曲线如图所示。下列说法正确的是
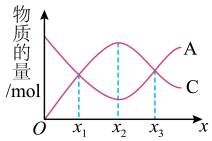


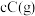 。反应过程中,物质A和C的物质的量随某物理量(x)的变化曲线如图所示。下列说法正确的是
。反应过程中,物质A和C的物质的量随某物理量(x)的变化曲线如图所示。下列说法正确的是
A.若x为温度,则xn对应的平衡常数: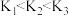 |
B.若x为恒压条件下加入物质B的物质的量,则化学反应速率: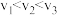 |
C.若x为压强,则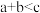 |
D.对于任何物理量x,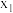 和 和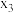 处各物质的百分含量和转化率均相同 处各物质的百分含量和转化率均相同 |
您最近一年使用:0次
2020-11-26更新
|
177次组卷
|
3卷引用:江苏省启东市2021届高三上学期期中考试化学试题
江苏省启东市2021届高三上学期期中考试化学试题(已下线)小题必刷28 化学平衡及平衡移动——2021年高考化学一轮复习小题必刷(通用版本)黑龙江省虎林市高级中学2023-2024学年高二上学期第一次月考化学试题
名校
解题方法
6 . 某温度下,将2mol E和3mol F充入一密闭容器中,发生反应:aE(g)+F(g)⇌M(g)+N(g),平衡常数K等于1,在温度不变的情况下将容器的体积扩大为原来的2倍,F百分含量不发生变化,则E的转化率为
| A.60% | B.50% | C.30% | D.无法确定 |
您最近一年使用:0次
2020-11-21更新
|
108次组卷
|
5卷引用:安徽省池州市第一中学2020-2021学年高二上学期期中考试化学试题
名校
解题方法
7 . 氮是地球上含量较丰富的一种元素,氮的化合物在工业生产和生活中有重要的作用。
I.已知298K时,发生反应:N2O4(g) 2NO2(g)△H>0
2NO2(g)△H>0
(1)在密闭容器内,一定条件下该反应达到平衡,当分别改变下列条件时,填写下列空白:
①达到平衡时,升高温度,平衡将________ 移动。(填“正向”、“逆向”或“不”)
②达到平衡时,充入Ar气,并保持体积不变,平衡将_________ 移动。(填“正向”、“逆向"或“不”)
③保持容器容积不变,再通入一定量N2O4,,达到平衡时NO2的百分含量________ (填“增大”“减小”或“不变”,下同)。
④保持压强不变,通入氖气使体系的容积增大一倍,则达到平衡时N2O4的转化率_____ 。
(2)恒容密闭容器中发生上述反应,已知v正=k正·p(N2O4),v逆=k逆·p2(NO2),Kp=__________ (用k正、k逆表示)。若初始压强为100kPa,k正=2.7×104s-1,当NO2的物质的量分数为50%时,v正=_________ kPa·s-1。[其中Kp为平衡常数,用平衡分压代替平衡浓度计算,p(N2O4)和p(NO2)分别是N2O4和NO2的分压,分压=p总×物质的量分数,k正、k逆为速率常数]
II.在催化剂作用下,H2可以还原NO消除污染,反应为:2NO(g)+2H2(g) N2(g)+2H2O(g)△H=-664kJ/mol
N2(g)+2H2O(g)△H=-664kJ/mol
(3)将2molNO和1molH2充入一个恒容的密闭容器中,经相同时间测得N2的体积分数与温度的关系如图所示。

低于900K时,N2的体积分数_______ (填“是”或“不是")对应温度下平衡时的体积分数,原因是_______________________________ 。高于900K时,Nz的体积分数降低的可能原因是__________________________________________________________ (答出两点)。
I.已知298K时,发生反应:N2O4(g)
 2NO2(g)△H>0
2NO2(g)△H>0(1)在密闭容器内,一定条件下该反应达到平衡,当分别改变下列条件时,填写下列空白:
①达到平衡时,升高温度,平衡将
②达到平衡时,充入Ar气,并保持体积不变,平衡将
③保持容器容积不变,再通入一定量N2O4,,达到平衡时NO2的百分含量
④保持压强不变,通入氖气使体系的容积增大一倍,则达到平衡时N2O4的转化率
(2)恒容密闭容器中发生上述反应,已知v正=k正·p(N2O4),v逆=k逆·p2(NO2),Kp=
II.在催化剂作用下,H2可以还原NO消除污染,反应为:2NO(g)+2H2(g)
 N2(g)+2H2O(g)△H=-664kJ/mol
N2(g)+2H2O(g)△H=-664kJ/mol(3)将2molNO和1molH2充入一个恒容的密闭容器中,经相同时间测得N2的体积分数与温度的关系如图所示。

低于900K时,N2的体积分数
您最近一年使用:0次
8 . 现有反应:mA(g)+nB(g)  pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)该反应的逆反应为________ 热反应,且m+n______ p (填“>”、“=”或“<”) 。
(2)减压时,A的质量分数__________ 。(填“增大”、“减小”或“不变”,下同)
(3)若容积不变加入B,则B的转化率__________ 。
(4)若升高温度,则平衡时B、C的浓度之比将__________ 。
(5)若加入催化剂,平衡时气体混合物的总物质的量__________ 。
(6)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色__________ ;而维持容器内压强不变,充入氖气时,混合物颜色 _______ 。(填“变深”、“变浅”或“不变”)。
 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:(1)该反应的逆反应为
(2)减压时,A的质量分数
(3)若容积不变加入B,则B的转化率
(4)若升高温度,则平衡时B、C的浓度之比将
(5)若加入催化剂,平衡时气体混合物的总物质的量
(6)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色
您最近一年使用:0次
2019-01-30更新
|
151次组卷
|
3卷引用:2015-2016学年吉林省松原市油田高中高一下期中化学试卷
11-12高二上·山东济宁·期中
名校
9 . 在一密闭容器中,反应mA(g)  nB(g)+nC(g)达平衡后,保持温度不变,将容器容积压缩到原来的一半,当达到新的平衡时,B和C的浓度均是原来的1.8倍,则
nB(g)+nC(g)达平衡后,保持温度不变,将容器容积压缩到原来的一半,当达到新的平衡时,B和C的浓度均是原来的1.8倍,则
 nB(g)+nC(g)达平衡后,保持温度不变,将容器容积压缩到原来的一半,当达到新的平衡时,B和C的浓度均是原来的1.8倍,则
nB(g)+nC(g)达平衡后,保持温度不变,将容器容积压缩到原来的一半,当达到新的平衡时,B和C的浓度均是原来的1.8倍,则| A.平衡向逆反应方向移动了 | B.物质A的转化率增大 |
| C.物质C的质量分数增大 | D.m > 2n |
您最近一年使用:0次
2018-09-29更新
|
298次组卷
|
4卷引用:2011-2012学年山东省兖州市高二上学期期中考试化学试卷
(已下线)2011-2012学年山东省兖州市高二上学期期中考试化学试卷山西省朔州市平鲁区李林中学2018-2019学年高二上学期第一次月考化学试题四川省南充市阆中中学2020届高三化学选择题专项训练(18)吉林油田高级中学2019-2020学年高一下学期期末考试化学试题
名校
解题方法
10 . (1)在密闭容器中,一定量混合气体发生下列反应:aM(g)+bN(g)⇌cW(g),达一平衡后,测得M气体的浓度为0.5mol/L。当在恒温下,将密闭容器的体积扩大1倍,再达平衡时,测得M气体的浓度为0.3mol/L。则N的转化率_______ (填变大,变小或不变)
(2)将一定量纯净的氨基甲酸铵置于密闭真空恒容容器中(固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)⇌2NH3(g)+CO2(g)。判断该分解反应已经达到化学平衡的是_______
A.2v(NH3)=v(CO2)
B.密闭容器中c(NH3)∶c(CO2)=2∶1
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
(3)向相同容积的甲、乙两容器中都分别充入1 mol SO2和0.5 mol O2,若甲容器保持温度、容积不变,乙容器保持温度、压强不变,分别达到平衡,下列说法正确的是_______
A.平衡时,容器内的压强:甲>乙
B.反应达到平衡时所需时间:甲<乙
C.平衡时,氧气的浓度:甲<乙
D.平衡时,容器内SO3的体积百分数:甲>乙
(4)下列说法正确的是_______
(2)将一定量纯净的氨基甲酸铵置于密闭真空恒容容器中(固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)⇌2NH3(g)+CO2(g)。判断该分解反应已经达到化学平衡的是
A.2v(NH3)=v(CO2)
B.密闭容器中c(NH3)∶c(CO2)=2∶1
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
(3)向相同容积的甲、乙两容器中都分别充入1 mol SO2和0.5 mol O2,若甲容器保持温度、容积不变,乙容器保持温度、压强不变,分别达到平衡,下列说法正确的是
A.平衡时,容器内的压强:甲>乙
B.反应达到平衡时所需时间:甲<乙
C.平衡时,氧气的浓度:甲<乙
D.平衡时,容器内SO3的体积百分数:甲>乙
(4)下列说法正确的是
| A | B | C | D |
 |  |  |  |
| 绝热恒容密闭容器中通入A和B,发生反应:2A (g)+B (g)⇌2C(g),如图为其正反应速率随时间变化的示意图,则该反应为放热反应 | 催化剂能降低反应的活化能,提高活化分子的百分含量,从而加快化学反应速率。如图显示的是催化反应与无催化反应过程中的能量关系 | 将BaO2放入密闭真空容器中,反应2BaO2(s)⇌2BaO(s)+O2(g)达到平衡时体系压强为P,保持温度不变,t0时刻将容器体积缩小为原来的1/2,体系重新达到平衡,体系压强变化如图所示 | 将一定量的NO2充入针筒中后封口,发生反应2NO2 (g)⇌N2O4(g),如图表示在拉伸和压缩针筒活塞的过程中气体透光率随时间的变化(气体颜色越深,透光率越小).则c点与a点相比,c(NO2)增大,c(N2O4)减小 |
您最近一年使用:0次



