1 . 关于水的说法,下列错误的是
| A.水的电离方程式2H2O ⇌H3O++OH- | B.纯水的pH可能为6 |
| C.25℃时水中通入少量HCl,KW减小 | D.水的电离∆H>0 |
您最近一年使用:0次
2023-01-04更新
|
458次组卷
|
4卷引用:上海市第三女子中学2023-2024学年高二上学期等级班12月测试化学试题
2 . 碘及其化合物在生产生活中应用广泛。回答下列问题:
(1)单质碘与氟反应可得IF5,实验表明液态IF5具有一定的导电性,原因在于IF5的自偶电离(如:2H2O H3O++OH﹣),IF5的自偶电离方程式为
H3O++OH﹣),IF5的自偶电离方程式为 _______ 。
(2)亚硫酸钠和碘酸钾在酸性溶液中的反应是:Na2SO3+KIO3+H2SO4→Na2SO4+K2SO4+I2+H2O(未配平),该反应过程和机理较复杂,一般认为分为以下几步:
①IO +SO
+SO →IO
→IO +SO
+SO (慢)
(慢)
②IO +SO
+SO →IO﹣+SO
→IO﹣+SO (快)
(快)
③5I﹣+6H++IO3﹣→3I2+3H2O(快)
④I2+SO +H2O→2I﹣+SO
+H2O→2I﹣+SO +2H+(快)
+2H+(快)
根据上述条件推测,此反应的总反应速率由_______ 步反应决定(填序号)。若预先加入淀粉溶液,由题述看必在 _______ 离子消耗完时,才会有淀粉变蓝的现象产生。
(3)碘离子的吸附是重要的研究课题。
①已知SO2与I2的反应,速率极快且平衡常数大,溶液中存在如下平衡:I2(aq)+I﹣(aq) I
I (aq)。现将1molSO2缓缓通入含1mol I2的水溶液中至恰好完全反应,溶液中I
(aq)。现将1molSO2缓缓通入含1mol I2的水溶液中至恰好完全反应,溶液中I 的物质的量n(I
的物质的量n(I )随反应时间(t)的变化曲线如图1所示。开始阶段,n(I
)随反应时间(t)的变化曲线如图1所示。开始阶段,n(I )逐渐增大的原因是
)逐渐增大的原因是 _______ 。

②科研小组用新型材料Ag/TiO2对溶液中碘离子进行吸附研究。如图2是不同pH条件下,碘离子吸附效果的变化曲线。据此推断Ag/TiO2材料最适合吸附_______ (填“酸性”“中性”或“碱性”)溶液中的I﹣。

③氯化银复合吸附剂也可有效吸附碘离子。氯化银复合吸附剂对碘离子的吸附反应为:I﹣(aq)+AgCl(s) AgI(s)+Cl﹣(aq),反应达到平衡后溶液中c(Cl﹣)=1.0 mol•L﹣1,则溶液中c(I﹣)=
AgI(s)+Cl﹣(aq),反应达到平衡后溶液中c(Cl﹣)=1.0 mol•L﹣1,则溶液中c(I﹣)=_______ mol•L﹣1[Ksp(AgCl)=2.0×10﹣10,Ksp(AgI)=8.4×10﹣17]。
(4)Fe3+与I﹣在溶液中发生反应:2 Fe3++2 I﹣ 2Fe2++I2,该反应的正反应速率和Fe3+与I﹣的浓度关系为v=k•cm(I﹣)•cn(Fe3+)(其中k为常数)。
2Fe2++I2,该反应的正反应速率和Fe3+与I﹣的浓度关系为v=k•cm(I﹣)•cn(Fe3+)(其中k为常数)。
①在v=k•cm(I﹣)•cn(Fe3+)中m、n的值为_______ (填序号)。
A.m=1、n=1
B.m=1、n=2
C.m=2、n=1
D.m=2、n=2
②I﹣浓度对反应速率的影响_______ (填“大于”、“小于”或“等于”)Fe3+浓度对反应速率的影响。
(1)单质碘与氟反应可得IF5,实验表明液态IF5具有一定的导电性,原因在于IF5的自偶电离(如:2H2O
 H3O++OH﹣),IF5的自偶电离方程式为
H3O++OH﹣),IF5的自偶电离方程式为 (2)亚硫酸钠和碘酸钾在酸性溶液中的反应是:Na2SO3+KIO3+H2SO4→Na2SO4+K2SO4+I2+H2O(未配平),该反应过程和机理较复杂,一般认为分为以下几步:
①IO
 +SO
+SO →IO
→IO +SO
+SO (慢)
(慢)②IO
 +SO
+SO →IO﹣+SO
→IO﹣+SO (快)
(快)③5I﹣+6H++IO3﹣→3I2+3H2O(快)
④I2+SO
 +H2O→2I﹣+SO
+H2O→2I﹣+SO +2H+(快)
+2H+(快)根据上述条件推测,此反应的总反应速率由
(3)碘离子的吸附是重要的研究课题。
①已知SO2与I2的反应,速率极快且平衡常数大,溶液中存在如下平衡:I2(aq)+I﹣(aq)
 I
I (aq)。现将1molSO2缓缓通入含1mol I2的水溶液中至恰好完全反应,溶液中I
(aq)。现将1molSO2缓缓通入含1mol I2的水溶液中至恰好完全反应,溶液中I 的物质的量n(I
的物质的量n(I )随反应时间(t)的变化曲线如图1所示。开始阶段,n(I
)随反应时间(t)的变化曲线如图1所示。开始阶段,n(I )逐渐增大的原因是
)逐渐增大的原因是 
②科研小组用新型材料Ag/TiO2对溶液中碘离子进行吸附研究。如图2是不同pH条件下,碘离子吸附效果的变化曲线。据此推断Ag/TiO2材料最适合吸附

③氯化银复合吸附剂也可有效吸附碘离子。氯化银复合吸附剂对碘离子的吸附反应为:I﹣(aq)+AgCl(s)
 AgI(s)+Cl﹣(aq),反应达到平衡后溶液中c(Cl﹣)=1.0 mol•L﹣1,则溶液中c(I﹣)=
AgI(s)+Cl﹣(aq),反应达到平衡后溶液中c(Cl﹣)=1.0 mol•L﹣1,则溶液中c(I﹣)=(4)Fe3+与I﹣在溶液中发生反应:2 Fe3++2 I﹣
 2Fe2++I2,该反应的正反应速率和Fe3+与I﹣的浓度关系为v=k•cm(I﹣)•cn(Fe3+)(其中k为常数)。
2Fe2++I2,该反应的正反应速率和Fe3+与I﹣的浓度关系为v=k•cm(I﹣)•cn(Fe3+)(其中k为常数)。| c(I﹣)/mol•L﹣1 | c(Fe3+)/mol•L﹣1 | v/mol•L﹣1•s﹣1 | |
| a | 0.20 | 0.80 | 0.032k |
| b | 0.60 | 0.40 | 0.144k |
| c | 0.80 | 0.20 | 0.128k |
①在v=k•cm(I﹣)•cn(Fe3+)中m、n的值为
A.m=1、n=1
B.m=1、n=2
C.m=2、n=1
D.m=2、n=2
②I﹣浓度对反应速率的影响
您最近一年使用:0次
20-21高二上·重庆长寿·期末
解题方法
3 . 下列说法正确的是
| A.1 mol·L-1的稀硫酸中存在OH- |
| B.Kw=10-14适用于任何温度、任何溶液 |
| C.Kw随溶液中c(H+)和c(OH-)的变化而改变 |
| D.水的电离只受温度影响,酸碱性对其无影响 |
您最近一年使用:0次
2021-04-19更新
|
450次组卷
|
5卷引用:3.1.1 水的电离和溶液的酸碱性-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)
(已下线)3.1.1 水的电离和溶液的酸碱性-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)重庆市长寿区2020-2021学年高二上学期学业质量联合检测化学试题(已下线)3.2.1 水的电离-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)3.2.1 水的电离 溶液的酸碱性(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)专题11 水溶液中的离子反应与平衡-2023年高考化学一轮复习小题多维练(全国通用)
名校
解题方法
4 . 科学家经过研究后发现,把水加热加压到 374℃、22.lMPa以上时具有很多特性, 如其中含有的氢离子浓度远远大于10-7mol/L,还具有很强的溶解有机物的能力。由此可知,处于这种状态下的水
| A.显中性, pH一定等于 7 | B.表现出非极性溶剂的特性 |
| C.显酸性,pH 一定小于 7 | D.表现出极性溶剂的特性 |
您最近一年使用:0次
5 . 水是极弱的电解质,改变外界条件对水的电离有促进或抑制作用,下列说法错误的是
| A.在蒸馏水中加入强酸或强碱对水的电离均有抑制作用;增加水的量,促进水的电离 |
| B.在蒸馏水中加入盐对水的电离可能有抑制作用,也可能有促进作用 |
| C.压强对水的电离影响较小,升高温度对水的电离有促进作用 |
| D.pH=4的某电解质溶液,其溶质可能是酸或者盐 |
您最近一年使用:0次
6 . 水是我们日常生活中最宝贵的资源之一。关于水的叙述正确的是( )
| A.4℃的纯水pH为7 |
B.水的电离方程式为:H2O 2H++O2- 2H++O2- |
| C.重水(D2O)中,质量数是质子数的两倍 |
| D.相同质量的水具有的能量:固体>液体>气体 |
您最近一年使用:0次
7 . 25℃时,0.005mol/LBa(OH)2中H+浓度是( )
A.1× mol/L mol/L | B.1×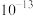 mol/L mol/L |
C.5× mol/L mol/L | D.5×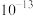 mol/L mol/L |
您最近一年使用:0次
2019-10-28更新
|
793次组卷
|
9卷引用:2019年上海市普通高中学业水平等级性考试(高考)化学试卷
2019年上海市普通高中学业水平等级性考试(高考)化学试卷上海市徐汇区徐汇中学2022-2023学年高三上学期11月期中考试化学试题2020届高考化学小题狂练(全国通用版)专练15 弱电解质的电离平衡和溶液酸碱性(已下线)专题十二 水溶液中的离子平衡(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训重庆市云阳江口中学校2020-2021学年高二上学期第一次月考化学试题江西省抚州市金溪县第一中学2020-2021学年高二上学期第二次月考化学试题(已下线)3.2.1 水的电离和溶液的酸碱性-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)考向25 水的电离和溶液的酸碱性-备战2022年高考化学一轮复习考点微专题江西省抚州市金溪县第一中学2021-2022学年高二下学期第二次月考化学试题
8 . 水是自然界最重要的分散剂,关于水的叙述错误的是( )
| A.水分子是含极性键的极性分子 |
| B.水的电离方程式为:H2O⇌2H++O2﹣ |
| C.重水(D2O)分子中,各原子质量数之和是质子数之和的两倍 |
| D.相同质量的水具有的内能:固体<液体<气体 |
您最近一年使用:0次
名校
9 . 90℃时水的离子积常数Kw=3.8×10-13,该温度时纯水的pH最接近
| A.6.2 | B.7 | C.12.7 | D.无法确定 |
您最近一年使用:0次
10 . 加入水能抑制水的电离的物质是
| A.碘化钾 | B.氯化钠 | C.硫酸 | D.硫酸钠 |
您最近一年使用:0次



