名校
1 . 已知:下表为25℃时某些弱酸的电离平衡常数。
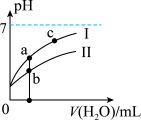
如图表示常温下,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化.下列说法正确的是( )
| CH3COOH | HClO | H2CO3 |
| Ka=1.8×10﹣5 | Ka=3.0×10﹣8 | Ka1=4.4×10﹣7Ka2=4.7×10﹣11 |

| A.Ⅰ曲线代表 HClO,Ⅱ曲线代表CH3COOH |
| B.向NaClO溶液中通入少量二氧化碳的离子方程式为:ClO﹣+CO2+H2O=HClO+CO32- |
C.图象中a、c两点处的溶液中 相等(HR代表CH3COOH或HClO) 相等(HR代表CH3COOH或HClO) |
| D.图象中a点酸的总浓度大于b点酸的总浓度 |
您最近一年使用:0次
2019-11-03更新
|
229次组卷
|
3卷引用:西藏拉萨中学2019-2020学年高二上学期第二次月考理综化学试题
名校
2 . 下列图示与对应的叙述相符的是( )
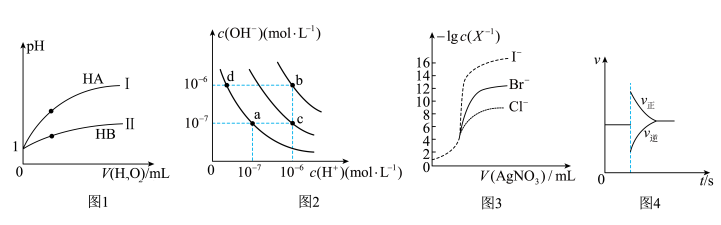

| A.图1表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则等物质的量浓度的NaA和NaB混合溶液中:c(Na+)>c(A-)>c(B-)>c(OH-)>c(H+) |
| B.图2中在b点对应温度下,将pH=2的H2SO4溶液与pH=12的NaOH溶液等体积混合后,溶液显中性 |
| C.用0.0100 mol/L硝酸银标准溶液,滴定浓度均为0.1000 mol/L Cl-、Br-及I-的混合溶液,由图3曲线,可确定首先沉淀的是Cl- |
D.图4表示在N2(g)+3H2(g)  2NH3(g)达到平衡后,减小NH3浓度时速率的变化 2NH3(g)达到平衡后,减小NH3浓度时速率的变化 |
您最近一年使用:0次
2019-03-09更新
|
774次组卷
|
8卷引用:西藏拉萨中学2019-2020学年高二上学期第三次月考理综化学试题
西藏拉萨中学2019-2020学年高二上学期第三次月考理综化学试题【全国百强校】广西南宁市第三中学2018-2019学年高二下学期第一次月考化学试题【全国百强校】福建省厦门市外国语学校2018-2019学年高二下学期期中考试化学试题江西省吉安市重点高中2018-2019学年高二下学期5月联考化学试题江西吉安市重点高中2019-2020学年高二上第一次联考化学试题(已下线)第三章 检测-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)河北省石家庄市第二十四中学2023-2024高二上学期期末考试化学试题【校级联考】江西省上饶市重点中学2019届高三下学期第一次六校联考理科综合化学试题



