名校
解题方法
1 . 下列电离方程式正确的是
A. 溶于水: 溶于水: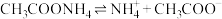 |
B. 溶于水: 溶于水: |
C.HCl溶于水: |
D. 溶于水: 溶于水: |
您最近一年使用:0次
名校
解题方法
2 . 下列水溶液中 的电离方程式书写正确的是
A.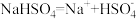 | B.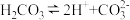 |
C. | D.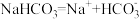 |
您最近一年使用:0次
名校
解题方法
3 . 下列离子方程式或电离方程式书写正确的是
| A.铁与稀盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
| B.硝酸银溶液中加入铁粉:Ag++Fe=Fe2++Ag |
C.硫酸钠熔化状态下的电离方程式:Na2SO4=2Na++ |
| D.氟化氢的电离方程式:HF=H++F- |
您最近一年使用:0次
4 . 导电性实验可以作为研究电解质电离本质及反应机理的有效方法。
(1)在如下图所示的装置里,若灯泡亮,广口瓶内的物质A 可以是_______ (填序号)。

①干燥的氯化钠晶体 ②干燥的氢氧化钠晶体 ③蔗糖晶体 ④酒精 ⑤氯化钠溶液 ⑥ 氢氧化钠溶液 ⑦稀盐酸 ⑧硫酸铜溶液
(2)写出一水合氨的电离方程式_______ 。
(3)在电解质溶液的导电性装置(如下图所示)中,若向某一电解质溶液中逐滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是_______ (填字母),并写出发生反应的离子方程式_______ 。
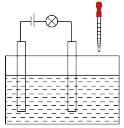
A.盐酸中逐滴加入食盐溶液 B.硫酸中逐滴加入氢氧化钠溶液
C.石灰乳中滴加稀盐酸 D.硫酸中逐滴加入氢氧化钡溶液
(4)已知:CO2+Ca(OH)2=CaCO3↓+H2O,CaCO3+CO2+H2O=Ca(HCO3)2,且 Ca(HCO3)2易溶于水。若在(3)题图中,电解质溶液为 Ca(OH)2溶液,向溶液中逐渐通入 CO2。则:下列四个图中,_______(填字母)能比较准确地反映出溶液的导电能力和通入CO2 气体量的关系(x 轴表示 CO2通入的量,y 轴表示导电能力)。
(1)在如下图所示的装置里,若灯泡亮,广口瓶内的物质A 可以是

①干燥的氯化钠晶体 ②干燥的氢氧化钠晶体 ③蔗糖晶体 ④酒精 ⑤氯化钠溶液 ⑥ 氢氧化钠溶液 ⑦稀盐酸 ⑧硫酸铜溶液
(2)写出一水合氨的电离方程式
(3)在电解质溶液的导电性装置(如下图所示)中,若向某一电解质溶液中逐滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是

A.盐酸中逐滴加入食盐溶液 B.硫酸中逐滴加入氢氧化钠溶液
C.石灰乳中滴加稀盐酸 D.硫酸中逐滴加入氢氧化钡溶液
(4)已知:CO2+Ca(OH)2=CaCO3↓+H2O,CaCO3+CO2+H2O=Ca(HCO3)2,且 Ca(HCO3)2易溶于水。若在(3)题图中,电解质溶液为 Ca(OH)2溶液,向溶液中逐渐通入 CO2。则:下列四个图中,_______(填字母)能比较准确地反映出溶液的导电能力和通入CO2 气体量的关系(x 轴表示 CO2通入的量,y 轴表示导电能力)。
A. | B.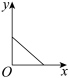 | C.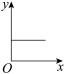 | D.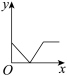 |
您最近一年使用:0次
5 . 下列离子方程式或电离方程式书写正确的是
| A.铁与稀盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
| B.硝酸银溶液中加入铁粉:Ag++Fe=Fe2++Ag |
C.碳酸氢钠电离方程式:NaHCO3=Na++HCO |
| D.氟化氢的电离方程式:HF=H++F- |
您最近一年使用:0次
解题方法
6 . 中国政府承诺:力争 的排放在2030年前实现“碳达峰”,2060年前实现“碳中和”。
的排放在2030年前实现“碳达峰”,2060年前实现“碳中和”。 的捕集与利用成为当前研究的热点。
的捕集与利用成为当前研究的热点。
Ⅰ.“氨法”捕集二氧化碳是实现“碳中和”的重要途径之一
反应的化学方程式为: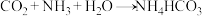 。
。
完成下列填空:
(1)写出氮原子的核外电子排布式_______ ,写出 分子的电子式
分子的电子式_______ 。
(2)用方程式表示二氧化碳溶于水溶液呈现酸性的原因_______ 。
(3)组成 的四种元素中,由其中任意两种元素组成且含非极性键的分子可以是
的四种元素中,由其中任意两种元素组成且含非极性键的分子可以是_______ (写出一种,下同);由其中任意三种元素组成的离子化合物可以是_______ 。
(4)上述氨法吸收废气中 时,一般温度控制在30℃,用化学方程式表示温度不宜太高的原因。
时,一般温度控制在30℃,用化学方程式表示温度不宜太高的原因。_______
Ⅱ.我国化学家研究在铜基催化剂作用下将 高效转化为甲酸,合成铜基催化剂时有一步反应为:
高效转化为甲酸,合成铜基催化剂时有一步反应为: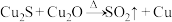 (未配平)。
(未配平)。
(5)配平上述化学方程式_______ 。若反应中转移 电子,则生成气体在标准状态下的体积为
电子,则生成气体在标准状态下的体积为_______ L。
 的排放在2030年前实现“碳达峰”,2060年前实现“碳中和”。
的排放在2030年前实现“碳达峰”,2060年前实现“碳中和”。 的捕集与利用成为当前研究的热点。
的捕集与利用成为当前研究的热点。Ⅰ.“氨法”捕集二氧化碳是实现“碳中和”的重要途径之一
反应的化学方程式为:
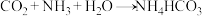 。
。完成下列填空:
(1)写出氮原子的核外电子排布式
 分子的电子式
分子的电子式(2)用方程式表示二氧化碳溶于水溶液呈现酸性的原因
(3)组成
 的四种元素中,由其中任意两种元素组成且含非极性键的分子可以是
的四种元素中,由其中任意两种元素组成且含非极性键的分子可以是(4)上述氨法吸收废气中
 时,一般温度控制在30℃,用化学方程式表示温度不宜太高的原因。
时,一般温度控制在30℃,用化学方程式表示温度不宜太高的原因。Ⅱ.我国化学家研究在铜基催化剂作用下将
 高效转化为甲酸,合成铜基催化剂时有一步反应为:
高效转化为甲酸,合成铜基催化剂时有一步反应为: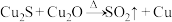 (未配平)。
(未配平)。(5)配平上述化学方程式
 电子,则生成气体在标准状态下的体积为
电子,则生成气体在标准状态下的体积为
您最近一年使用:0次
名校
7 . 磷有多种化合物,次磷酸(H3PO2)和次磷酸钠(NaH2PO2)常为化工生产中的还原剂。完成下列填空:
(1)P元素在周期表中的位置是_______ ,NaH2PO2中涉及到四种元素,它们的原子半径由大到小的顺序为_______ 。写出与磷同周期的主族元素中,离子半径最小的元素的最高价氧化物对应水化物的化学式_______ 。
(2)白磷(P4)在过量的热NaOH溶液中,会生成PH3气体和NaH2PO2,写出该反应的化学方程式_______ ,已知白磷中只存在P-P键,画出白磷的球棍模型_______ 。
(3)已知H3PO2是一种弱酸,写出其电离方程式_______ ,如何实验证明其是一种弱酸_______ 。
(4)NaH2PO2可在酸性条件下与Ni2+作用进行“化学镀镍”(如在木材表面生成一层Ni-P合金),反应中磷元素化合价发生的变化是_______ (选填编号)。
a.升高 b.降低 c.既升高又降低
(5)Ba(H2PO2)2溶液中加入盐酸制备H3PO2,写出该反应的离子方程式_______ 有人说应该用硫酸代替盐酸,请说明用硫酸代替盐酸的优点_____ 。
(1)P元素在周期表中的位置是
(2)白磷(P4)在过量的热NaOH溶液中,会生成PH3气体和NaH2PO2,写出该反应的化学方程式
(3)已知H3PO2是一种弱酸,写出其电离方程式
(4)NaH2PO2可在酸性条件下与Ni2+作用进行“化学镀镍”(如在木材表面生成一层Ni-P合金),反应中磷元素化合价发生的变化是
a.升高 b.降低 c.既升高又降低
(5)Ba(H2PO2)2溶液中加入盐酸制备H3PO2,写出该反应的离子方程式
您最近一年使用:0次
名校
解题方法
8 . 下列离子方程式或电离方程式书写正确的是
| A.铁与稀盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
| B.硝酸银溶液中加入铁粉:Ag++Fe=Fe2++Ag |
C.硫酸氢钠熔化状态下的电离方程式:NaHSO4=Na++HSO |
| D.氟化氢的电离方程式:HF=H++F— |
您最近一年使用:0次
名校
解题方法
9 . 下列电离方程式中,正确的是
A.CH3COONH4=CH3COO-+NH | B.H2S 2H++S2- 2H++S2- |
C.NaHCO3=Na++H++CO | D.Ba(OH)2 Ba2++2OH- Ba2++2OH- |
您最近一年使用:0次
名校
10 . 下列电离方程式中,正确的是( )
| A.CH3COOH=CH3COO-+H+ | B.NaHCO3=Na++HCO3- |
C.KClO3 K++ClO3- K++ClO3- | D.BaSO4=Ba2++S2-+4O2- |
您最近一年使用:0次



