1 . 下列关于常温下的 溶液说法不正确的是
溶液说法不正确的是
资料: 时,
时,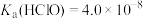 ,
, ,
,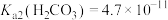
 溶液说法不正确的是
溶液说法不正确的是资料:
 时,
时,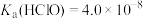 ,
, ,
,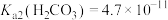
A. 溶液显碱性 溶液显碱性 |
B. 的 的 和 和 的混合溶液中, 的混合溶液中,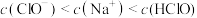 |
C.在酸性条件下可能与 溶液反应产生氯气 溶液反应产生氯气 |
D.与少量 反应的离子方程式为 反应的离子方程式为 |
您最近一年使用:0次
2024-06-03更新
|
251次组卷
|
5卷引用:北京市昌平区2023-2024学年高三下学期二模化学试题
北京市昌平区2023-2024学年高三下学期二模化学试题2024届北京市中关村中学高三下学期化学学科练习北京市顺义区第一中学2024届高三下学期三模化学试题 北京市中国人民大学附属中学2024届高三下学期化学热身练习(三模) (已下线)湖北省十堰市2024届高三下学期第三次模拟化学试题
名校
2 . “84消毒液”广泛应用于杀菌消毒,其有效成分是NaClO。实验小组制备消毒液,并利用其性质探索制备碘水的方法并测定相关反应的平衡常数。
资料:i.HClO的电离常数为Ka=4.7×10-8;H2CO3的电离常数为K1=4.3×10-7、K2=5.6×10-11
ii.碘的化合物主要以I-和 的形式存在,
的形式存在, +5I-+6H+=3I2+3H2O。
+5I-+6H+=3I2+3H2O。
iii.碘单质能与I-反应:I2+I-
 (
( 低浓度时显黄色,高浓度时为棕色)。
低浓度时显黄色,高浓度时为棕色)。
I制备消毒液(夹持装置略)
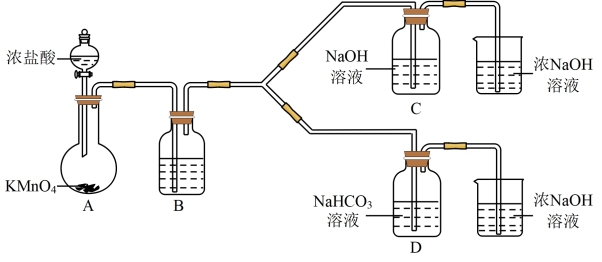
(1)制备NaClO的离子反应方程式___________ 。
(2)结合资料i,写出D中反应的化学方程式___________ 。
II.利用消毒液的性质探究碘水的制备方法
将某品牌“84消毒液”稀释10倍,各取100mL于三个烧杯中,设计如下实验方案制备碘水:
(3)针对烧杯3“滴加淀粉溶液不变蓝”的原因,提出两种假设:
假设1:过量的NaClO将反应生成的I2氧化为 。
。
设计实验a证实了假设1成立。NaClO氧化I2生成 的离子方程式是
的离子方程式是___________ 。
假设2:生成的I2在碱性溶液中不能存在。
设计实验b证实了假设2成立,实验b的操作及现象是___________ 。
(4)某小组检验烧杯3所得溶液中含 :取烧杯3所得无色溶液少许,加入稀硫酸酸化的KI溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在
:取烧杯3所得无色溶液少许,加入稀硫酸酸化的KI溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在 ,说明理由
,说明理由___________ 。
(5)预测烧杯1反应后加淀粉溶液的实验现象,结合方程式说明预测依据___________ 。
资料:i.HClO的电离常数为Ka=4.7×10-8;H2CO3的电离常数为K1=4.3×10-7、K2=5.6×10-11
ii.碘的化合物主要以I-和
 的形式存在,
的形式存在, +5I-+6H+=3I2+3H2O。
+5I-+6H+=3I2+3H2O。iii.碘单质能与I-反应:I2+I-

 (
( 低浓度时显黄色,高浓度时为棕色)。
低浓度时显黄色,高浓度时为棕色)。I制备消毒液(夹持装置略)

(1)制备NaClO的离子反应方程式
(2)结合资料i,写出D中反应的化学方程式
II.利用消毒液的性质探究碘水的制备方法
将某品牌“84消毒液”稀释10倍,各取100mL于三个烧杯中,设计如下实验方案制备碘水:
| 方案 | 操作 | 现象 | 反应后加淀粉溶液 |
| 1 | 烧杯1溶液中加入9gKI固体 | |溶液为橙黄色 | …… |
| 2 | 烧杯2溶液中加入9gKI固体,再加入1mol/L盐酸10mL | 溶液颜色快速加深,呈紫红色 | 变蓝 |
| 3 | 烧杯3溶液中加入少量KI固体(小于0.5g) | 振荡后溶液保持无色 | 不变蓝 |
假设1:过量的NaClO将反应生成的I2氧化为
 。
。设计实验a证实了假设1成立。NaClO氧化I2生成
 的离子方程式是
的离子方程式是假设2:生成的I2在碱性溶液中不能存在。
设计实验b证实了假设2成立,实验b的操作及现象是
(4)某小组检验烧杯3所得溶液中含
 :取烧杯3所得无色溶液少许,加入稀硫酸酸化的KI溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在
:取烧杯3所得无色溶液少许,加入稀硫酸酸化的KI溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在 ,说明理由
,说明理由(5)预测烧杯1反应后加淀粉溶液的实验现象,结合方程式说明预测依据
您最近一年使用:0次
2022-05-31更新
|
509次组卷
|
3卷引用:北京市第一六六中学2022届高三下学期三模化学试题
3 . 稍过量零价铁与亚硫酸钠体系能有效降解废水中有机污染物活性红。
已知:
ⅰ.体系中产生的 、
、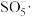 和
和 可将活性红氧化,其中
可将活性红氧化,其中 具有强氧化性
具有强氧化性
ⅱ.

ⅲ. 开始沉淀时pH=6.3,完全沉淀时pH=8.3
开始沉淀时pH=6.3,完全沉淀时pH=8.3
 开始沉淀时pH=1.5,完全沉淀时pH=2.8
开始沉淀时pH=1.5,完全沉淀时pH=2.8 体系中各含硫粒子的物质的量分数与pH的关系
体系中各含硫粒子的物质的量分数与pH的关系
下列说法不正确 的是
已知:
ⅰ.体系中产生的
 、
、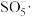 和
和 可将活性红氧化,其中
可将活性红氧化,其中 具有强氧化性
具有强氧化性ⅱ.


ⅲ.
 开始沉淀时pH=6.3,完全沉淀时pH=8.3
开始沉淀时pH=6.3,完全沉淀时pH=8.3 开始沉淀时pH=1.5,完全沉淀时pH=2.8
开始沉淀时pH=1.5,完全沉淀时pH=2.8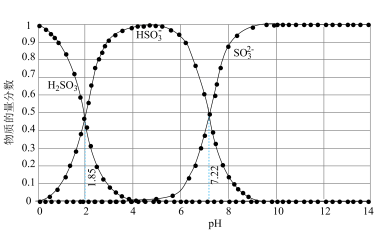
 体系中各含硫粒子的物质的量分数与pH的关系
体系中各含硫粒子的物质的量分数与pH的关系 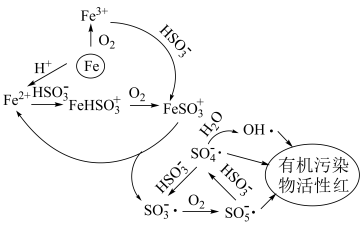
下列说法
A.由图1,25℃时 的 的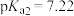 |
| B.pH=4时较pH=8时具有更好的降解效果 |
C.反应一段时间后零价铁表面产生 ,投入 ,投入 可消除 可消除 |
| D.用等物质的量的硫酸亚铁代替零价铁可提高有机物的降解率 |
您最近一年使用:0次
4 . “绿水青山就是金山银山”。研究含氮和含硫化合物的性质在工业生产和环境保护中有重要意义。
(1)制备硫酸可以有如下两种途径:
2SO2(g)+O2(g)=2SO3(g)ΔH=-198 kJ· mol-1
SO2(g)+NO2(g)=SO3(g)+NO(g) ΔH=-41.8 kJ· mol-1
若CO的标准燃烧热为 283 kJ· mol-1,则1 mol NO2和1 mol CO反应生成CO2和NO的能量变化示意图中E2=________ kJ· mol-1。

(2)已知某温度下,H2SO3的电离常数为K1≈1.5×10-2,K2≈1.0×10-7,用NaOH溶液吸收SO2。当溶液中HSO3-、SO32-离子浓度相等时,溶液的pH约为_______________ 。
(3)连二亚硫酸钠(Na2S2O4)具有强还原性,废水处理时可在弱酸性条件下加入亚硫酸氢钠电解产生连二亚硫酸根,进而将废水中的HNO2还原成无害气体排放,连二亚硫酸根氧化为原料循环电解。产生连二亚硫酸根的电极反应式为________________ ,连二亚硫酸根与HNO2(HNO2的电离常数为Ka=5.1×10-4)反应的离子方程式为________________________________ 。
(4)锅炉烟道气含CO、SO2,可通过如下反应回收硫:2CO(g)+SO2(g) S(l)+2CO2(g)。某温度下在2 L恒容密闭容器中通入2 mol SO2和一定量的CO发生反应,5 min后达到平衡,生成1 mol CO2。
S(l)+2CO2(g)。某温度下在2 L恒容密闭容器中通入2 mol SO2和一定量的CO发生反应,5 min后达到平衡,生成1 mol CO2。
①其他条件不变时,随着温度的升高,SO2的平衡转化率变化如图A,请解释其原因________________________________ 。(已知硫的沸点约是445°C)
②保持其他条件不变,第8分钟时,将容器体积迅速压缩至1 L,在10分钟时达到平衡,CO的物质的量变化了1 mol。请在图B中画出SO2浓度6~11分钟的变化曲线。______

(1)制备硫酸可以有如下两种途径:
2SO2(g)+O2(g)=2SO3(g)ΔH=-198 kJ· mol-1
SO2(g)+NO2(g)=SO3(g)+NO(g) ΔH=-41.8 kJ· mol-1
若CO的标准燃烧热为 283 kJ· mol-1,则1 mol NO2和1 mol CO反应生成CO2和NO的能量变化示意图中E2=

(2)已知某温度下,H2SO3的电离常数为K1≈1.5×10-2,K2≈1.0×10-7,用NaOH溶液吸收SO2。当溶液中HSO3-、SO32-离子浓度相等时,溶液的pH约为
(3)连二亚硫酸钠(Na2S2O4)具有强还原性,废水处理时可在弱酸性条件下加入亚硫酸氢钠电解产生连二亚硫酸根,进而将废水中的HNO2还原成无害气体排放,连二亚硫酸根氧化为原料循环电解。产生连二亚硫酸根的电极反应式为
(4)锅炉烟道气含CO、SO2,可通过如下反应回收硫:2CO(g)+SO2(g)
 S(l)+2CO2(g)。某温度下在2 L恒容密闭容器中通入2 mol SO2和一定量的CO发生反应,5 min后达到平衡,生成1 mol CO2。
S(l)+2CO2(g)。某温度下在2 L恒容密闭容器中通入2 mol SO2和一定量的CO发生反应,5 min后达到平衡,生成1 mol CO2。①其他条件不变时,随着温度的升高,SO2的平衡转化率变化如图A,请解释其原因
②保持其他条件不变,第8分钟时,将容器体积迅速压缩至1 L,在10分钟时达到平衡,CO的物质的量变化了1 mol。请在图B中画出SO2浓度6~11分钟的变化曲线。

您最近一年使用:0次



