1 . 稍过量零价铁与亚硫酸钠体系能有效降解废水中有机污染物活性红。
已知:
ⅰ.体系中产生的 、
、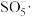 和
和 可将活性红氧化,其中
可将活性红氧化,其中 具有强氧化性
具有强氧化性
ⅱ.

ⅲ. 开始沉淀时pH=6.3,完全沉淀时pH=8.3
开始沉淀时pH=6.3,完全沉淀时pH=8.3
 开始沉淀时pH=1.5,完全沉淀时pH=2.8
开始沉淀时pH=1.5,完全沉淀时pH=2.8 体系中各含硫粒子的物质的量分数与pH的关系
体系中各含硫粒子的物质的量分数与pH的关系
下列说法不正确 的是
已知:
ⅰ.体系中产生的
 、
、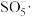 和
和 可将活性红氧化,其中
可将活性红氧化,其中 具有强氧化性
具有强氧化性ⅱ.


ⅲ.
 开始沉淀时pH=6.3,完全沉淀时pH=8.3
开始沉淀时pH=6.3,完全沉淀时pH=8.3 开始沉淀时pH=1.5,完全沉淀时pH=2.8
开始沉淀时pH=1.5,完全沉淀时pH=2.8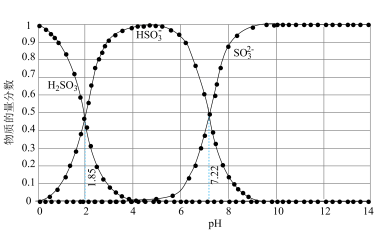
 体系中各含硫粒子的物质的量分数与pH的关系
体系中各含硫粒子的物质的量分数与pH的关系 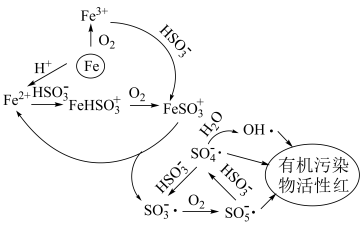
下列说法
A.由图1,25℃时 的 的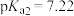 |
| B.pH=4时较pH=8时具有更好的降解效果 |
C.反应一段时间后零价铁表面产生 ,投入 ,投入 可消除 可消除 |
| D.用等物质的量的硫酸亚铁代替零价铁可提高有机物的降解率 |
您最近一年使用:0次
2 . 下列关于常温下的 溶液说法不正确的是
溶液说法不正确的是
资料: 时,
时,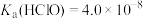 ,
, ,
,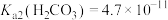
 溶液说法不正确的是
溶液说法不正确的是资料:
 时,
时,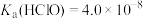 ,
, ,
,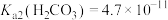
A. 溶液显碱性 溶液显碱性 |
B. 的 的 和 和 的混合溶液中, 的混合溶液中,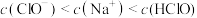 |
C.在酸性条件下可能与 溶液反应产生氯气 溶液反应产生氯气 |
D.与少量 反应的离子方程式为 反应的离子方程式为 |
您最近一年使用:0次
解题方法
3 . 常温下,用0.20mol·L-1盐酸滴定25.00mL0.20mol·L-1NH3·H2O溶液,所得溶液的pH、NH4+和NH3·H2O的物质的量分数(x)与滴加盐酸体积的关系如图所示。下列说法不正确 的是
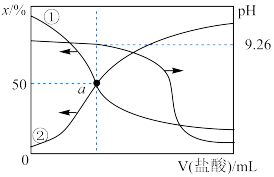
| A.曲线①代表x(NH3·H2O) |
| B.当溶液显中性时,滴入盐酸的体积小于25.00mL |
| C.NH3·H2O的电离常数约为1×10-9.26 |
D.a点的溶液中存在c(NH )=c(NH3·H2O)>c(Cl-) )=c(NH3·H2O)>c(Cl-) |
您最近一年使用:0次
4 . 25℃时,某小组同学分别用如下方法测定CH3COOH的电离常数(Ka)。
【方法一】实验步骤:
i.取amL稀CH3COOH溶液于锥形瓶中,再加入……
ii.用c1mol•L-1NaOH标准溶液滴定至终点,消耗NaOH溶液的体积为V1mL。
iii.另取一份该稀CH3COOH溶液于烧杯中,用pH计测得其pH为x。
(1)CH3COOH电离方程式为______ 。
(2)补全i中试剂及用量______ 。
(3)该稀CH3COOH溶液的浓度c=______ mol•L-1(用代数式表示)。
数据处理:醋酸的电离平衡常数Ka=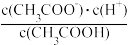 ≈
≈ 。代入相关数据,即可得Ka。
。代入相关数据,即可得Ka。
误差分析:
(4)若i中锥形瓶提前用该稀CH3COOH溶液进行了润洗,会使测得的Ka______ 。(填“偏大”、“偏小”、“无影响”)
【方法二】实验原理:
由CH3COOH的电离平衡常数表达式可知,当c(CH3COO-)=c(CH3COOH)时,Ka=c(H+)。
实验步骤:①取25mL某CH3COOH溶液,用NaOH溶液滴定至终点。
②继续向①中加入一定量的该CH3COOH溶液。
③用pH计测定②中混合溶液的pH为y。
(5)为保证c(CH3COO-)≈c(CH3COOH),步骤②中加入的CH3COOH溶液应为______ 。(填序号)
数据处理:
(6)Ka=______ (用代数式表示)。
迁移应用:
(7)已知亚磷酸(H3PO3)为二元弱酸,其溶液中含磷粒子的物质的量分数与pH的关系如图所示。

下列说法正确的是______ (填字母序号)。
A.H3PO3的Ka1=10-1.43
B.NaH2PO3溶液显碱性
C.向H3PO3溶液中逐滴加入NaOH溶液至pH=6.54,发生反应:3OH-+2H3PO3=H2PO +HPO
+HPO +3H2O
+3H2O
【方法一】实验步骤:
i.取amL稀CH3COOH溶液于锥形瓶中,再加入……
ii.用c1mol•L-1NaOH标准溶液滴定至终点,消耗NaOH溶液的体积为V1mL。
iii.另取一份该稀CH3COOH溶液于烧杯中,用pH计测得其pH为x。
(1)CH3COOH电离方程式为
(2)补全i中试剂及用量
(3)该稀CH3COOH溶液的浓度c=
数据处理:醋酸的电离平衡常数Ka=
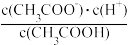 ≈
≈ 。代入相关数据,即可得Ka。
。代入相关数据,即可得Ka。误差分析:
(4)若i中锥形瓶提前用该稀CH3COOH溶液进行了润洗,会使测得的Ka
【方法二】实验原理:
由CH3COOH的电离平衡常数表达式可知,当c(CH3COO-)=c(CH3COOH)时,Ka=c(H+)。
实验步骤:①取25mL某CH3COOH溶液,用NaOH溶液滴定至终点。
②继续向①中加入一定量的该CH3COOH溶液。
③用pH计测定②中混合溶液的pH为y。
(5)为保证c(CH3COO-)≈c(CH3COOH),步骤②中加入的CH3COOH溶液应为
| A.25mL | B.50mL | C.75mL | D.用量与①中使用的NaOH溶液浓度有关 |
数据处理:
(6)Ka=
迁移应用:
(7)已知亚磷酸(H3PO3)为二元弱酸,其溶液中含磷粒子的物质的量分数与pH的关系如图所示。

下列说法正确的是
A.H3PO3的Ka1=10-1.43
B.NaH2PO3溶液显碱性
C.向H3PO3溶液中逐滴加入NaOH溶液至pH=6.54,发生反应:3OH-+2H3PO3=H2PO
 +HPO
+HPO +3H2O
+3H2O
您最近一年使用:0次
5 . 常温下,某弱酸HA溶液中主要成分的物质的量浓度分数随pH的变化如图所示。下列有关叙述不正确的是


A.常温下,HA的电离平衡常数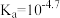 | B.若温度升高,曲线交点M会向左移动 |
C.NaA的水解平衡常数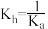 | D.某 的缓冲溶液,pH约为4 的缓冲溶液,pH约为4 |
您最近一年使用:0次
6 . 硫酸工业尾气中的 可用
可用 溶液吸收。25℃,
溶液吸收。25℃, 、
、 的电离平衡常数如下表。
的电离平衡常数如下表。
下列分析正确的是
 可用
可用 溶液吸收。25℃,
溶液吸收。25℃, 、
、 的电离平衡常数如下表。
的电离平衡常数如下表。 |  | |
 | 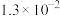 | 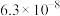 |
 | 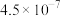 | 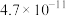 |
A. 是强电解质, 是强电解质, 是弱电解质 是弱电解质 |
B. 溶液和 溶液和 溶液的反应主要为: 溶液的反应主要为: |
C. 溶液呈碱性的原因: 溶液呈碱性的原因: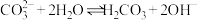 |
D. 溶液的pH大于 溶液的pH大于 溶液的pH 溶液的pH |
您最近一年使用:0次
名校
7 . “84消毒液”广泛应用于杀菌消毒,其有效成分是NaClO。实验小组制备消毒液,并利用其性质探索制备碘水的方法并测定相关反应的平衡常数。
资料:i.HClO的电离常数为Ka=4.7×10-8;H2CO3的电离常数为K1=4.3×10-7、K2=5.6×10-11
ii.碘的化合物主要以I-和 的形式存在,
的形式存在, +5I-+6H+=3I2+3H2O。
+5I-+6H+=3I2+3H2O。
iii.碘单质能与I-反应:I2+I-
 (
( 低浓度时显黄色,高浓度时为棕色)。
低浓度时显黄色,高浓度时为棕色)。
I制备消毒液(夹持装置略)
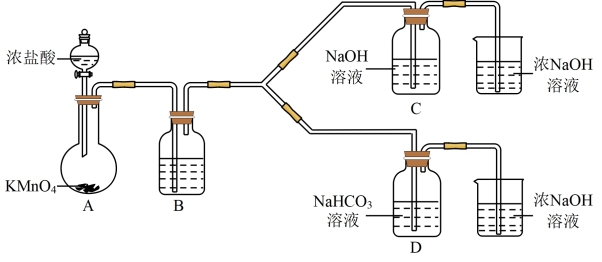
(1)制备NaClO的离子反应方程式___________ 。
(2)结合资料i,写出D中反应的化学方程式___________ 。
II.利用消毒液的性质探究碘水的制备方法
将某品牌“84消毒液”稀释10倍,各取100mL于三个烧杯中,设计如下实验方案制备碘水:
(3)针对烧杯3“滴加淀粉溶液不变蓝”的原因,提出两种假设:
假设1:过量的NaClO将反应生成的I2氧化为 。
。
设计实验a证实了假设1成立。NaClO氧化I2生成 的离子方程式是
的离子方程式是___________ 。
假设2:生成的I2在碱性溶液中不能存在。
设计实验b证实了假设2成立,实验b的操作及现象是___________ 。
(4)某小组检验烧杯3所得溶液中含 :取烧杯3所得无色溶液少许,加入稀硫酸酸化的KI溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在
:取烧杯3所得无色溶液少许,加入稀硫酸酸化的KI溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在 ,说明理由
,说明理由___________ 。
(5)预测烧杯1反应后加淀粉溶液的实验现象,结合方程式说明预测依据___________ 。
资料:i.HClO的电离常数为Ka=4.7×10-8;H2CO3的电离常数为K1=4.3×10-7、K2=5.6×10-11
ii.碘的化合物主要以I-和
 的形式存在,
的形式存在, +5I-+6H+=3I2+3H2O。
+5I-+6H+=3I2+3H2O。iii.碘单质能与I-反应:I2+I-

 (
( 低浓度时显黄色,高浓度时为棕色)。
低浓度时显黄色,高浓度时为棕色)。I制备消毒液(夹持装置略)

(1)制备NaClO的离子反应方程式
(2)结合资料i,写出D中反应的化学方程式
II.利用消毒液的性质探究碘水的制备方法
将某品牌“84消毒液”稀释10倍,各取100mL于三个烧杯中,设计如下实验方案制备碘水:
| 方案 | 操作 | 现象 | 反应后加淀粉溶液 |
| 1 | 烧杯1溶液中加入9gKI固体 | |溶液为橙黄色 | …… |
| 2 | 烧杯2溶液中加入9gKI固体,再加入1mol/L盐酸10mL | 溶液颜色快速加深,呈紫红色 | 变蓝 |
| 3 | 烧杯3溶液中加入少量KI固体(小于0.5g) | 振荡后溶液保持无色 | 不变蓝 |
假设1:过量的NaClO将反应生成的I2氧化为
 。
。设计实验a证实了假设1成立。NaClO氧化I2生成
 的离子方程式是
的离子方程式是假设2:生成的I2在碱性溶液中不能存在。
设计实验b证实了假设2成立,实验b的操作及现象是
(4)某小组检验烧杯3所得溶液中含
 :取烧杯3所得无色溶液少许,加入稀硫酸酸化的KI溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在
:取烧杯3所得无色溶液少许,加入稀硫酸酸化的KI溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在 ,说明理由
,说明理由(5)预测烧杯1反应后加淀粉溶液的实验现象,结合方程式说明预测依据
您最近一年使用:0次
2022-05-31更新
|
507次组卷
|
3卷引用:北京市第一六六中学2022届高三下学期三模化学试题
名校
8 . 常温下,向20mL0.2mol/LH2X溶液中滴加0.2mol/LNaOH溶液,溶液中各微粒的物质的量分数随pH的变化如图所示,以下说法不正确的是


| A.由图可推测,H2X为弱酸 |
| B.滴加过程中发生的反应有:H2X+OH-=HX-+H2O,HX-+OH-=X2-+H2O |
| C.水的电离程度:a点与b点大致相等 |
| D.若常温下Ka(HY)=1.1×10-2,HY与少量Na2X发生的反应是:2HY+X2-=H2X+2Y- |
您最近一年使用:0次
2022-05-06更新
|
812次组卷
|
11卷引用:北京市昌平区2022届高三二模化学试题
北京市昌平区2022届高三二模化学试题北京市育才学校2022届高三下学期三模化学试题(已下线)专题13 水溶液中的离子平衡-备战2023年高考化学母题题源解密(全国通用)湖南省株洲市九方中学2021-2022学年高二下学期期末考试化学试题黑龙江省哈尔滨市实验中学2022-2023学年高三上学期期中考试化学试题山东省青岛市莱西市2022-2023学年高二上学期12月期末考试化学试题黑龙江省哈尔滨市第一中学校2023-2024学年高二上学期期末考试化学试卷天津市重点校2023-2024学年高二上学期期末考试化学试题湖北省沙市中学2023-2024学年高二上学期1月期末化学试题黑龙江省哈尔滨市双城区兆麟中学2023-2024学年高二下学期开学验收考试化学黑龙江省哈尔滨市双城区兆麟中学2023-2024学年高二下学期开学化学试题
名校
9 . 电离平衡常数有重要的功能,下列推测不合理的是
| 化学式 | H2CO3 | HCN | HF |
| 电离平衡常数(K) | Ka1=4.5×10-7 Ka2=4.7×10-11 | 6.2×10-10 | 6.8×10-4 |
A.电离出H+的能力:HF>H2CO3>HCN> |
| B.相同物质的量浓度溶液的pH:NaF<NaHCO3<NaCN |
| C.HCN和HF均能与Na2CO3溶液发生反应 |
D.CO2通入NaCN溶液中:CO2+2CN-+H2O=2HCN+ |
您最近一年使用:0次
2022-04-29更新
|
476次组卷
|
6卷引用:北京市丰台区2022届高三二模化学试题
名校
10 . 火法有色金属冶炼烟气制酸过程中会产生大量含砷污酸,采用硫化-石膏中和法处理含砷污酸可获得达标废水,同时实现变废为宝得到多级产品,工艺流程如下:
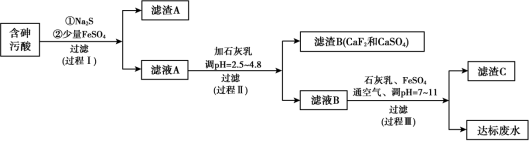
资料:
ⅰ. 常温下H2CO3的Ka1 = 4.4×10-7 ,Ka2 = 4.7×10-11;H2S的Ka1 = 1.3×10-7 ,Ka2 = 7.1×10-15;
ⅱ. 含砷污酸中砷的主要存在形式为亚砷酸(H3AsO3,弱酸),除砷外H+、Cu2+、F-、SO 含量均超标;
含量均超标;
ⅲ.室温下三价砷在水溶液中的存在形式与溶液pH的关系:
(1)工业上制备Na2S时,用NaOH溶液吸收H2S,不能以纯碱代替NaOH。结合方程式解释不能使用纯碱的原因___________ 。
(2)过程Ⅰ可除去含砷污酸中的Cu2+和部分砷,滤渣A 的主要成分为CuS和As2S3,生成As2S3的离子方程式是___________ 。
(3)过程Ⅰ会发生副反应As2S3(s)+3S2-(aq) 2AsS
2AsS (aq),影响后续处理。加入Na2S充分反应后加入少量FeSO4,结合平衡移动原理解释加入FeSO4的原因
(aq),影响后续处理。加入Na2S充分反应后加入少量FeSO4,结合平衡移动原理解释加入FeSO4的原因___________ 。
(4)过程Ⅲ中获得的滤渣C主要成分是FeAsO4, 该过程通入空气的作用是___________ 。
(5)利用反应AsO +2I-+2H+ =AsO
+2I-+2H+ =AsO +I2+H2O 测定滤渣C中FeAsO4含量。取a g样品,用硫酸溶液溶解,加入过量KI,充分反应后将溶液转移至锥形瓶中,以淀粉为指示剂,用c mol·L-1的Na2S2O3标准溶液滴定,观察到
+I2+H2O 测定滤渣C中FeAsO4含量。取a g样品,用硫酸溶液溶解,加入过量KI,充分反应后将溶液转移至锥形瓶中,以淀粉为指示剂,用c mol·L-1的Na2S2O3标准溶液滴定,观察到___________ 现象说明已到滴定终点,重复三次实验,记录用去Na2S2O3溶液体积为V mL,计算样品纯度为 ___________ (用字母表示)。
资料:2Na2S2O3+I2=Na2S4O6+2NaI;FeAsO4相对分子质量为195

资料:
ⅰ. 常温下H2CO3的Ka1 = 4.4×10-7 ,Ka2 = 4.7×10-11;H2S的Ka1 = 1.3×10-7 ,Ka2 = 7.1×10-15;
ⅱ. 含砷污酸中砷的主要存在形式为亚砷酸(H3AsO3,弱酸),除砷外H+、Cu2+、F-、SO
 含量均超标;
含量均超标;ⅲ.室温下三价砷在水溶液中的存在形式与溶液pH的关系:
| pH值 | pH<7 | pH=10~11 |
| 主要存在形式 | H3AsO3 | H2AsO |
(2)过程Ⅰ可除去含砷污酸中的Cu2+和部分砷,滤渣A 的主要成分为CuS和As2S3,生成As2S3的离子方程式是
(3)过程Ⅰ会发生副反应As2S3(s)+3S2-(aq)
 2AsS
2AsS (aq),影响后续处理。加入Na2S充分反应后加入少量FeSO4,结合平衡移动原理解释加入FeSO4的原因
(aq),影响后续处理。加入Na2S充分反应后加入少量FeSO4,结合平衡移动原理解释加入FeSO4的原因(4)过程Ⅲ中获得的滤渣C主要成分是FeAsO4, 该过程通入空气的作用是
(5)利用反应AsO
 +2I-+2H+ =AsO
+2I-+2H+ =AsO +I2+H2O 测定滤渣C中FeAsO4含量。取a g样品,用硫酸溶液溶解,加入过量KI,充分反应后将溶液转移至锥形瓶中,以淀粉为指示剂,用c mol·L-1的Na2S2O3标准溶液滴定,观察到
+I2+H2O 测定滤渣C中FeAsO4含量。取a g样品,用硫酸溶液溶解,加入过量KI,充分反应后将溶液转移至锥形瓶中,以淀粉为指示剂,用c mol·L-1的Na2S2O3标准溶液滴定,观察到资料:2Na2S2O3+I2=Na2S4O6+2NaI;FeAsO4相对分子质量为195
您最近一年使用:0次
2022-04-16更新
|
516次组卷
|
3卷引用:北京市顺义区2021-2022学年高三下学期4月第二次统练化学试题
北京市顺义区2021-2022学年高三下学期4月第二次统练化学试题北京市第十二中学2022-2023学年高二下学期3月练习化学试题(已下线)专项15 工艺流程综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)



