名校
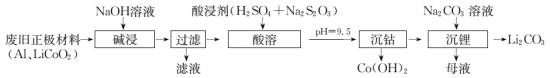
1 . 某工厂以废旧电池正极材料为主要原料制取Li2CO3及Co(OH)2,其工艺流程如图所示(LiCoO2难溶于水及碱溶液,酸性条件下+3价的钴具有强氧化性)。
回答下列问题:
(1)要提高“碱浸”速率,可以采取的措施有______ 、______ (写两条)。“碱浸”时发生反应的方程式为_______ 。
(2)以2.00 mol∙L−1的H2SO4标准液滴定20.00mL“碱浸”所用的NaOH溶液,试剂a为指示剂,达到滴定终点时消耗15.00mLH2SO4标准液。
①2.00 mol∙L−1的H2SO4标准液中,c水(H+)=______ mol∙L−1。
②试剂a为_____ ,c(NaOH)=______ mol∙L−1。
(3)温度升高“滤液”碱性增强,其原因是______ 。
(4)某温度下,Co(OH)2、CoCO3达到溶解平衡的某悬浊液中,c(Co2+)=10−5 mol∙L−1,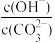 =
=______ {Ksp[Co(OH)2]=4×10−15,Ksp(CoCO3)=1×10−13}。

回答下列问题:
(1)要提高“碱浸”速率,可以采取的措施有
(2)以2.00 mol∙L−1的H2SO4标准液滴定20.00mL“碱浸”所用的NaOH溶液,试剂a为指示剂,达到滴定终点时消耗15.00mLH2SO4标准液。
①2.00 mol∙L−1的H2SO4标准液中,c水(H+)=
②试剂a为
(3)温度升高“滤液”碱性增强,其原因是
(4)某温度下,Co(OH)2、CoCO3达到溶解平衡的某悬浊液中,c(Co2+)=10−5 mol∙L−1,
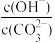 =
=
您最近一年使用:0次
2 . 化学实验和查阅资料有助于我们进一步加强对所学知识的巩固,某班同学在老师的指导下展开了对铁及其化合物的延伸学习
(1)实验组同学分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol•L﹣1的溶液。在配制FeCl2溶液时需加入少量铁屑,其目的是_____
(2)甲组同学取2 mLFeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯气反应的离子方程式为_____
(3)乙组同学认为甲组的实验不够严谨,该组同学在2 mLFeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是_____
(4)丙组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为_____
(5)丁组同学在完成实验后又对高铁酸钠(Na2FeO4)是一种高效多功能水处理剂产生了兴趣,查阅资料获得如下知识:
Ⅰ.高铁酸钠具有很强的氧化性;
Ⅱ.高铁酸钠投入水中的反应为:4Na2FeO4+10H2O═8NaOH+4Fe(OH)3+3O2↑
Ⅲ.湿法制备的主要离子反应为:2Fe(OH)3+3ClO﹣+4OH﹣═2FeO42﹣+3Cl﹣+H2O
干法制备的主要反应为:2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑
①湿法中的还原剂为_____ 。
②干法中每生成1moNa2FeO4,转移电子的物质的量为_____
③高铁酸钠能作为高效多功能水处理剂的原因_____ 、_____
(1)实验组同学分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol•L﹣1的溶液。在配制FeCl2溶液时需加入少量铁屑,其目的是
(2)甲组同学取2 mLFeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯气反应的离子方程式为
(3)乙组同学认为甲组的实验不够严谨,该组同学在2 mLFeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是
(4)丙组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为
(5)丁组同学在完成实验后又对高铁酸钠(Na2FeO4)是一种高效多功能水处理剂产生了兴趣,查阅资料获得如下知识:
Ⅰ.高铁酸钠具有很强的氧化性;
Ⅱ.高铁酸钠投入水中的反应为:4Na2FeO4+10H2O═8NaOH+4Fe(OH)3+3O2↑
Ⅲ.湿法制备的主要离子反应为:2Fe(OH)3+3ClO﹣+4OH﹣═2FeO42﹣+3Cl﹣+H2O
干法制备的主要反应为:2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑
①湿法中的还原剂为
②干法中每生成1moNa2FeO4,转移电子的物质的量为
③高铁酸钠能作为高效多功能水处理剂的原因
您最近一年使用:0次
名校
解题方法
3 . 下列有关物质的性质与用途不具有 对应关系的是
| A.FeCl3具有氧化性,可用作净水剂 |
| B.NH4Cl溶液呈酸性,可用于除铁锈剂 |
| C.小苏打可以与酸反应,可用作抗酸药 |
| D.SO2具有还原性,可用作葡萄酒抗氧化剂 |
您最近一年使用:0次
名校
解题方法
4 . 下列钠及其化合物的性质与用途具有对应关系的是
| A.Na质软,可用于冶炼金属钛 |
B. 溶液显碱性,可用于去除物品表面的油污 溶液显碱性,可用于去除物品表面的油污 |
C. 具有还原性,可用于吸收 具有还原性,可用于吸收 尾气 尾气 |
D. 呈淡黄色,可用于呼吸面罩中作供氧剂 呈淡黄色,可用于呼吸面罩中作供氧剂 |
您最近一年使用:0次
2023-11-21更新
|
179次组卷
|
2卷引用:江苏省徐州市2023-2024学年高三上学期期中考试化学试题
名校
解题方法
5 . VA族元素及其化合物应用广泛。 催化氧化生成
催化氧化生成 ,
, 继续被氧化为
继续被氧化为 ,将
,将 通入水中制取
通入水中制取 。工业上用白磷(
。工业上用白磷( )与
)与 反应生成
反应生成 和一种盐,该盐可与
和一种盐,该盐可与 反应制备一元弱酸
反应制备一元弱酸 。雌黄(
。雌黄( )和
)和 在盐酸中反应转化为雄黄(
在盐酸中反应转化为雄黄( )和
)和 (沸点114℃)并放出
(沸点114℃)并放出 气体。砷化镓(
气体。砷化镓( )是第三代半导体材料,熔点高,硬度大。下列氮及其化合物的性质与用途具有对应关系的是
)是第三代半导体材料,熔点高,硬度大。下列氮及其化合物的性质与用途具有对应关系的是
 催化氧化生成
催化氧化生成 ,
, 继续被氧化为
继续被氧化为 ,将
,将 通入水中制取
通入水中制取 。工业上用白磷(
。工业上用白磷( )与
)与 反应生成
反应生成 和一种盐,该盐可与
和一种盐,该盐可与 反应制备一元弱酸
反应制备一元弱酸 。雌黄(
。雌黄( )和
)和 在盐酸中反应转化为雄黄(
在盐酸中反应转化为雄黄( )和
)和 (沸点114℃)并放出
(沸点114℃)并放出 气体。砷化镓(
气体。砷化镓( )是第三代半导体材料,熔点高,硬度大。下列氮及其化合物的性质与用途具有对应关系的是
)是第三代半导体材料,熔点高,硬度大。下列氮及其化合物的性质与用途具有对应关系的是A. 难溶于水,可用作瓜果保护气 难溶于水,可用作瓜果保护气 | B. 溶液呈酸性,可用于除铁锈 溶液呈酸性,可用于除铁锈 |
C. 具有还原性,可用作制冷剂 具有还原性,可用作制冷剂 | D. 具有强氧化性,可用于制硝酸铵 具有强氧化性,可用于制硝酸铵 |
您最近一年使用:0次
解题方法
6 . 下列有关物质性质与用途对应关系不正确 的是
| A.Na2CO3溶液呈碱性,可用除油污 | B.明矾易溶于水,可用作净水剂 |
| C.ClO2具有强氧化性,可用作消毒剂 | D.FeCl3具有氧化性,可用于蚀刻电路板 |
您最近一年使用:0次
名校
解题方法
7 . 对下列家务劳动所涉及原理的解释不正确的是
| 选项 | 家务劳动 | 化学知识 |
| A | 餐后将铁锅洗净后擦干 | Fe在潮湿的空气中易生锈 |
| B | 使用白醋除去水壶中的水垢 | 白醋可与CaCO3、Mg(OH)2反应 |
| C | 使用“84”消毒液(主要成分为NaClO、NaCl)进行环境消毒 | NaCl具有强氧化性 |
| D | 用温热的纯碱溶液清洗油污 | 油脂在碱性条件下可发生水解反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-07-29更新
|
308次组卷
|
3卷引用:2023年江苏省扬州市普通高中学业水平合格性模拟试卷(二)化学试题
名校
解题方法
8 . 铁及其化合物可制得FeSO4·7H2O、FeCl3、K2FeO4等化工产品,它们在生产、生活中具有广泛应用,印刷电路板原理:2FeCl3+Cu=2FeCl2+CuCl2。下列关于物质的性质与用途具有对应关系的是
| A.Fe具有还原性,可用作抗氧化剂 | B.Fe具有导电性,可用于湿法炼铜 |
| C.FeCl3溶液具有氧化性,可用于净水 | D.FeCl3溶液呈酸性,可用于刻蚀铜板 |
您最近一年使用:0次
2022-03-22更新
|
335次组卷
|
4卷引用:江苏省靖江高级中学、丹阳中学、沭阳中学三校2021-2022学年高三上学期12月联考化学试题
江苏省靖江高级中学、丹阳中学、沭阳中学三校2021-2022学年高三上学期12月联考化学试题(已下线)易错点06 铁及其化合物-备战2023年高考化学考试易错题广东省梅州市大埔县虎山中学2022-2023学年高三上学期12月月考化学试题(已下线)2019年高考浙江卷化学试题变式题(单选题21-25)
9 . 氮元素及其化合物在自然界中广泛存在且具有重要应用。氮的氧化物有NO、 等,氢化物有
等,氢化物有 、
、 等,同时含氮的物质还包括
等,同时含氮的物质还包括 、
、 、
、 等。自然界中固氮主要生成氮氧化物。工业合成氨中,
等。自然界中固氮主要生成氮氧化物。工业合成氨中, (g)与足量的
(g)与足量的 (g)反应生成1mol
(g)反应生成1mol  (g)放出46.2kJ的热量。
(g)放出46.2kJ的热量。 是重要的化工原料,通过催化氧化可以实现
是重要的化工原料,通过催化氧化可以实现 转变为氮氧化物。柴油汽车中常需要补充
转变为氮氧化物。柴油汽车中常需要补充 来进行尾气处理,含
来进行尾气处理,含 的废水在碱性条件下可用电解法进行处理,N与Si组成的
的废水在碱性条件下可用电解法进行处理,N与Si组成的 硬度媲美金刚石。下列物质结构与性质或物质性质与用途具有对应关系的是
硬度媲美金刚石。下列物质结构与性质或物质性质与用途具有对应关系的是
 等,氢化物有
等,氢化物有 、
、 等,同时含氮的物质还包括
等,同时含氮的物质还包括 、
、 、
、 等。自然界中固氮主要生成氮氧化物。工业合成氨中,
等。自然界中固氮主要生成氮氧化物。工业合成氨中, (g)与足量的
(g)与足量的 (g)反应生成1mol
(g)反应生成1mol  (g)放出46.2kJ的热量。
(g)放出46.2kJ的热量。 是重要的化工原料,通过催化氧化可以实现
是重要的化工原料,通过催化氧化可以实现 转变为氮氧化物。柴油汽车中常需要补充
转变为氮氧化物。柴油汽车中常需要补充 来进行尾气处理,含
来进行尾气处理,含 的废水在碱性条件下可用电解法进行处理,N与Si组成的
的废水在碱性条件下可用电解法进行处理,N与Si组成的 硬度媲美金刚石。下列物质结构与性质或物质性质与用途具有对应关系的是
硬度媲美金刚石。下列物质结构与性质或物质性质与用途具有对应关系的是A. 与 与 分子之间形成氢键,可用作制冷剂 分子之间形成氢键,可用作制冷剂 |
B. 溶液显酸性,可用来除铁锈 溶液显酸性,可用来除铁锈 |
C. 是离子晶体,受热不容易分解 是离子晶体,受热不容易分解 |
D. 具有氧化性,可用于处理汽车尾气 具有氧化性,可用于处理汽车尾气 |
您最近一年使用:0次
2023-12-04更新
|
168次组卷
|
2卷引用:江苏省南通市如东县2023-2024学年高三上学期期中考试化学试卷
解题方法
10 . 三氯化六氨合钴(Ⅲ){[Co(NH3)6]Cl3}是制备其它三价钴配合物的重要试剂。实验室以含钴单质(杂质不溶于盐酸)为原料经二氯化钴制备[Co(NH3)6]Cl3·6H2O 晶体。
已知:① Co2+不易被氧化,Co3+具有强氧化性;[Co(NH3)6]2+具有较强还原性,[Co(NH3)6]3+性质稳定。
② [Co(NH3)6]Cl3·6H2O 在水中的溶解度随温度的升高而增大,加入浓盐酸有利于晶体析出。
(1)溶解。将钴单质溶于稀盐酸,过滤除去杂质,得到CoCl2溶液。写出该反应的化学方程式___________ 。
(2)混合。向CoCl2溶液中加入少量NH4Cl溶液,加入活性炭作催化剂。加入的 NH4Cl溶液有利于后续Co2+与NH3的配合反应,其原理是___________ 。
(3)配合、氧化。如图装置,先向三颈烧瓶滴加过量氨水、H2O2中的一种,充分反应,再向混合溶液中滴加另一种溶液,加热,充分搅拌,生成的[Co(NH3)6]Cl3吸附在活性炭上。

①另一种溶液是___________ 。
②控制三颈烧瓶中溶液温度为60℃的原因是___________ 。
③加入H2O2溶液时发生反应的离子方程式为___________ 。
(4)制备[Co(NH3)6]Cl3·6H2O。请补充完整实验方案:将三颈烧瓶中所得混合物___________ ,低温干燥。
已知:稀盐酸可将吸附在活性炭上的[Co(NH3)6]Cl3溶解。
实验中须使用的试剂:稀盐酸、浓盐酸、无水乙醇。
已知:① Co2+不易被氧化,Co3+具有强氧化性;[Co(NH3)6]2+具有较强还原性,[Co(NH3)6]3+性质稳定。
② [Co(NH3)6]Cl3·6H2O 在水中的溶解度随温度的升高而增大,加入浓盐酸有利于晶体析出。
(1)溶解。将钴单质溶于稀盐酸,过滤除去杂质,得到CoCl2溶液。写出该反应的化学方程式
(2)混合。向CoCl2溶液中加入少量NH4Cl溶液,加入活性炭作催化剂。加入的 NH4Cl溶液有利于后续Co2+与NH3的配合反应,其原理是
(3)配合、氧化。如图装置,先向三颈烧瓶滴加过量氨水、H2O2中的一种,充分反应,再向混合溶液中滴加另一种溶液,加热,充分搅拌,生成的[Co(NH3)6]Cl3吸附在活性炭上。

①另一种溶液是
②控制三颈烧瓶中溶液温度为60℃的原因是
③加入H2O2溶液时发生反应的离子方程式为
(4)制备[Co(NH3)6]Cl3·6H2O。请补充完整实验方案:将三颈烧瓶中所得混合物
已知:稀盐酸可将吸附在活性炭上的[Co(NH3)6]Cl3溶解。
实验中须使用的试剂:稀盐酸、浓盐酸、无水乙醇。
您最近一年使用:0次



