1 . 化学深入生活、生产的方方面面。下列物质应用正确的是
| A.镧镍合金用作储氢材料 | B.二氧化硅用作太阳能电池板 |
| C.热的纯碱溶液可用于除铁锈 | D.铁粉用作食品包装袋中的干燥剂 |
您最近一年使用:0次
解题方法
2 . 离子反应和氧化还原反应是高中化学的重要内容之一,下列有关说法正确的是
| A.碘化氢与双氧水反应时,H2O2作还原剂 |
B.Fe2+有还原性, 有强氧化性,故Fe2+与 有强氧化性,故Fe2+与 不能大量共存 不能大量共存 |
C.泡沫灭火器的原理:Al3+ + 3 =Al(OH)3↓+3CO2↑ =Al(OH)3↓+3CO2↑ |
| D.往硫化铜悬浊液中滴加稀硫酸:CuS+2H+=H2S+Cu2+ |
您最近一年使用:0次
解题方法
3 . 按要求完成下题。
(1)写出H2S的电离方程式:___________ 。
(2)0.1mol/LNH4Cl溶液中各离子浓度大小顺序为___________ 。
(3)pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,所得溶液显___________ 性。
(4)把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是___________ 。
(5)常温时的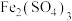 的水溶液
的水溶液
___________ 7(填“>”、“=”、“<”)。原因是___________ (用离子方程式表示)。配制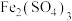 的溶液时,常在溶液中加入一些
的溶液时,常在溶液中加入一些___________ 以抑制其水解。
(6)常温下,pH=10的CH3COONa溶液中,由水电离出的c(OH-)=___________ mol/L。
(7)常温下,0.05mol/LH2SO4溶液的pH=___________ 。
(1)写出H2S的电离方程式:
(2)0.1mol/LNH4Cl溶液中各离子浓度大小顺序为
(3)pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,所得溶液显
(4)把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是
(5)常温时的
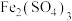 的水溶液
的水溶液
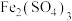 的溶液时,常在溶液中加入一些
的溶液时,常在溶液中加入一些(6)常温下,pH=10的CH3COONa溶液中,由水电离出的c(OH-)=
(7)常温下,0.05mol/LH2SO4溶液的pH=
您最近一年使用:0次
名校
解题方法
4 . 下列实验装置或操作能达到实验目的的是
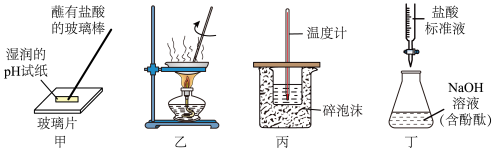
| A.甲操作可以测定盐酸的pH |
| B.乙操作将氯化铁溶液直接蒸发结晶获得无水氯化铁 |
| C.丙装置测定中和热 |
| D.丁装置用于测定NaOH溶液浓度 |
您最近一年使用:0次
名校
解题方法
5 . 下列描述与盐类水解无关 的是
| A.用纯碱溶液清洗油污 |
| B.1 mol·L-1的醋酸加水稀释,溶液的pH增大,导电能力减弱 |
| C.铵态氮肥NH4HCO3与钾肥K2CO3混施可能会降低肥效 |
| D.用FeCl3晶体配制溶液时,先将其溶于较浓盐酸中 |
您最近一年使用:0次
名校
6 . 下列说法正确的是
| A.强电解质溶液导电能力一定比弱电解质溶液导电能力强 |
| B.用已知浓度盐酸滴定未知浓度的氨水时可选择酚酞为指示剂 |
| C.AlCl3和 FeCl3均既可作净水剂也可作消毒剂 |
| D.将碳酸钠溶液蒸干并灼烧,所得固体的成分仍为碳酸钠 |
您最近一年使用:0次
名校
7 . 下列做法中,主要依据的不是盐类水解原理的是
A.实验室配制 溶液时,往往在 溶液时,往往在 溶液中加入少量的盐酸 溶液中加入少量的盐酸 |
| B.游泳馆常用可溶性铜盐作游泳池水的消毒剂 |
C.用 和 和 两种溶液可作泡沫灭火剂 两种溶液可作泡沫灭火剂 |
| D.用明矾做净水剂吸附水中的悬浮杂质 |
您最近一年使用:0次
名校
8 . 下列变化与勒夏特列原理无关的是
| A.红棕色的NO2体系加压后,颜色先变深后逐渐变浅 |
| B.将0.01mol/LFeCl3溶液加热,溶液的颜色加深 |
| C.在配制硫酸亚铁溶液时往往要加入少量铁粉 |
| D.加热蒸干AlCl3溶液不能得到无水AlCl3 |
您最近一年使用:0次
2024-06-21更新
|
87次组卷
|
2卷引用:广东省东莞第一中学、东莞实验中学等三校2023-2024学年高二下学期联考化学试题
名校
解题方法
9 . 下列实验操作规范且能达到目的的是
| 目的 | 操作 | |
| A | 取20.00 mL盐酸 | 在50 mL酸式滴定管中装入盐酸,调整初始读数为30.00 mL后,将剩余盐酸放入锥形瓶 |
| B | 探究浓度对反应速率的影响 | 向2支盛有5mL不同浓度NaHSO3溶液的试管中同时加入2mL 5%H2O2溶液,观察实验现象 |
| C | 测定醋酸钠溶液pH | 用玻璃棒蘸取溶液,点在湿润的pH试纸上 |
| D | 配制氯化铁溶液 | 将氯化铁固体溶解在较浓的盐酸中再加水稀释 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
10 . 化学与生活密切相关。下列说法错误的是
| A.疫苗冷藏存放可减小蛋白质变性的速率 |
| B.FeS可作为沉淀剂除去污水中重金属离子 |
| C.碳酸钡常作X射线透视肠胃的内服造影剂 |
| D.碳酸钠可用于去除餐具的油污 |
您最近一年使用:0次



