1 . 某研究小组拟在实验室以废铁屑(含有少量炭和 杂质)为原料制备无水
杂质)为原料制备无水 ,设计如下流程(已知
,设计如下流程(已知 易水解):
易水解):不正确 的是
 杂质)为原料制备无水
杂质)为原料制备无水 ,设计如下流程(已知
,设计如下流程(已知 易水解):
易水解):
| A.试剂X可选用硫酸 |
B.“氧化”时: |
| C.操作①②均需用到漏斗、烧杯、玻璃棒 |
| D.“脱水”时可能会产生亚铁盐 |
您最近一年使用:0次
2 . 物质的性质决定其用途,下列有关物质性质和应用的关系正确的是
A. 的水解程度很大,可用来制备 的水解程度很大,可用来制备 |
| B.钠能与水剧烈反应,可用作95%乙醇的强除水剂 |
| C.碳酸氢铵受热易分解,可用作植物生长的肥料 |
D. 是酸性氧化物,能用氢氟酸(HF)雕刻玻璃 是酸性氧化物,能用氢氟酸(HF)雕刻玻璃 |
您最近一年使用:0次
3 .  可用作理离子电池的电解质。以LiF、HF和
可用作理离子电池的电解质。以LiF、HF和 为原料制备
为原料制备 的某工艺流程如图所示:
的某工艺流程如图所示: 极易水解。下列说法错误的是
极易水解。下列说法错误的是
 可用作理离子电池的电解质。以LiF、HF和
可用作理离子电池的电解质。以LiF、HF和 为原料制备
为原料制备 的某工艺流程如图所示:
的某工艺流程如图所示: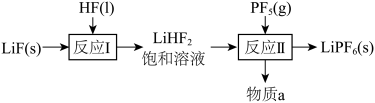
 极易水解。下列说法错误的是
极易水解。下列说法错误的是| A.“反应I”中HF既作反应物又作溶剂 | B.“反应Ⅱ”结束后,可使用玻璃漏斗过滤得到 |
| C.物质a可在该流程中循环使用 | D.整个制备过程需要在低温、干燥条件下进行 |
您最近一年使用:0次
4 . 化学与生产生活密切相关,下列物质应用中涉及氧化还原反应的是
A.利用葡萄糖酸- -内酯使豆浆凝固 -内酯使豆浆凝固 | B.使用含氟牙膏预防龋齿 |
| C.将植物油氢化以便于运输和储存 | D.利用明矾溶液清除铜镜表面的铜锈 |
您最近一年使用:0次
昨日更新
|
68次组卷
|
2卷引用:湖南省2024届普通高中高三下学期学业水平选择性考试临考预测押题密卷化学试题(B卷)
名校
5 . 下列各组离子在溶液中可以大量共存,且加入试剂后发生反应的离子方程式书写也正确的是
选项 | 微粒组 | 加入试剂 | 发生反应的离子方程式 |
A |  、 、 、 、 、 、 | 少量HCl溶液 | 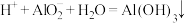 |
B |  、 、 、 、 、 、 | 少量 溶液 溶液 | 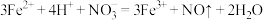 |
C | 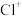 、 、 、 、 、 、 | 过量醋酸溶液 | 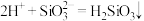 |
D |  、 、 、 、 、 、 | 通入少量 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
6 . 在西汉刘安组织编撰的《淮南万毕术》中,有“曾青得铁则化为铜”的记载。下列说法错误的是
| A.这个反应是湿法冶金的基础,冶金过程中金属元素都发生还原反应 |
| B.铁表面镀锌可以增强其抗腐蚀性 |
| C.中国古代利用明矾溶液的酸性清除铜镜表面的铜锈 |
| D.还原铁粉可以在食品包装袋内做脱氧剂 |
您最近一年使用:0次
7 . 五氯化锑(SbCl5)主要用作氟化工的催化剂、纺织工业织物的阻燃剂、染料工业的中间体。实验室根据反应 ,利用如下装置制备SbCl5 (加热及夹持装置略)。
,利用如下装置制备SbCl5 (加热及夹持装置略)。
实验室制备SbCl5的步骤如下:
ⅰ.保持80℃的条件,在盛有SbCl3的三颈烧瓶中通入Cl2,反应生成SbCl5;
ⅱ.将三颈烧瓶中的反应混合物转移到双颈烧瓶中;
ⅲ.减压蒸馏,收集目标物质。
回答下列问题:
(1)写出用K2MnO4和浓盐酸制备Cl2的离子方程式___________ ,其中体现还原性和酸性的HCl的物质的量之比为___________ 。
(2)实验装置中,两个冷凝管___________ (填“能”或“不能”)交换使用,步骤ⅰ中对三颈烧瓶进行加热的最佳方式是___________ 加热。
(3)写出图示实验装置存在的一处弊端:___________ 。
(4)步骤ⅱ将反应后混合液转移至双颈烧瓶中的方法:在b处连接减压装置,使三颈烧瓶中的液体流入双颈烧瓶。进行该操作前,需___________ (填活塞1和2的开、关的情况)。
(5)步骤ⅲ采用减压蒸馏,而不是常压蒸馏的原因是___________ ;调节减压装置至1.86kPa,收集___________ ℃左右的馏分。减压蒸馏时,玻璃毛细管的作用有___________ (填字母)。
a.防止暴沸 b.搅拌 c.连通大气,保持常压
 ,利用如下装置制备SbCl5 (加热及夹持装置略)。
,利用如下装置制备SbCl5 (加热及夹持装置略)。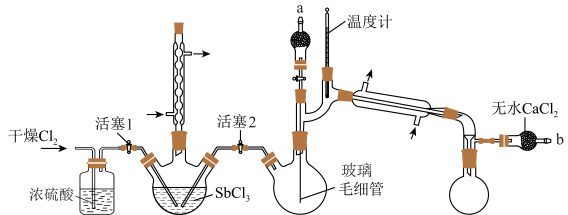
| 物质 | 熔点/℃ | 沸点/℃ | 性质 |
| SbCl3 | 73.4 | 223(101.3kPa) | 均极易水解 |
| SbCl5 | 2.8 | 176(101.3kPa,140℃)时分解 | |
| 68(1.86kPa)、79(2.90kPa) |
ⅰ.保持80℃的条件,在盛有SbCl3的三颈烧瓶中通入Cl2,反应生成SbCl5;
ⅱ.将三颈烧瓶中的反应混合物转移到双颈烧瓶中;
ⅲ.减压蒸馏,收集目标物质。
回答下列问题:
(1)写出用K2MnO4和浓盐酸制备Cl2的离子方程式
(2)实验装置中,两个冷凝管
(3)写出图示实验装置存在的一处弊端:
(4)步骤ⅱ将反应后混合液转移至双颈烧瓶中的方法:在b处连接减压装置,使三颈烧瓶中的液体流入双颈烧瓶。进行该操作前,需
(5)步骤ⅲ采用减压蒸馏,而不是常压蒸馏的原因是
a.防止暴沸 b.搅拌 c.连通大气,保持常压
您最近一年使用:0次
8 . 化学与生活息息相关。下列叙述错误的是
| A.饮用水加明矾杀菌消毒和净水 | B.水果罐头里添加 作抗氧化剂 作抗氧化剂 |
| C.热的纯碱溶液常作餐具洗涤剂 | D.聚乙烯塑料常用作食品外包装材料 |
您最近一年使用:0次
9 . 下列有关实验操作的叙述错误的是
| A.用剩的药品能否放回原试剂瓶,应视具体情况而定 |
| B.在蒸馏操作中,应先通入冷凝水再加热蒸馏烧瓶 |
C.在实验室配制 溶液时,常将 溶液时,常将 晶体先溶于较浓的盐酸中,再加水稀释 晶体先溶于较浓的盐酸中,再加水稀释 |
| D.提纯混有少量硝酸钾的氯化钠,应先在较高温度下制得浓溶液,再冷却结晶、过滤、干燥 |
您最近一年使用:0次
10 . 硫酰氯( )是一种重要的化工试剂,被广泛应用于制造医药品、染料、表面活性剂等。某兴趣小组在实验室利用
)是一种重要的化工试剂,被广泛应用于制造医药品、染料、表面活性剂等。某兴趣小组在实验室利用 和
和 反应合成
反应合成 。
。
已知:① 。
。
② 的熔点为
的熔点为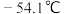 ,沸点为
,沸点为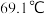 ;
; 以上会分解;遇水能发生剧烈反应,并产生白雾。
以上会分解;遇水能发生剧烈反应,并产生白雾。
回答下列问题:
(1)从甲~戊中选择合适的装置(可以重复选用)制备 ,正确的连接顺序是
,正确的连接顺序是
_______  (用小写字母表示)。
(用小写字母表示)。_______ ;仪器Y中盛放的试剂为_______ (填名称),其作用为_______ 。
(3)装置丙中发生反应的离子方程式为_______ 。
(4)装置丁的作用有除去少量 气体、平衡气压和
气体、平衡气压和_______ 。
(5)硫酰氯纯度的测定:取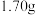 硫酰氯产品在密闭条件下溶于烧碱溶液,最后定容为
硫酰氯产品在密闭条件下溶于烧碱溶液,最后定容为 溶液,取
溶液,取 该溶液于锥形瓶中,调
该溶液于锥形瓶中,调 为
为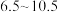 ,加入少量
,加入少量 作指示剂,用
作指示剂,用 的
的 标准溶液滴定(滴定过程中
标准溶液滴定(滴定过程中 不参与反应),平行滴定三次,平均消耗
不参与反应),平行滴定三次,平均消耗 标准溶液
标准溶液 。
。
①下列操作使测定结果偏低的是_______ (填字母)。
A.调节 过低
过低
B.滴定终点时,俯视标准液液面读数
C.锥形瓶未用待测液润洗
②该硫酰氯产品的纯度为_______ 。
(6)亚硫酰氯( )易水解,被广泛应用于结晶水合物的脱水。将
)易水解,被广泛应用于结晶水合物的脱水。将 与
与 混合并加热,可得到无水
混合并加热,可得到无水 ,写出该反应的化学方程式:
,写出该反应的化学方程式:_______ 。
 )是一种重要的化工试剂,被广泛应用于制造医药品、染料、表面活性剂等。某兴趣小组在实验室利用
)是一种重要的化工试剂,被广泛应用于制造医药品、染料、表面活性剂等。某兴趣小组在实验室利用 和
和 反应合成
反应合成 。
。已知:①
 。
。②
 的熔点为
的熔点为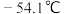 ,沸点为
,沸点为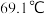 ;
; 以上会分解;遇水能发生剧烈反应,并产生白雾。
以上会分解;遇水能发生剧烈反应,并产生白雾。回答下列问题:
(1)从甲~戊中选择合适的装置(可以重复选用)制备
 ,正确的连接顺序是
,正确的连接顺序是
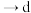 (用小写字母表示)。
(用小写字母表示)。
(3)装置丙中发生反应的离子方程式为
(4)装置丁的作用有除去少量
 气体、平衡气压和
气体、平衡气压和(5)硫酰氯纯度的测定:取
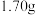 硫酰氯产品在密闭条件下溶于烧碱溶液,最后定容为
硫酰氯产品在密闭条件下溶于烧碱溶液,最后定容为 溶液,取
溶液,取 该溶液于锥形瓶中,调
该溶液于锥形瓶中,调 为
为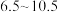 ,加入少量
,加入少量 作指示剂,用
作指示剂,用 的
的 标准溶液滴定(滴定过程中
标准溶液滴定(滴定过程中 不参与反应),平行滴定三次,平均消耗
不参与反应),平行滴定三次,平均消耗 标准溶液
标准溶液 。
。①下列操作使测定结果偏低的是
A.调节
 过低
过低B.滴定终点时,俯视标准液液面读数
C.锥形瓶未用待测液润洗
②该硫酰氯产品的纯度为
(6)亚硫酰氯(
 )易水解,被广泛应用于结晶水合物的脱水。将
)易水解,被广泛应用于结晶水合物的脱水。将 与
与 混合并加热,可得到无水
混合并加热,可得到无水 ,写出该反应的化学方程式:
,写出该反应的化学方程式:
您最近一年使用:0次



