解题方法
1 . 下列反应的离子方程式书写正确的是
A.向 溶液中滴加稀 溶液中滴加稀 : :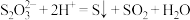 |
B.将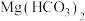 溶液长时间煮沸时形成水垢: 溶液长时间煮沸时形成水垢: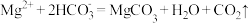 |
C.铅酸蓄电池充电时的阴极反应: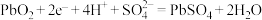 |
D.向含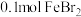 的溶液中通入 的溶液中通入 |
您最近一年使用:0次
2 . 草酸钴是制作氧化钴和金属钴的原料。一种利用含钴废料(主要成分为 ,含少量
,含少量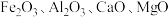 、碳及有机物)制取
、碳及有机物)制取 的工艺流程如图所示:
的工艺流程如图所示: 。
。
(1)“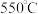 焙烧”的目的是
焙烧”的目的是_______ ,提高焙烧速率的措施有_______ 。
(2)“碱浸”过程中发生反应的离子方程式是_______ 。
(3)基态 原子的价电子排布式是
原子的价电子排布式是_______ ;“钴浸出”过程中,不能用盐酸代替硫酸,原因是_______ 。
(4)“净化除杂1”过程中,先在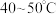 加入
加入 的作用是
的作用是_______ ;再升温至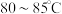 ,加入
,加入 溶液,调
溶液,调 至4.5沉铁,该反应的离子方程式为
至4.5沉铁,该反应的离子方程式为_______ 。
(5)“净化除杂2”过程中,加入 以除去原溶液中的
以除去原溶液中的 (浓度为
(浓度为 )和
)和 ,若控制溶液中
,若控制溶液中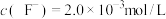 ,则
,则 的去除率准确值为
的去除率准确值为_______ 。[已知某温度下,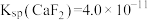 ]
]
 ,含少量
,含少量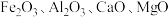 、碳及有机物)制取
、碳及有机物)制取 的工艺流程如图所示:
的工艺流程如图所示: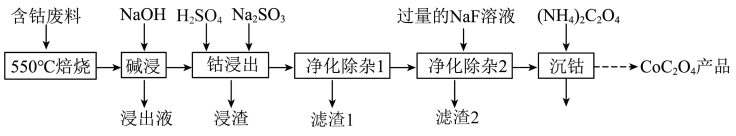
 。
。(1)“
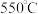 焙烧”的目的是
焙烧”的目的是(2)“碱浸”过程中发生反应的离子方程式是
(3)基态
 原子的价电子排布式是
原子的价电子排布式是(4)“净化除杂1”过程中,先在
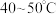 加入
加入 的作用是
的作用是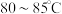 ,加入
,加入 溶液,调
溶液,调 至4.5沉铁,该反应的离子方程式为
至4.5沉铁,该反应的离子方程式为(5)“净化除杂2”过程中,加入
 以除去原溶液中的
以除去原溶液中的 (浓度为
(浓度为 )和
)和 ,若控制溶液中
,若控制溶液中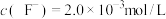 ,则
,则 的去除率准确值为
的去除率准确值为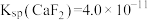 ]
]
您最近一年使用:0次
名校
解题方法
3 . 资料显示Fe2+呈淡绿色、Fe3+呈棕黄色、FeSO3是墨绿色沉淀Fe(OH)3胶体是红褐色液体。某高三老师在讲授“Fe3+的氧化性”时,组织学生进行探究实验。
(1)在课堂教学探究Na2SO3溶液与FeCl3溶液的实际反应时,同学们有以下猜想,请补充完整:
猜想一:Na2SO3溶液与FeCl3溶液发生氧化还原反应;
猜想二:Na2SO3溶液与FeCl3溶液发生双水解反应,产生了Fe(OH)3胶体;
猜想三:___________ 。
(2)甲同学认可猜想一,他预测的实验现象是_____ ,其反应的离子方程式为____ 。
老师安排甲同学做了如下实验i:
(3)乙同学观察实验现象后认为猜想二合理,并想用红色激光笔照射该红褐色液体以验证自己的猜想正确,他预测的现象是_____ 。实验发现,乙同学的猜想成立,反应的离子方程式为_____ 。
(4)针对“氧化还原反应有没有发生”,老师组织同学们讨论,同学们思考得出以下检验方案:
方案①:取少量W液体,加铁氰化钾溶液,检验是否有Fe2+
方案②:取少量W液体,加酸性高锰酸钾溶液,检验是否有Fe2+
方案③:取少量W液体,加盐酸酸化,再加氯化钡溶液,检验是否有
你认为方案②______ (填“合理”或“不合理”),你的理由是______ 。
甲同学在老师的指导下迅速完成了实验ii:
乙同学也在老师的指导下完成了方案①的操作,发现有蓝色沉淀生成。
通过实验探究,大家认识到Fe3+与 的反应体系中,氧化还原反应与水解反应不仅共存还存在竞争。
的反应体系中,氧化还原反应与水解反应不仅共存还存在竞争。
(1)在课堂教学探究Na2SO3溶液与FeCl3溶液的实际反应时,同学们有以下猜想,请补充完整:
猜想一:Na2SO3溶液与FeCl3溶液发生氧化还原反应;
猜想二:Na2SO3溶液与FeCl3溶液发生双水解反应,产生了Fe(OH)3胶体;
猜想三:
(2)甲同学认可猜想一,他预测的实验现象是
老师安排甲同学做了如下实验i:
| 装置 | 操作 | 现象 |
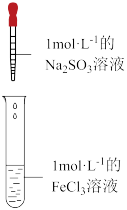 | 向2mL1mol•L-1的FeCl3溶液中,逐滴滴加2mL1mol•L-1的Na2SO3溶液 | 溶液黄色逐渐加深,最终得到红褐色液体(W) |
(4)针对“氧化还原反应有没有发生”,老师组织同学们讨论,同学们思考得出以下检验方案:
方案①:取少量W液体,加铁氰化钾溶液,检验是否有Fe2+
方案②:取少量W液体,加酸性高锰酸钾溶液,检验是否有Fe2+
方案③:取少量W液体,加盐酸酸化,再加氯化钡溶液,检验是否有

你认为方案②
甲同学在老师的指导下迅速完成了实验ii:
| 装置 | 操作 | 现象 |
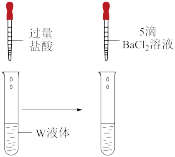 | 取1mLW液体于试管中,滴加过量盐酸,再滴加5滴BaCl2溶液 | 产生白色沉淀 |
通过实验探究,大家认识到Fe3+与
 的反应体系中,氧化还原反应与水解反应不仅共存还存在竞争。
的反应体系中,氧化还原反应与水解反应不仅共存还存在竞争。
您最近一年使用:0次
2020-12-01更新
|
323次组卷
|
2卷引用:贵州省罗甸县边阳中学2022届高三模拟测试化学试题



