1 . 回答下列问题:
(1)实验室在配制 的溶液时,常将
的溶液时,常将 固体先溶于较浓的硝酸中,再用蒸馏水稀释到所需的浓度,其目是
固体先溶于较浓的硝酸中,再用蒸馏水稀释到所需的浓度,其目是________________ 。
(2)将 溶液蒸干再灼烧,最后得到的主要固体物质是
溶液蒸干再灼烧,最后得到的主要固体物质是______ (写化学式,下同);将 溶液蒸干再灼烧,最后得到的主要固体物质是
溶液蒸干再灼烧,最后得到的主要固体物质是______ 。
(3)已知 晶体在空气中加热时,释放部分结晶水,同时生成
晶体在空气中加热时,释放部分结晶水,同时生成 (碱式氯化镁)或
(碱式氯化镁)或 ,下列是关于
,下列是关于 的综合应用:
的综合应用:______ 环境中加热。
(4)某小组同学探究饱和 和
和 溶液混合反应的实验,打开活塞向烧瓶中的
溶液混合反应的实验,打开活塞向烧瓶中的 加入饱和
加入饱和 溶液,产生大量的白色胶状沉淀,出现上述现象的原因是
溶液,产生大量的白色胶状沉淀,出现上述现象的原因是__________ (请用反应的离子方程式表示)。
(1)实验室在配制
 的溶液时,常将
的溶液时,常将 固体先溶于较浓的硝酸中,再用蒸馏水稀释到所需的浓度,其目是
固体先溶于较浓的硝酸中,再用蒸馏水稀释到所需的浓度,其目是(2)将
 溶液蒸干再灼烧,最后得到的主要固体物质是
溶液蒸干再灼烧,最后得到的主要固体物质是 溶液蒸干再灼烧,最后得到的主要固体物质是
溶液蒸干再灼烧,最后得到的主要固体物质是(3)已知
 晶体在空气中加热时,释放部分结晶水,同时生成
晶体在空气中加热时,释放部分结晶水,同时生成 (碱式氯化镁)或
(碱式氯化镁)或 ,下列是关于
,下列是关于 的综合应用:
的综合应用: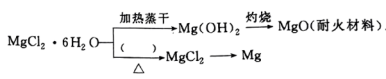
(4)某小组同学探究饱和
 和
和 溶液混合反应的实验,打开活塞向烧瓶中的
溶液混合反应的实验,打开活塞向烧瓶中的 加入饱和
加入饱和 溶液,产生大量的白色胶状沉淀,出现上述现象的原因是
溶液,产生大量的白色胶状沉淀,出现上述现象的原因是
您最近一年使用:0次
2 . 下列说法中,与盐的水解无关的正确说法是
①明矾可以做净水剂;
②实验室配制FeCl3溶液时,往往在FeCl3溶液中加入少量的盐酸;
③用NaHCO3和Al2(SO4)3两种溶液可作泡沫灭火剂;
④在NH4Cl溶液中加入金属镁会产生氢气;⑤草木灰与铵态氮肥不能混合施用;
⑥比较NH4Cl和Na2S等某些盐溶液的酸碱性。
| A.①④⑥ | B.②③⑤ | C.③④⑤ | D.全有关 |
您最近一年使用:0次
名校
解题方法
3 . 从宏观现象探究微观本质是重要的化学学科素养。为研究FeCl3溶液的性质,某小组同学进行了如下探究实验。
Ⅰ.配制FeCl3溶液
(1)先将FeCl3固体溶于浓盐酸,再稀释至指定浓度。浓盐酸的作用是______ 。
Ⅱ.FeCl3溶液与Na2CO3溶液反应
(2)向2mL1mol/L的Na2CO3溶液中加入2mL1mol/LFeCl3溶液,产生了红褐色沉淀和无色气体。反应的离子方程式为______ 。
Ⅲ.FeCl3溶液与Na2S溶液反应
(3)甲同学认为Fe3+和S2-的水解平衡相互促进并完全水解,实验中会观察到红褐色沉淀并闻到臭鸡蛋气味;乙同学认为会发生氧化还原反应,并预测还原产物为______ (填化学式)。两位同学实验如下:
(4)两位同学猜测实验a中的黑色沉淀可能是Fe2S3。继续实验:
根据实验b说明黑色沉淀是Fe2S3,写出实验b中Fe2S3与盐酸反应的化学方程式:______ 。
(5)①实验a中生成黑色沉淀Fe2S3的离子方程式为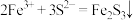 。该反应类型从四种基本反应类型看属于
。该反应类型从四种基本反应类型看属于______ 。
②实验a中Fe2S3溶解时生成的黄色固体为______ ,乙同学推测是因为随着FeCl3溶液滴加至一定量, 浓度增大,其氧化性增强,将Fe2S3氧化所致。
浓度增大,其氧化性增强,将Fe2S3氧化所致。
(6)已知: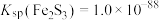 ,
,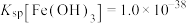 。针对实验a过程中未观察到红褐色沉淀,甲同学认为可能是产生的量比较少,被黑色所遮盖。乙同学根据
。针对实验a过程中未观察到红褐色沉淀,甲同学认为可能是产生的量比较少,被黑色所遮盖。乙同学根据 数据计算认为就算产生红褐色沉淀,也会转化为黑色沉淀,写出该转化过程的离子方程式:
数据计算认为就算产生红褐色沉淀,也会转化为黑色沉淀,写出该转化过程的离子方程式:______ 。
Ⅰ.配制FeCl3溶液
(1)先将FeCl3固体溶于浓盐酸,再稀释至指定浓度。浓盐酸的作用是
Ⅱ.FeCl3溶液与Na2CO3溶液反应
(2)向2mL1mol/L的Na2CO3溶液中加入2mL1mol/LFeCl3溶液,产生了红褐色沉淀和无色气体。反应的离子方程式为
Ⅲ.FeCl3溶液与Na2S溶液反应
(3)甲同学认为Fe3+和S2-的水解平衡相互促进并完全水解,实验中会观察到红褐色沉淀并闻到臭鸡蛋气味;乙同学认为会发生氧化还原反应,并预测还原产物为
| 实验a | 向稀Na2S溶液中逐滴加入FeCl3稀溶液,直至过量 |
| 实验现象 | 立即产生黑色沉淀并逐渐增加,无臭鸡蛋气味;FeCl3溶液过量后,黑色沉淀部分溶解,出现黄色沉淀 |
| 实验b | 将实验a中黑色沉淀过滤,并用CS2处理后洗净。向沉淀中加入6mol/L的盐酸,振荡试管 |
| 实验现象 | 加入盐酸后黑色沉淀溶解,转为乳黄色沉淀,并伴有臭鸡蛋气味 |
(5)①实验a中生成黑色沉淀Fe2S3的离子方程式为
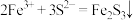 。该反应类型从四种基本反应类型看属于
。该反应类型从四种基本反应类型看属于②实验a中Fe2S3溶解时生成的黄色固体为
 浓度增大,其氧化性增强,将Fe2S3氧化所致。
浓度增大,其氧化性增强,将Fe2S3氧化所致。(6)已知:
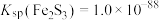 ,
,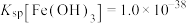 。针对实验a过程中未观察到红褐色沉淀,甲同学认为可能是产生的量比较少,被黑色所遮盖。乙同学根据
。针对实验a过程中未观察到红褐色沉淀,甲同学认为可能是产生的量比较少,被黑色所遮盖。乙同学根据 数据计算认为就算产生红褐色沉淀,也会转化为黑色沉淀,写出该转化过程的离子方程式:
数据计算认为就算产生红褐色沉淀,也会转化为黑色沉淀,写出该转化过程的离子方程式:
您最近一年使用:0次
名校
解题方法
4 . 下列离子方程式书写正确的是
[已知:
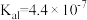
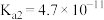

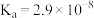 ]
]
[已知:

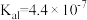
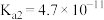

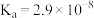 ]
]A.泡沫灭火器的原理: |
B.少量氯气通入碳酸钠溶液中: |
C.用铅电极电解 溶液: 溶液: |
D.向 悬浊液中通入 悬浊液中通入 气体: 气体: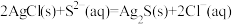 |
您最近一年使用:0次
名校
5 . 常温下,下列离子组在指定溶液中能大量共存的是
A.在1mol/L的FeCl3溶液中:NH 、Na+、SO 、Na+、SO 、NO 、NO |
B.使甲基橙变红的溶液中:Fe2+、Na+、SO 、NO 、NO |
C. 的溶液中: 的溶液中: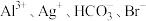 |
D.pH=1的溶液中:Na+、Mg2+、NO 、CH3COO- 、CH3COO- |
您最近一年使用:0次
名校
解题方法
6 . 某废合金的主要成分为Sn、Cu、Pb、Fe,一种综合回收的工艺流程如图所示:
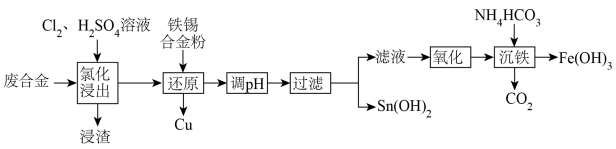
已知:常温下,Ksp(PbCl2)=1.6×10-5,Ksp(PbSO4)=1.6×10-8,Ksp[Sn(OH)2]=1.0×10-27.85。
回答下列问题:
(1)“氯化浸出”浸出液中金属阳离子主要有Sn4+、Cu2+、______ ;浸渣的主要成分为______ (填化学式)。“氯化没出”时温度不宜过高或过低的原因是_______ 。
(2)写出“还原”中Fe与SnCl4反应的化学方程式:_______ 。
(3)常温下,为使Sn2+完全沉淀,“调pH”时应使溶液pH不低于______ (结果保留1位小数)。
(4)写出“沉铁”时发生反应的离子反应方程式:_______ 。
(5)Fe(OH)3受热后可制得物质A,写出物质A的一种用途:______ 。

已知:常温下,Ksp(PbCl2)=1.6×10-5,Ksp(PbSO4)=1.6×10-8,Ksp[Sn(OH)2]=1.0×10-27.85。
回答下列问题:
(1)“氯化浸出”浸出液中金属阳离子主要有Sn4+、Cu2+、
(2)写出“还原”中Fe与SnCl4反应的化学方程式:
(3)常温下,为使Sn2+完全沉淀,“调pH”时应使溶液pH不低于
(4)写出“沉铁”时发生反应的离子反应方程式:
(5)Fe(OH)3受热后可制得物质A,写出物质A的一种用途:
您最近一年使用:0次
名校
7 . 25℃时,下列各组离子在指定溶液中能大量共存的是
A.能使石蕊变红的溶液: , , , , |
B.澄清透明的溶液: , , , , |
C. 的溶液: 的溶液: , , , , |
D.含 的溶液: 的溶液: , , , , |
您最近一年使用:0次
2024-03-02更新
|
98次组卷
|
2卷引用:甘肃省兰州市第五十五中学2023-2024学年高二下学期开学测试化学试卷
8 . 常温下,下列各组离子在指定溶液中能大量共存的是
A.使甲基橙呈红色的溶液中: |
B.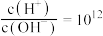 的水溶液中: 的水溶液中: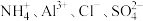 |
C.由水电离出的 的溶液中: 的溶液中: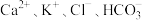 |
D. 的溶液中: 的溶液中: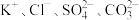 |
您最近一年使用:0次
名校
解题方法
9 . 下列各组离子在指定溶液中一定能大量共存的是
A.澄清透明溶液中: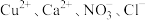 |
B.滴加石蕊试液显红色的溶液中: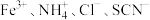 |
C.与Al反应产生H2的溶液中: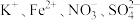 |
D.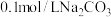 溶液中: 溶液中: |
您最近一年使用:0次
2024-01-22更新
|
114次组卷
|
3卷引用:江西省宜春市丰城中学东校区(九中)2023-2024学年高二下学期开学考试化学试卷
名校
解题方法
10 . 25℃时,下列各组离子在指定溶液中一定能大量共存的是
A. 108的溶液中: 108的溶液中: 、 、 、 、 、Ba2+ 、Ba2+ |
B.使甲基橙变红色的溶液: 、 、 、 、 、CO 、CO |
C.无色溶液中: 、 、 、 、 、 、 |
D.由水电离出的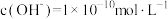 的溶液中:Fe2+、Cl-、 的溶液中:Fe2+、Cl-、 、 、 |
您最近一年使用:0次
2023-11-20更新
|
355次组卷
|
3卷引用:江西省宜春市宜丰中学2023-2024学年高二下学期开学考试化学试题



