解题方法
1 .  在生产和生活中用途广泛。
在生产和生活中用途广泛。
Ⅰ. 溶液的配制及浓度的标定
溶液的配制及浓度的标定
(1) 溶液的配制
溶液的配制
①配制100mL一定浓度的 溶液需用到的仪器有
溶液需用到的仪器有___________ (填字母)。 溶液时,需要将
溶液时,需要将 固体溶解在浓盐酸中,原因为
固体溶解在浓盐酸中,原因为___________ 。
(2) 溶液浓度的标定
溶液浓度的标定
量取10.00mL 溶液于碘量瓶中,加入过量KI溶液,充分反应后加入少量淀粉溶液、再用
溶液于碘量瓶中,加入过量KI溶液,充分反应后加入少量淀粉溶液、再用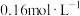
 标准溶液滴定至蓝色恰好消失,重复操作三次,平均消耗
标准溶液滴定至蓝色恰好消失,重复操作三次,平均消耗 标准溶液的体积为20.00mL,已知:
标准溶液的体积为20.00mL,已知: ,则该
,则该 溶液的浓度为
溶液的浓度为___________  。
。
Ⅱ. 与
与 反应的探究
反应的探究
(3)预测现象1:向 溶液中加入
溶液中加入 溶液,溶液由黄色变为浅绿色。作出该预测的原因为
溶液,溶液由黄色变为浅绿色。作出该预测的原因为___________ (用离子方程式表示)。
预测现象2:向 溶液中加入
溶液中加入 溶液,生成红褐色沉淀。
溶液,生成红褐色沉淀。
(4)实验验证:小组同学设计以下实验探究溶液中 浓度相同时
浓度相同时 的加入量对反应的影响,其中
的加入量对反应的影响,其中 溶液为Ⅰ中所配溶液,
溶液为Ⅰ中所配溶液, 溶液浓度为
溶液浓度为 。静置6小时观察现象,测定反应后溶液的pH,并记录数据:
。静置6小时观察现象,测定反应后溶液的pH,并记录数据:
①请补充表格中的数据:a=___________ 。
②实验ⅱ~ⅳ中,反应后溶液的pH基本不变,其原因可能是___________ 。
③实验ⅵ和ⅶ的实验现象说明溶液中 的水解与
的水解与 的水解相互促进(即发生了双水解反应),请写出反应的化学方程式:
的水解相互促进(即发生了双水解反应),请写出反应的化学方程式:___________ 。
④甲同学认为实验ⅵ和ⅶ中, 与
与 除发生双水解反应外,还发生了氧化还原反应。请设计实验证明猜想:分别取实验ⅵ和ⅶ中上层清液于两支试管中,
除发生双水解反应外,还发生了氧化还原反应。请设计实验证明猜想:分别取实验ⅵ和ⅶ中上层清液于两支试管中,___________ (填实验操作与现象),则说明猜想成立。
(5)请举出一种水解反应在生产或生活中的应用:___________ 。
 在生产和生活中用途广泛。
在生产和生活中用途广泛。Ⅰ.
 溶液的配制及浓度的标定
溶液的配制及浓度的标定(1)
 溶液的配制
溶液的配制①配制100mL一定浓度的
 溶液需用到的仪器有
溶液需用到的仪器有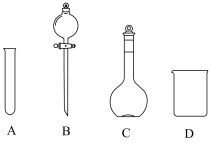
 溶液时,需要将
溶液时,需要将 固体溶解在浓盐酸中,原因为
固体溶解在浓盐酸中,原因为(2)
 溶液浓度的标定
溶液浓度的标定量取10.00mL
 溶液于碘量瓶中,加入过量KI溶液,充分反应后加入少量淀粉溶液、再用
溶液于碘量瓶中,加入过量KI溶液,充分反应后加入少量淀粉溶液、再用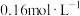
 标准溶液滴定至蓝色恰好消失,重复操作三次,平均消耗
标准溶液滴定至蓝色恰好消失,重复操作三次,平均消耗 标准溶液的体积为20.00mL,已知:
标准溶液的体积为20.00mL,已知: ,则该
,则该 溶液的浓度为
溶液的浓度为 。
。Ⅱ.
 与
与 反应的探究
反应的探究(3)预测现象1:向
 溶液中加入
溶液中加入 溶液,溶液由黄色变为浅绿色。作出该预测的原因为
溶液,溶液由黄色变为浅绿色。作出该预测的原因为预测现象2:向
 溶液中加入
溶液中加入 溶液,生成红褐色沉淀。
溶液,生成红褐色沉淀。(4)实验验证:小组同学设计以下实验探究溶液中
 浓度相同时
浓度相同时 的加入量对反应的影响,其中
的加入量对反应的影响,其中 溶液为Ⅰ中所配溶液,
溶液为Ⅰ中所配溶液, 溶液浓度为
溶液浓度为 。静置6小时观察现象,测定反应后溶液的pH,并记录数据:
。静置6小时观察现象,测定反应后溶液的pH,并记录数据:| 序号 | ⅰ | ⅱ | ⅲ | ⅳ | ⅴ | ⅵ | ⅶ |
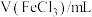 | 2.0 | 2.0 | 2.0 | 2.0 | 2.0 | 2.0 | 2.0 |
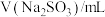 | 0 | 1.0 | 2.0 | 5.0 | a | 20.0 | 26.0 |
 | 38.0 | 37.0 | 36.0 | 33.0 | 23.0 | 18.0 | 12.0 |
| 现象 | 溶液接近无色透明 | 出现褐色沉淀 | |||||
| pH | 1.7 | 1.7 | 1.7 | 1.8 | 2.8 | 5.4 | 6.2 |
②实验ⅱ~ⅳ中,反应后溶液的pH基本不变,其原因可能是
③实验ⅵ和ⅶ的实验现象说明溶液中
 的水解与
的水解与 的水解相互促进(即发生了双水解反应),请写出反应的化学方程式:
的水解相互促进(即发生了双水解反应),请写出反应的化学方程式:④甲同学认为实验ⅵ和ⅶ中,
 与
与 除发生双水解反应外,还发生了氧化还原反应。请设计实验证明猜想:分别取实验ⅵ和ⅶ中上层清液于两支试管中,
除发生双水解反应外,还发生了氧化还原反应。请设计实验证明猜想:分别取实验ⅵ和ⅶ中上层清液于两支试管中,(5)请举出一种水解反应在生产或生活中的应用:
您最近一年使用:0次
名校
解题方法
2 . 酸浸法回收废炉渣中(主要为铜、钴、镍、铁等金属元素的氧化物)的铜、钴、镍的流程如下: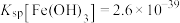 ,
, 。
。
(1)“磨细”过程的目的是_______ 。
(2)酸浸液中大量铁元素以 存在,加入
存在,加入 可减少铁屑的消耗从而降低成本,
可减少铁屑的消耗从而降低成本, 与
与 反应过程中会产生气泡,其离子方程式为
反应过程中会产生气泡,其离子方程式为_______ 。
(3)“滤渣2”主要成分为_______ (填化学式)。
(4)“镍钴分离”过程 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(5)“酸溶1”过程用 替换
替换 ,从绿色化学角度分析其可行性
,从绿色化学角度分析其可行性_______ 。
(6)“焙烧”过程发生反应的化学方程式为_______ 。
(7)已知当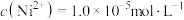 时,认为其沉淀完全。“沉镍”过程的目的是为了将“
时,认为其沉淀完全。“沉镍”过程的目的是为了将“ ”,此时应调节溶液的pH为
”,此时应调节溶液的pH为_______ 。
(8)“操作X”为_______ 。
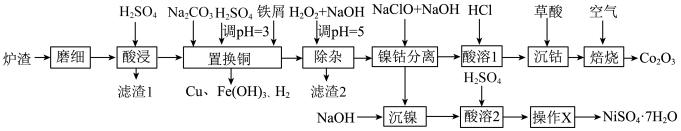
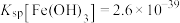 ,
, 。
。(1)“磨细”过程的目的是
(2)酸浸液中大量铁元素以
 存在,加入
存在,加入 可减少铁屑的消耗从而降低成本,
可减少铁屑的消耗从而降低成本, 与
与 反应过程中会产生气泡,其离子方程式为
反应过程中会产生气泡,其离子方程式为(3)“滤渣2”主要成分为
(4)“镍钴分离”过程
 发生反应的离子方程式为
发生反应的离子方程式为(5)“酸溶1”过程用
 替换
替换 ,从绿色化学角度分析其可行性
,从绿色化学角度分析其可行性(6)“焙烧”过程发生反应的化学方程式为
(7)已知当
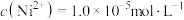 时,认为其沉淀完全。“沉镍”过程的目的是为了将“
时,认为其沉淀完全。“沉镍”过程的目的是为了将“ ”,此时应调节溶液的pH为
”,此时应调节溶液的pH为(8)“操作X”为
您最近一年使用:0次
2024-02-20更新
|
484次组卷
|
2卷引用:福建省2024届名校联盟全国优质校高三大联考化学试题
名校
解题方法
3 . 以废旧锂离子电池(主要成分为 )为原料制备棒状草酸钴晶体(
)为原料制备棒状草酸钴晶体( ,微溶于水,溶解度随温度升高而逐渐增大)的一种方法如下图所示,该法经济可行,为工业化回收废旧锂电池中有色金属提供了依据。
,微溶于水,溶解度随温度升高而逐渐增大)的一种方法如下图所示,该法经济可行,为工业化回收废旧锂电池中有色金属提供了依据。 外,还含
外,还含 、
、 ,
, ,
, ,
, ,
, 等离子;
等离子;
② ,
,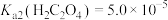 ;
;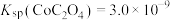 。
。
回答下列问题:
(1)“浸出”时, 与
与 、稀硫酸反应中氧化剂与还原剂的物质的量之比为
、稀硫酸反应中氧化剂与还原剂的物质的量之比为___________ 。
(2)“水解沉淀铝铜”时,沉淀铝反应的离子方程式为___________ 。
(3)沉淀2的成分为 和
和___________ ,“氧化沉淀铁锰”时,生成 的离子方程式为
的离子方程式为___________ 。
(4)“沉钴”时,温度与钴的沉淀率的关系如图所示,沉淀反应时间为10 min,反应温度为50℃以上时,温度升高,而钴的沉淀率下降,可能原因为___________ 。 溶液代替
溶液代替 ,反应为
,反应为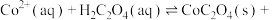
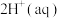 ,则该反应的平衡常数为
,则该反应的平衡常数为___________ ,若平衡时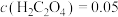 mol⋅L-1,
mol⋅L-1, ,则此时Co2+是否沉淀完全?
,则此时Co2+是否沉淀完全?___________ (填“是”或“否”,离子浓度≤10-5 mol⋅L-1即可认为沉淀完全)。
 )为原料制备棒状草酸钴晶体(
)为原料制备棒状草酸钴晶体( ,微溶于水,溶解度随温度升高而逐渐增大)的一种方法如下图所示,该法经济可行,为工业化回收废旧锂电池中有色金属提供了依据。
,微溶于水,溶解度随温度升高而逐渐增大)的一种方法如下图所示,该法经济可行,为工业化回收废旧锂电池中有色金属提供了依据。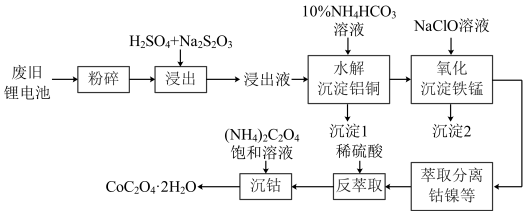
 外,还含
外,还含 、
、 ,
, ,
, ,
, ,
, 等离子;
等离子;②
 ,
,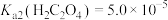 ;
;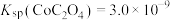 。
。回答下列问题:
(1)“浸出”时,
 与
与 、稀硫酸反应中氧化剂与还原剂的物质的量之比为
、稀硫酸反应中氧化剂与还原剂的物质的量之比为(2)“水解沉淀铝铜”时,沉淀铝反应的离子方程式为
(3)沉淀2的成分为
 和
和 的离子方程式为
的离子方程式为(4)“沉钴”时,温度与钴的沉淀率的关系如图所示,沉淀反应时间为10 min,反应温度为50℃以上时,温度升高,而钴的沉淀率下降,可能原因为
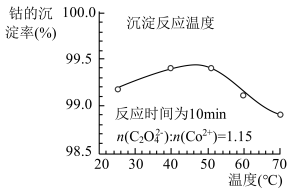
 溶液代替
溶液代替 ,反应为
,反应为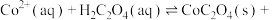
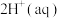 ,则该反应的平衡常数为
,则该反应的平衡常数为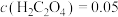 mol⋅L-1,
mol⋅L-1, ,则此时Co2+是否沉淀完全?
,则此时Co2+是否沉淀完全?
您最近一年使用:0次
2024-02-01更新
|
337次组卷
|
2卷引用:江西省宜春市第一中学2023-2024学年高三上学期1月质量检测化学试题



