1 . 已知 ,用
,用 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
 ,用
,用 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是A.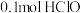 中, 中, 数目为 数目为 |
B.若向水中缓慢通入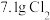 并充分反应,则消耗的水分子数目为 并充分反应,则消耗的水分子数目为 |
C.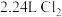 中氯原子数目为 中氯原子数目为 |
D.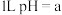 的氯水中, 的氯水中,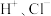 数目的和为 数目的和为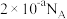 |
您最近一年使用:0次
名校
2 . 在室温下,下列五种溶液:
①0.1 mol·L-1NH4Cl ②0.1 mol·L-1CH3COONH4 ③0.1 mol·L-1NH4HSO4
④0.1 mol·L-1NH3·H2O和 0.1 mol·L-1NH4Cl混合液 ⑤pH=a的CH3COOH
请根据要求填写下列空白:
(1)溶液①呈酸性的原因是___________ (用离子方程式表示)。
(2)比较溶液②、③中c(NH )的大小关系是②
)的大小关系是②___________ ③(填“>”“<”或“=”)。
(3)在溶液④中,NH3·H2O和______ 物质的量浓度之和为0.2 mol·L-1(填微粒符号)。
(4)室温,溶液②的pH=7,CH3COO-与NH 浓度的大小关系是c(CH3COO-)
浓度的大小关系是c(CH3COO-)______ c(NH )(填“>”“<”或“=”)。
)(填“>”“<”或“=”)。
(5)溶液⑤稀释100倍后所得溶液pH___ a+2(填“>”或“<”或“=”)。
①0.1 mol·L-1NH4Cl ②0.1 mol·L-1CH3COONH4 ③0.1 mol·L-1NH4HSO4
④0.1 mol·L-1NH3·H2O和 0.1 mol·L-1NH4Cl混合液 ⑤pH=a的CH3COOH
请根据要求填写下列空白:
(1)溶液①呈酸性的原因是
(2)比较溶液②、③中c(NH
 )的大小关系是②
)的大小关系是②(3)在溶液④中,NH3·H2O和
(4)室温,溶液②的pH=7,CH3COO-与NH
 浓度的大小关系是c(CH3COO-)
浓度的大小关系是c(CH3COO-) )(填“>”“<”或“=”)。
)(填“>”“<”或“=”)。(5)溶液⑤稀释100倍后所得溶液pH
您最近一年使用:0次
2022-04-01更新
|
696次组卷
|
4卷引用:江西省上饶市铅山县第一中学2021-2022学年高二下学期开学考试化学试题
名校
解题方法
3 . 某溶液中只含有Al3+、Na+、Cl-、SO 四种离子,已知前三种离于的个数比为2:3:1,则溶液中Na+和SO
四种离子,已知前三种离于的个数比为2:3:1,则溶液中Na+和SO 的个数比为( )
的个数比为( )
 四种离子,已知前三种离于的个数比为2:3:1,则溶液中Na+和SO
四种离子,已知前三种离于的个数比为2:3:1,则溶液中Na+和SO 的个数比为( )
的个数比为( )| A.2:1 | B.3:4 | C.3:5 | D.2:5 |
您最近一年使用:0次
2020-10-28更新
|
510次组卷
|
5卷引用:江西省兴国县第三中学2020-2021学年上学期高一期中考试化学试题
名校
解题方法
4 . 某溶液中大量存在以下浓度的五种离子:0.4mol/L Cl﹣、0.8mol/L SO42﹣、0.2mol/L Al3+、0.6mol/L H+、M,则M及其物质的量浓度可能为
| A.Na+0.6mol/L | B.CO32﹣0.2 mol/L |
| C.Mg2+0.4 mol/L | D.Ba2+0.4mol/L |
您最近一年使用:0次
2017-01-09更新
|
730次组卷
|
6卷引用:2016-2017学年江西省南昌市八一中学等五校高一上联考二化学试卷



