名校
1 . CuCl为白色粉末,微溶于水,溶于浓盐酸或NaCl浓溶液,不溶于乙醇。一种由海绵铜(Cu和少量CuO等)为原料制备CuCl的工艺流程如图:
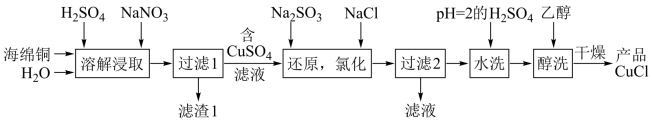
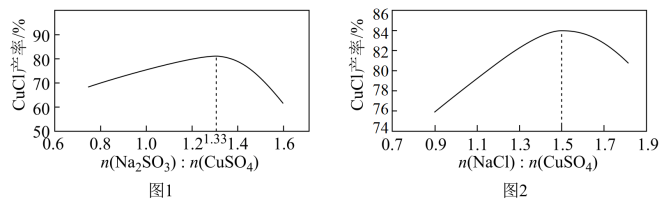
(1)“还原,氯化”时,Na2SO3和NaCl的用量对CuCl产率的影响如图1、图2所示。
①CuSO4与Na2SO3、NaCl在溶液中反应生成CuCl的离子方程式为___ 。
②当n(Na2SO3):n(CuSO4)>1.33时,比值越大CuCl产率越小,其原因是___ 。
③当1.0<n(NaCl):n(CuSO4)<1.5时,比值越大CuCl产率越大,结合沉淀平衡移动原理分析其原因是___ 。
(2)用“醇洗”可快速去除滤渣表面的水,防止滤渣被空气氧化为Cu2(OH)3Cl。CuCl被氧化为Cu2(OH)3Cl的化学方程式为___ 。
(3)为测定某氯化亚铜样品中CuCl的含量,某同学设计如下实验:准确称取氯化亚铜样品mg,将其置于过量的FeCl3溶液中,待固体完全溶解后,加入适量稀硫酸,用amol/L的K2Cr2O7溶液氧化反应生成的Fe2+,消耗K2Cr2O7溶液bmL,反应中Cr2O 被还原为Cr3+,求样品中CuCl的质量分数
被还原为Cr3+,求样品中CuCl的质量分数___ (写计算过程)。

(1)“还原,氯化”时,Na2SO3和NaCl的用量对CuCl产率的影响如图1、图2所示。

①CuSO4与Na2SO3、NaCl在溶液中反应生成CuCl的离子方程式为
②当n(Na2SO3):n(CuSO4)>1.33时,比值越大CuCl产率越小,其原因是
③当1.0<n(NaCl):n(CuSO4)<1.5时,比值越大CuCl产率越大,结合沉淀平衡移动原理分析其原因是
(2)用“醇洗”可快速去除滤渣表面的水,防止滤渣被空气氧化为Cu2(OH)3Cl。CuCl被氧化为Cu2(OH)3Cl的化学方程式为
(3)为测定某氯化亚铜样品中CuCl的含量,某同学设计如下实验:准确称取氯化亚铜样品mg,将其置于过量的FeCl3溶液中,待固体完全溶解后,加入适量稀硫酸,用amol/L的K2Cr2O7溶液氧化反应生成的Fe2+,消耗K2Cr2O7溶液bmL,反应中Cr2O
 被还原为Cr3+,求样品中CuCl的质量分数
被还原为Cr3+,求样品中CuCl的质量分数
您最近一年使用:0次
2021-12-22更新
|
744次组卷
|
7卷引用:江苏省前黄高级中学、如东中学、姜堰中学2021-2022学年高三上学期12月份阶段性测试化学试题
江苏省前黄高级中学、如东中学、姜堰中学2021-2022学年高三上学期12月份阶段性测试化学试题江苏省姜堰中学、如东中学、前黄中学三校2021- 2022学年高三联考化学试题(已下线)黄金卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(江苏卷)江苏省徐州市第七中学2021-2022学年高三下学期2月检测化学试题湖南省益阳市第一中学2021-2022学年高二下学期期末考试化学试题(已下线)2022年江苏卷高考真题变式题14-17(已下线)江苏省2022年普通高中学业水平选择性考试变式题(实验探究题)
名校
2 . 下列表达式正确的是
A.碳酸的电离:H2CO3=H++ |
B.硫化钠水解:S2-+2H2O H2S↑+2OH- H2S↑+2OH- |
C.硫氢根离子的电离:HS-+H2O  H3O++S2- H3O++S2- |
D.CaCO3的溶解平衡:CaCO3  Ca2++ Ca2++ |
您最近一年使用:0次
3 . 环境保护工程师的主要工作包括对环境问题的调查研究、分析检测、管理监督和对环境污染的控制与治理等。下列说法错误的是
| A.空气质量监测项目包括颗粒物、NO2、SO2、CO2等的含量 |
| B.可用光谱分析的方法对环境中的污染物进行分析和鉴定 |
| C.以K2CrO4为指示剂,用AgNO3标准液配位滴定(以配位反应为基础)水体中CN-的含量 |
| D.用氨催化吸收法处理工业尾气中的氮氧化物(NOx) |
您最近一年使用:0次
2021·全国·模拟预测
名校
解题方法
4 . T℃时,CdCO3和Cd(OH)2的沉淀溶解平衡曲线如图所示,已知pCd2+为Cd2+浓度的负对数,pN为阴离子浓度的负对数,下列说法正确的是
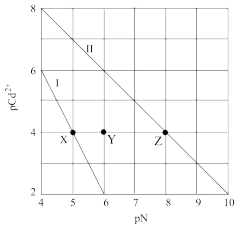

A.X点:c(Cd2+)<c(OH-);Z点:c(CO )<c(Cd2+) )<c(Cd2+) |
| B.溶度积的负对数:pKsp(CdCO3)<pKsp[Cd(OH)2] |
| C.Y点对应的CdCO3溶液为不饱和溶液,可以继续溶解CdCO3 |
D.T℃时,Cd(OH)2(s)+ (aq)⇌CdCO3(s)+2OH-(aq)的平衡常数K为102 (aq)⇌CdCO3(s)+2OH-(aq)的平衡常数K为102 |
您最近一年使用:0次
2021-12-17更新
|
1368次组卷
|
6卷引用:第16周 周测卷-备战2022年高考化学周测与晚练(新高考专用)
(已下线)第16周 周测卷-备战2022年高考化学周测与晚练(新高考专用)河南省商城县观庙高级中学2021-2022学年高二上学期12月月考化学试题福建省福州高级中学2021-2022学年高二上学期期末化学考试题(已下线)【直击双一流】02-备战2022年高考化学名校进阶模拟卷(通用版)(已下线)押江苏卷第13题 水溶液中的离子平衡 -备战2022年高考化学临考题号押题(江苏卷)湖南省株洲市攸县第一中学2022届高三下学期四月月考化学试题
5 . 氯化银固体难溶于水,但在水中存在沉淀溶解平衡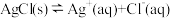

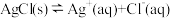 ,对该平衡的说法中
,对该平衡的说法中错误 的是
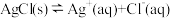

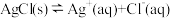 ,对该平衡的说法中
,对该平衡的说法中A.向该平衡中加入 固体,平衡向左移动, 固体,平衡向左移动, 溶解度减小 溶解度减小 |
B.向该平衡中加入 固体,平衡不移动 固体,平衡不移动 |
C.向该平衡中加水,平衡向右移动, 溶解度增大 溶解度增大 |
D.向该平衡中加入 固体,平衡向右移动, 固体,平衡向右移动, 转化为 转化为 |
您最近一年使用:0次
2021-12-15更新
|
412次组卷
|
2卷引用:湘鄂冀三省益阳平高学校、长沙市平高中学等七校联考2021-2022学年高二上学期期中考试化学试题
名校
6 . 已知25℃时,Ksp[Mg(OH)2]=5.61×10-12,Ksp(AgCl)=1.8×10-10,在该温度下,下列判断正确的是
| A.向AgCl浊液中滴入KBr溶液,沉淀变成浅黄色,说明Ksp(AgBr)>Ksp(AgCl) |
| B.向饱和AgCl水溶液中加入NaCl溶液,Ksp(AgCl)减小 |
| C.在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)增大 |
| D.Mg(OH)2固体在氨水中的Ksp比在NH4Cl溶液中的Ksp小 |
您最近一年使用:0次
名校
7 . 氯化银在水中存在溶解平衡:AgCl Ag++Cl—。在相同温度下,将足量氯化银分别放入相同体积的下列溶液中,Ag+的浓度最小的是
Ag++Cl—。在相同温度下,将足量氯化银分别放入相同体积的下列溶液中,Ag+的浓度最小的是
 Ag++Cl—。在相同温度下,将足量氯化银分别放入相同体积的下列溶液中,Ag+的浓度最小的是
Ag++Cl—。在相同温度下,将足量氯化银分别放入相同体积的下列溶液中,Ag+的浓度最小的是| A.0.1mol/L HCl | B.蒸馏水 |
| C.0.1mol/LAlCl3 | D.0.1mol/LMgCl2 |
您最近一年使用:0次
名校
8 . 用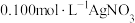 滴定
滴定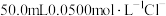 溶液的滴定曲线如图所示。下列有关描述错误的是
溶液的滴定曲线如图所示。下列有关描述错误的是
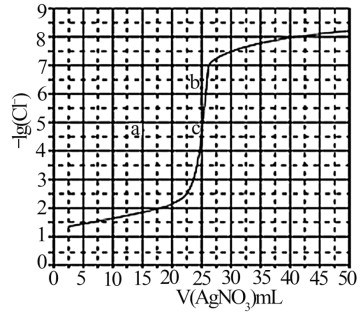
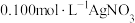 滴定
滴定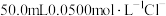 溶液的滴定曲线如图所示。下列有关描述错误的是
溶液的滴定曲线如图所示。下列有关描述错误的是
A.相同实验条件下,若改为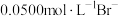 ,反应终点c向b方向移动 ,反应终点c向b方向移动 |
B.曲线上各点的溶液满足关系式 |
C.根据曲线数据计算可知的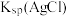 数量级为 数量级为 |
D.相同实验条件下,若改为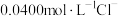 ,反应终点c移到a ,反应终点c移到a |
您最近一年使用:0次
名校
解题方法
9 . 下列相关原理解释不正确 的是
A.向沸水中滴加饱和 溶液制备 溶液制备 胶体: 胶体: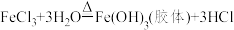 |
B.硫酸氢钠溶于水的电离方程式: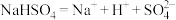 |
C.碳酸钡悬浊液中,溶解平衡表达式: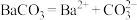 |
D.向 悬浊液中滴加几滴稀 悬浊液中滴加几滴稀 溶液,沉淀逐渐变为黑色的原因: 溶液,沉淀逐渐变为黑色的原因: |
您最近一年使用:0次
名校
10 . 下列表达式书写正确的是
A.CaCO3的电离方程式:CaCO3 Ca2++CO Ca2++CO |
B.HCO 的电离方程式:HCO 的电离方程式:HCO +H2O +H2O H3O++CO H3O++CO |
C.CO 的水解方程式:CO 的水解方程式:CO +2H2O +2H2O H2CO3+2OH- H2CO3+2OH- |
D.CaCO3的沉淀溶解平衡表达式:CaCO3(s)=Ca2+(aq)+CO (aq) (aq) |
您最近一年使用:0次
2021-12-08更新
|
289次组卷
|
4卷引用:广东省梅州市三校(蕉岭中学、虎山中学、平远中学)2021-2022学年高二上学期(11月)联考化学试题



