1 . 已知:常温下 、
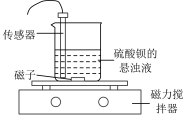
、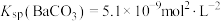 ,向硫酸钡的悬浊液中加入饱和碳酸钠溶液,充分搅拌后静置、分层,装置如图所示。下列说法正确的是
,向硫酸钡的悬浊液中加入饱和碳酸钠溶液,充分搅拌后静置、分层,装置如图所示。下列说法正确的是
 、
、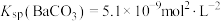 ,向硫酸钡的悬浊液中加入饱和碳酸钠溶液,充分搅拌后静置、分层,装置如图所示。下列说法正确的是
,向硫酸钡的悬浊液中加入饱和碳酸钠溶液,充分搅拌后静置、分层,装置如图所示。下列说法正确的是
| A.下层难溶的固体中含有碳酸钡 | B.下层难溶的固体中只含有硫酸钡 |
| C.下层难溶的固体中只含有碳酸钡 | D.上层溶液中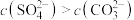 |
您最近一年使用:0次
名校
解题方法
2 . 下列指定反应的离子方程式书写正确的是
| A.工业上生产漂白粉的原理:Cl2+2OH−=Cl−+ClO−+H2O |
B.四氧化三铁溶于足量稀硝酸:3Fe3O4+28H++NO =9Fe3++NO↑+14H2O =9Fe3++NO↑+14H2O |
C.向硫酸氢铵溶液中滴入少量氢氧化钠溶液:NH +OH−=NH3·H2O +OH−=NH3·H2O |
D.氯化银悬浊液滴入过量氨水变澄清:Ag++2NH3·H2O= Ag(NH3) +2H2O +2H2O |
您最近一年使用:0次
名校
3 . 为分析某铜合金的成分,用足量酸将其完全溶解后,用 溶液调节
溶液调节 ,当
,当 时开始出现沉淀,分别在
时开始出现沉淀,分别在 为7.0、8.0时过滤沉淀,结合题图信息推断该合金中除铜外一定含有
为7.0、8.0时过滤沉淀,结合题图信息推断该合金中除铜外一定含有

 溶液调节
溶液调节 ,当
,当 时开始出现沉淀,分别在
时开始出现沉淀,分别在 为7.0、8.0时过滤沉淀,结合题图信息推断该合金中除铜外一定含有
为7.0、8.0时过滤沉淀,结合题图信息推断该合金中除铜外一定含有
A. 、 、 | B. 、 、 | C. 、 、 | D. 、 、 、 、 |
您最近一年使用:0次
2021-11-04更新
|
295次组卷
|
3卷引用:安徽师范大学附属中学2021-2022学年高三上学期11月考试化学试题
名校
解题方法
4 . 工业上利用锌焙砂(主要含ZnO、ZnFe2O4还含有少量FeO、CuO等)湿法制取金属锌的流程如图所示。
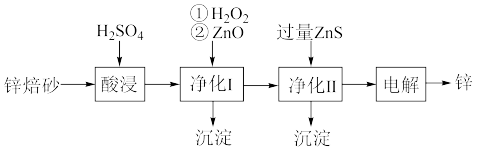
下列说法错误的是

下列说法错误的是
| A.ZnFe2O4溶于硫酸的离子方程式:ZnFe2O4+8H+=Zn2++2Fe3++4H2O |
| B.加入ZnO的目的是调节溶液的pH以除去溶液中的Fe3+ |
| C.加过量ZnS可除去溶液中的Cu2+是利用了Ksp(ZnS)>Ksp(CuS) |
| D.为加快反应速率,净化I和净化II均应在较高的温度下进行 |
您最近一年使用:0次
2021-05-13更新
|
1304次组卷
|
12卷引用:安徽省六安市第一中学2022届高三上学期第三次月考化学试题
安徽省六安市第一中学2022届高三上学期第三次月考化学试题山东省烟台市2021届高三5月二模化学试题(已下线)专题讲座(八) 无机化工流程题的解题策略(精练)-2022年高考化学一轮复习讲练测(已下线)专题12 工艺流程选择题-备战2022年高考化学真题及地市好题专项集训【山东专用】内蒙古通辽和市赤峰市部分学校联考2021-2022学年高三上学期10月联考质量检测化学试题(已下线)2022年山东省高考真题变式题(不定项选择题)湖南省长沙市长郡中学2022-2023学年高三第三次月考化学试题(已下线)作业10 沉淀溶解平衡-2021年高二化学暑假作业(人教版2019)河南省新乡名校2020-2021学年高二下学期期末联考化学试题(已下线)必考点08 沉淀溶解平衡-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版选择性必修1)第三章 综合拔高练黑龙江省大庆实验中学实验二部2023-2024学年高二上学期 期中化学试卷
解题方法
5 . 2020年12月17日,中国探月工程嫦娥五号任务取得圆满成功。嫦娥五号锂离子蓄电池选用了比能量更高的钴酸锂(LiCoO2)正极材料和石墨负极材料。钴是一种稀有的贵重金属,废旧锂离子电池电极材料的回收再生意义重大,钴酸锂回收再生流程如图:

(1)用H2SO4酸浸时,通常需添加30%的H2O2以提高浸出效率,写出相应反应的化学方程式:__ 。
(2)用盐酸代替H2SO4和H2O2,浸出效率也很高。但工业上不使用盐酸,主要原因是会产生有毒、有污染的气体___ (填化学式)。
(3)其他条件不变时,相同反应时间,随着温度升高,含钴酸锂的固体滤渣在H2SO4和30%的H2O2混合液中的浸出率如下表所示,请分析80℃时钴的浸出率最大的原因:___ 。
(4)已知常温下草酸Ka1=5.6×10-2,Ka2=1.5×10-4,Ksp(CoC2O4)=4.0×10-6,求常温下Co2+与草酸反应生成CoC2O4沉淀的平衡常数K=___ 。
(5)高温下,在O2存在时,纯净的CoC2O4与Li2CO3再生为LiCoO2的化学方程式为___ 。
(6)在空气中煅烧CoC2O4生成钴的氧化物和CO2,若测得充分煅烧后固体的质量为3.615g,CO2的体积为2.016L(标准状况),则钴的氧化物的化学式为___ 。

(1)用H2SO4酸浸时,通常需添加30%的H2O2以提高浸出效率,写出相应反应的化学方程式:
(2)用盐酸代替H2SO4和H2O2,浸出效率也很高。但工业上不使用盐酸,主要原因是会产生有毒、有污染的气体
(3)其他条件不变时,相同反应时间,随着温度升高,含钴酸锂的固体滤渣在H2SO4和30%的H2O2混合液中的浸出率如下表所示,请分析80℃时钴的浸出率最大的原因:
| 反应温度/℃ | 60 | 70 | 80 | 90 |
| 钴的浸出率/% | 88 | 90.5 | 93 | 91 |
(4)已知常温下草酸Ka1=5.6×10-2,Ka2=1.5×10-4,Ksp(CoC2O4)=4.0×10-6,求常温下Co2+与草酸反应生成CoC2O4沉淀的平衡常数K=
(5)高温下,在O2存在时,纯净的CoC2O4与Li2CO3再生为LiCoO2的化学方程式为
(6)在空气中煅烧CoC2O4生成钴的氧化物和CO2,若测得充分煅烧后固体的质量为3.615g,CO2的体积为2.016L(标准状况),则钴的氧化物的化学式为
您最近一年使用:0次
6 . 往含I-和Cl-的稀溶液中滴入AgNO3溶液,产生沉淀的质量m(沉淀)与加入AgNO3溶液体积的关系如图所示。已知:Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16。则原溶液中 的比值为( )
的比值为( )

 的比值为( )
的比值为( )
A. | B. | C. | D.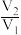 |
您最近一年使用:0次
2020-02-23更新
|
262次组卷
|
6卷引用:2016届安徽省六安一中高三下综合训练十三理综化学试卷
2016届安徽省六安一中高三下综合训练十三理综化学试卷2016届河北省石家庄市高三复习教学质检二理综化学试卷百所名校联考-仿真(三) 标准仿真预测卷2020届高三化学化学二轮复习——常考题型:沉淀溶解平衡的曲线分析【精编25题】(已下线)小题必刷34 沉淀溶解平衡、溶度积常数及其应用——2021年高考化学一轮复习小题必刷(通用版本)福建省莆田第一中学2017-2018学年高二下学期期初考试化学试题



