2021高三·全国·专题练习
1 . 已知:T ℃时,Ksp(PbS)=1.3×10-24,Ksp(ZnS)=1.0×10-22;当溶液中离子浓度≤10-5 mol·L-1时,表明该离子已除尽。T℃时,下列有关ZnS和PbS的说法不正确的是
| A.ZnS的饱和溶液中,c(Zn2+)=c(S2-)=1.0×10-11 mol·L-1 |
| B.欲将某工业废水中的Pb2+除去,则加入Na2S溶液后应保证溶液中c(S2-)≥1.3×10-19mol·L-1 |
| C.向同浓度的ZnCl2和PbCl2的混合溶液中滴加Na2S溶液,PbS先析出 |
| D.向PbS悬浊液中加入ZnCl2浓溶液,PbS不可能转化为ZnS |
您最近一年使用:0次
解题方法
2 . 下列叙述正确的是( )
| A.除去MgCl2溶液中混有的FeCl2溶液工业上一般先将Fe2+氧化为Fe3+再以Fe(OH)3除去,因为Fe(OH)2为白色絮状沉淀不易过滤。 |
| B.向饱和的FeCl3溶液中加入适量的NaOH溶液并加热至溶液呈红褐色,可以制得Fe(OH)3胶体 |
C.向饱和的NaHCO3溶液中滴加酚酞,溶液呈浅红色是因为 电离产生了H+ 电离产生了H+ |
| D.铝箔用砂纸仔细打磨,除去表面的保护膜,在酒精灯上加热会观察到铝受热融化并滴落 |
您最近一年使用:0次
解题方法
3 . 2020年12月17日,中国探月工程嫦娥五号任务取得圆满成功。嫦娥五号锂离子蓄电池选用了比能量更高的钴酸锂(LiCoO2)正极材料和石墨负极材料。钴是一种稀有的贵重金属,废旧锂离子电池电极材料的回收再生意义重大,钴酸锂回收再生流程如图:

(1)用H2SO4酸浸时,通常需添加30%的H2O2以提高浸出效率,写出相应反应的化学方程式:__ 。
(2)用盐酸代替H2SO4和H2O2,浸出效率也很高。但工业上不使用盐酸,主要原因是会产生有毒、有污染的气体___ (填化学式)。
(3)其他条件不变时,相同反应时间,随着温度升高,含钴酸锂的固体滤渣在H2SO4和30%的H2O2混合液中的浸出率如下表所示,请分析80℃时钴的浸出率最大的原因:___ 。
(4)已知常温下草酸Ka1=5.6×10-2,Ka2=1.5×10-4,Ksp(CoC2O4)=4.0×10-6,求常温下Co2+与草酸反应生成CoC2O4沉淀的平衡常数K=___ 。
(5)高温下,在O2存在时,纯净的CoC2O4与Li2CO3再生为LiCoO2的化学方程式为___ 。
(6)在空气中煅烧CoC2O4生成钴的氧化物和CO2,若测得充分煅烧后固体的质量为3.615g,CO2的体积为2.016L(标准状况),则钴的氧化物的化学式为___ 。

(1)用H2SO4酸浸时,通常需添加30%的H2O2以提高浸出效率,写出相应反应的化学方程式:
(2)用盐酸代替H2SO4和H2O2,浸出效率也很高。但工业上不使用盐酸,主要原因是会产生有毒、有污染的气体
(3)其他条件不变时,相同反应时间,随着温度升高,含钴酸锂的固体滤渣在H2SO4和30%的H2O2混合液中的浸出率如下表所示,请分析80℃时钴的浸出率最大的原因:
| 反应温度/℃ | 60 | 70 | 80 | 90 |
| 钴的浸出率/% | 88 | 90.5 | 93 | 91 |
(4)已知常温下草酸Ka1=5.6×10-2,Ka2=1.5×10-4,Ksp(CoC2O4)=4.0×10-6,求常温下Co2+与草酸反应生成CoC2O4沉淀的平衡常数K=
(5)高温下,在O2存在时,纯净的CoC2O4与Li2CO3再生为LiCoO2的化学方程式为
(6)在空气中煅烧CoC2O4生成钴的氧化物和CO2,若测得充分煅烧后固体的质量为3.615g,CO2的体积为2.016L(标准状况),则钴的氧化物的化学式为
您最近一年使用:0次
4 . 下列说法不正确的是
| A.反应MgO(s)+C(s)=Mg(s)+CO(g)在室温下不能自发进行,则该反应的∆H>0 |
| B.向有AgCl固体的饱和溶液中加少许水,c(Ag+)和Ksp(AgCl)都不变 |
C.0.1 mol·L-1CH3COOH溶液加水稀释后,溶液中 的值减小 的值减小 |
| D.锅炉中沉积的CaSO4可用饱和Na2CO3溶液浸泡,再将不溶物用稀盐酸溶解除去 |
您最近一年使用:0次
名校
5 . 下列实验操作、实验现象和实验结论均正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 将大小相同的金属钠分别投入水和乙醇中 | 钠与水反应比钠与乙醇反应剧烈 | 乙醇羟基中的氢原子比水分子中的氢原子活泼 |
| B | 将Fe(NO3)2样品溶于稀H2SO4,滴加KSCN溶液 | 溶液变红 | 稀硫酸能氧化Fe2+ |
| C | 室温下,用pH试纸分别测定浓度为0.1 mol∙L−1NaClO溶液和0.1 mol∙L−1CH3COONa溶液的pH | pH试纸都变成碱色 | 可以用 pH试纸的颜色与标准比色卡比较,从而判断HClO和CH3COOH的酸性强弱 |
| D | 向少量AgNO3溶液中滴加适量NaCl溶液,再滴加适量Na2S溶液 | 开始有白色沉淀生成,后有黑色沉淀生成 | Ksp(Ag2S) <Ksp(AgCl) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-01-01更新
|
579次组卷
|
6卷引用:广东省深圳市皇御苑学校2020-2021学年高二上学期期末测试化学试题
名校
解题方法
6 . 若定义pAg=-lgc(Ag+),pCl=-lgc(C1-),根据不同温度下氯化银饱和溶液的PAg和pCl 可绘制图象如下图所示,且已知氯化银的溶解度随温度的升高而增大,根据该图象,下列表述正确的是


| A.将A点的溶液降温,可能得到C 点的饱和溶液 |
| B.T3 <T2 <T1 |
| C.向B点所表示的溶液中加入氯化钠溶液,溶液可能改变至D点 |
| D.A点表示的是T1温度下的饱和溶液 |
您最近一年使用:0次
2020-12-23更新
|
457次组卷
|
4卷引用:宁夏青铜峡市高级中学2020-2021学年高二上学期期末考试化学试题
宁夏青铜峡市高级中学2020-2021学年高二上学期期末考试化学试题辽宁省实验中学东戴河分校2020-2021学年高二12月月考化学试题(已下线)【教材实验热点】16 难溶电解质的溶解平衡微专题(九)——沉淀溶解平衡曲线
名校
解题方法
7 . 结合水溶液中离子平衡的相关知识回答下列问题:
Ⅰ.温度为 t℃时,某 NaOH 稀溶液中 c(H+)=10-amol·L-1,c(OH-)=10-bmol·L-1,已知:a+b=12,请回答下列问题:
(1)该温度下水的离子积常数 Kw=___________ 。
(2)该 NaOH 溶液中由水电离出的 c(OH-)为___________ 。
Ⅱ.(1)某温度时,Ag2SO4 在水溶液中的沉淀溶解平衡曲线如图所示,计算此温度下 Ag2SO4 的溶度积常数 Ksp(Ag2SO4) =___________ 。

(2)某工业废水中含有 Fe2+、Cu2+、Mg2+等金属离子,且三者浓度相同。此条件下,各金属离子开始沉淀时的 pH 如下:
若采用向该溶液中滴加NaOH溶液的方法除去其中的金属离子,则先沉淀的是___________ 。
Ⅰ.温度为 t℃时,某 NaOH 稀溶液中 c(H+)=10-amol·L-1,c(OH-)=10-bmol·L-1,已知:a+b=12,请回答下列问题:
(1)该温度下水的离子积常数 Kw=
(2)该 NaOH 溶液中由水电离出的 c(OH-)为
Ⅱ.(1)某温度时,Ag2SO4 在水溶液中的沉淀溶解平衡曲线如图所示,计算此温度下 Ag2SO4 的溶度积常数 Ksp(Ag2SO4) =

(2)某工业废水中含有 Fe2+、Cu2+、Mg2+等金属离子,且三者浓度相同。此条件下,各金属离子开始沉淀时的 pH 如下:
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
您最近一年使用:0次
名校
解题方法
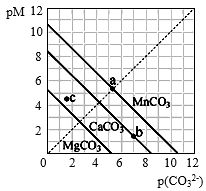
8 . 一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图所示。已知:pM=-lg c(M),p(CO )=-lg c(CO
)=-lg c(CO ),下列说法不正确的是
),下列说法不正确的是
 )=-lg c(CO
)=-lg c(CO ),下列说法不正确的是
),下列说法不正确的是
| A.MgCO3、CaCO3、MnCO3的Ksp依次增大 |
B.a点可表示MnCO3的饱和溶液,且c(Mn2+)=c(CO ) ) |
C.b点可表示CaCO3的饱和溶液,且c(Ca2+)>c(CO ) ) |
D.c点可表示MgCO3的不饱和溶液,且c(Mg2+)<c(CO ) ) |
您最近一年使用:0次
2020-12-14更新
|
318次组卷
|
4卷引用:安徽省庐江县2021-2022学年高二上学期期末考试化学试题
20-21高二上·全国·课后作业
名校
9 . 已知:工业生产中可用ZnS作为沉淀剂除去工业废水中的Cu2+,可表示为Cu2+(aq)+ZnS(s)  Zn2+(aq)+CuS(s)。下列说法不正确的是
Zn2+(aq)+CuS(s)。下列说法不正确的是
 Zn2+(aq)+CuS(s)。下列说法不正确的是
Zn2+(aq)+CuS(s)。下列说法不正确的是| A.相同温度时,溶解度:S(ZnS)>S(CuS) | B.通入气体H2S后,c(Zn2+)变小 |
C.反应平衡常数K=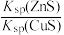 | D.反应达平衡时,c(Cu2+)=c(Zn2+) |
您最近一年使用:0次
2020-12-12更新
|
444次组卷
|
5卷引用:课时1 沉淀溶解平衡及其应用
课时1 沉淀溶解平衡及其应用(已下线)3.4.2 沉淀溶解平衡的应用(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)河南省兰考县第二高级中学2021-2022学年高二上学期第三次考试化学试题(已下线)3.4.2 沉淀溶解平衡的应用(练习)-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)湖南省张家界市民族中学2023-2024学年高二上学期第四次月考化学试题
10 . 某同学为验证Fe3+的氧化性进行了如下实验:
已知相同条件下AgCl的溶解度小于Ag2SO4.下列说法不正确的是
| 序号 | 操作 | 现象 |
| 实验I | 将2 mL 2 mol∙L−1Fe(NO3)3溶液加入有银镜的试管中 | 银镜消失 |
| 实验II | 将2 mL1 mol∙L−1 Fe2(SO4)3溶液加入有银镜的试管中 | 银镜减少,未消失 |
| 实验III | 将2mL2 mol∙L−1FeCl3溶液加入有银镜的试管中 | 银镜消失 |
| 实验IV | 将2mL 1 mol∙L−1 AgNO3溶液加入到1 mL 1 mol∙L−1 FeSO4溶液中 | 产生白色沉淀,随后有黑色固体产生 |
| A.实验I不能说明Fe3+氧化了Ag |
B.实验II和III说明溶液中存在平衡: Fe3++Ag Fe2++ Ag+ Fe2++ Ag+ |
| C.实验IV中产生白色沉淀,说明Ag+氧化了Fe2+ |
| D.欲证明实验IV中产生了Fe3+,可以取上层清液滴加KSCN溶液 |
您最近一年使用:0次



