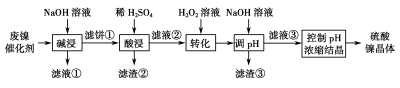
1 . 某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO4·7H2O):
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
利用上述表格数据,计算Ni(OH)2的Ksp=___________ (列出计算式)。如果“转化”后的溶液中Ni2+浓度为1.0 mol·L-1,则“调pH”应控制的pH范围是___________ 。

溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
| 开始沉淀时(c=0.01 mol·L-1)的pH | 7.2 | 3.7 | 2.2 | 7.5 |
| 沉淀完全时(c=1.0×10-5 mol·L-1)的pH | 8.7 | 4.7 | 3.2 | 9.0 |
利用上述表格数据,计算Ni(OH)2的Ksp=
您最近一年使用:0次
2 . 纳米铁粉和FeS都可以高效地去除被污染水体中的Cu2+、Hg2+等重金属离子,其原理是相同的(_______)
您最近一年使用:0次
3 . 根据实验操作和现象得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向某溶液中,先滴加氯水后,再滴加KSCN溶液,溶液变为红色 | 该溶液中一定含有Fe2+ |
| B | 向KMnO4溶液中通入SO2,溶液颜色褪去 | SO2具有漂白性 |
| C | 向2mL 0.1 mol/L的AgNO3溶液中滴入几滴0.1 mol/L的NaCl溶液,生成白色沉淀,再滴入几滴0.1 mol/L的NaI溶液,又生成黄色沉淀 | 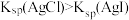 |
| D | 用醋酸浸泡有水垢的水壶,水垢会溶解消失 | 酸性:CH3COOH>H2CO3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 已知: 时,
时, 的溶度积分别为
的溶度积分别为 .下列说法正确的是
.下列说法正确的是
 时,
时, 的溶度积分别为
的溶度积分别为 .下列说法正确的是
.下列说法正确的是| A.可溶性硫化物可作为处理上述金属离子的沉淀剂 |
B.上述三种物质溶解度最小的是 |
C.在硫化铜悬浊液中滴加几滴 溶液,会生成 溶液,会生成 沉淀 沉淀 |
D.向含 均为 均为 的溶液中通入 的溶液中通入 气体,产生沉淀的顺序依次为 气体,产生沉淀的顺序依次为 |
您最近一年使用:0次
名校
5 . 下列事实不能用勒夏特列原理解释的是
A.溴水中存在Br2+H2O HBr+HBrO,当加入AgNO3溶液并静置后,溶液颜色变浅 HBr+HBrO,当加入AgNO3溶液并静置后,溶液颜色变浅 |
| B.合成氨反应中,为提高原料的转化率,可采用高温加热的条件 |
| C.棕红色NO2加压后颜色先变深后变浅 |
| D.向饱和NaCl溶液中通入HCl,有白色晶体析出 |
您最近一年使用:0次
解题方法
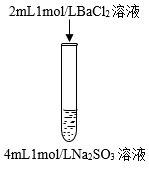
6 . 下列三组实验进行一段时间后,溶液中均有白色沉淀生成,下列结论正确的是
| 实验① | 实验② | 实验③ |
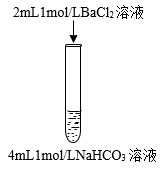 |  | 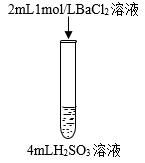 |
A.实验①中生成的沉淀是 |
B.实验①生成沉淀的离子方程式是: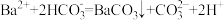 |
C.实验②沉淀中不可能含有 |
D.实验③生成沉淀的离子方程式是: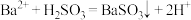 |
您最近一年使用:0次
名校
7 . 为分析某铜合金的成分,用足量酸将其完全溶解后,用 溶液调节
溶液调节 ,当
,当 时开始出现沉淀,分别在
时开始出现沉淀,分别在 为7.0、8.0时过滤沉淀,结合题图信息推断该合金中除铜外一定含有
为7.0、8.0时过滤沉淀,结合题图信息推断该合金中除铜外一定含有

 溶液调节
溶液调节 ,当
,当 时开始出现沉淀,分别在
时开始出现沉淀,分别在 为7.0、8.0时过滤沉淀,结合题图信息推断该合金中除铜外一定含有
为7.0、8.0时过滤沉淀,结合题图信息推断该合金中除铜外一定含有
A. 、 、 | B. 、 、 | C. 、 、 | D. 、 、 、 、 |
您最近一年使用:0次
2021-11-04更新
|
295次组卷
|
3卷引用:安徽师范大学附属中学2021-2022学年高三上学期11月考试化学试题
8 . 察尔汗盐湖是我国最大的钾肥生成基地,生产过程中会产生大量水氯镁石(MgCl2·6H2O)。为实现资源综合利用,以水氯镁石为原料制轻质氧化镁。工艺如下:

按要求回答问题:
(1)锂与镁元素性质相似,写出向Li2SO4溶液中滴加Na2CO3溶液的离子方程式为___________ 。
(2)在“水浸”时适当升温的目的是___________ 。
(3)“沉镁”采用的温度为90℃~95℃,温度不宜超过95℃的理由是___________ 。
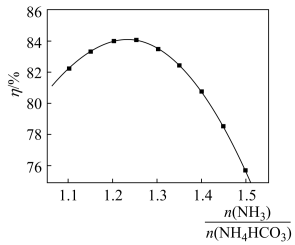
(4) 与沉镁效率(η)的关系如图所示,指出沉镁的
与沉镁效率(η)的关系如图所示,指出沉镁的 最佳范围为
最佳范围为___________ 。
(5)试说明“煅烧”后得到疏松多孔的MgO的原因是分解过程中产生大量的___________ 。
(6)“滤液”中的主要成分为___________ 。(填化学式)

按要求回答问题:
(1)锂与镁元素性质相似,写出向Li2SO4溶液中滴加Na2CO3溶液的离子方程式为
(2)在“水浸”时适当升温的目的是
(3)“沉镁”采用的温度为90℃~95℃,温度不宜超过95℃的理由是
(4)
 与沉镁效率(η)的关系如图所示,指出沉镁的
与沉镁效率(η)的关系如图所示,指出沉镁的 最佳范围为
最佳范围为
(5)试说明“煅烧”后得到疏松多孔的MgO的原因是分解过程中产生大量的
(6)“滤液”中的主要成分为
您最近一年使用:0次
9 . 化学与生产、生活密切相关。下列说法错误的是
| A.加入生石灰减少燃煤时排放的温室气体 |
| B.用Na2S除去工业废水中的Cu2+和Hg2+ |
| C.用纯碱溶液除油污,加热可提高去污能力 |
| D.用硫酸铁除去水中的悬浮物 |
您最近一年使用:0次
名校
10 . 天然铝土矿主要成分是Al2O3杂质主要为SiO2、Fe2O3、 MgO等,工业上用天然铝土矿生产铝的工艺流程如图:
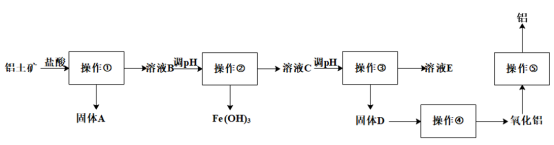
已知部分氢氧化物沉淀的pH如下表:
请回答下列问题:
(1)为了加快铝土矿和盐酸的反应速率,可以采取的措施为___________ (填一种即可)。
(2)固体A的主要成分是___________ (填化学式),溶液E中的金属离子主要为___________ (填化学式)。
(3)“溶液C”调节pH的范围为___________ 。
(4)为了验证“溶液C”中是否含有Fe3+,可取少量“溶液C”于试管中,向其中加入___________ 溶液(填试剂名称),溶液变成血红色,则证明“溶液C”中有Fe3+,其离子反应方程式为___________ 。
(5)生产中,若“溶液B”在调节pH时不当,造成同时生成了Fe(OH)3和Al(OH)3悬浊液,则其中c(A13+) :c(Fe3+) =___________
(6)操作⑤反应的化学方程式为___________ 。

已知部分氢氧化物沉淀的pH如下表:
| 沉淀物 | Fe( OH)3 | Al( OH)3 | Mg(OH)2 |
| 开始沉淀时的pH (离子初始浓度为0. 01mol·L-1) | 2.2 | 3.7 | 9. 6 |
| 完全沉淀时的pH (离子浓度<10-5mol·L-1) | 3.2 | 4.7 | 11.1 |
(1)为了加快铝土矿和盐酸的反应速率,可以采取的措施为
(2)固体A的主要成分是
(3)“溶液C”调节pH的范围为
(4)为了验证“溶液C”中是否含有Fe3+,可取少量“溶液C”于试管中,向其中加入
(5)生产中,若“溶液B”在调节pH时不当,造成同时生成了Fe(OH)3和Al(OH)3悬浊液,则其中c(A13+) :c(Fe3+) =
(6)操作⑤反应的化学方程式为
您最近一年使用:0次
2021-09-25更新
|
502次组卷
|
2卷引用:云南省师范大学附属中学2022届高三高考适应性月考卷(三)理科综合化学试题



