10-11高三上·福建福州·阶段练习
名校
1 . 下列叙述中,正确的是
| A.在船舶的外壳装上铜块可防止其发生电化学腐蚀 |
| B.MnO2、FeCl3和CuSO4都可加快H2O2的分解速率 |
| C.FeCl3溶液和Fe2(SO4)3溶液加热蒸干、灼烧都得到Fe2O3 |
| D.用惰性电极分别电解CuCl2溶液和MgCl2溶液分别得到单质Cu和Mg |
您最近一年使用:0次
11-12高二上·福建福州·期中
2 . 下列说法正确的是
| A.据能量守恒定律,反应物的总能量一定等于生成物的总能量 |
| B.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀 |
| C.在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
| D.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
您最近一年使用:0次
10-11高三上·山东济南·阶段练习
解题方法
3 . 钢铁在潮湿的空气中会形成原电池而被腐蚀,下列说法正确的是
| A.原电池的正极反应为:O2+2H2O+4e-→4OH- |
| B.原电池的负极反应为:Fe→Fe3++3e- |
| C.钢铁设备上连接铜块可以防止腐蚀 |
| D.钢铁与外加直流电源的正极相连可以防止腐蚀 |
您最近一年使用:0次
2016-12-09更新
|
1192次组卷
|
4卷引用:福建省福州第十五中学2022-2023学年高二上学期10月月考化学试题
福建省福州第十五中学2022-2023学年高二上学期10月月考化学试题(已下线)2011届山东省济南外国语学校高三上学期第三次质量检测化学试卷广东省广州市2021届高三年级阶段训练化学试题广东省肇庆市2020-2021学年高二上学期期末教学质量检测化学试题
10-11高二上·福建福州·期中
解题方法
4 . 钢铁工业是国家工业的基础。请回答钢铁冶炼、腐蚀、防护过程中的有关问题。
(1)下列哪个装置可防止铁棒被腐蚀_____________ 。
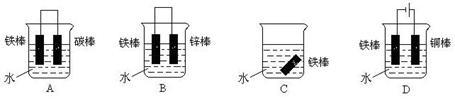
(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如右:
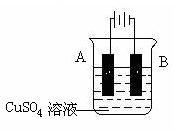
请回答:
①A电极对应的金属是______ (写元素名称),B电极的电极反应式是____________ 。
②若电镀前铁、铜两电极的质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为51.2 g,则电镀时电路中通过的电子物质的量为_______ 。
(1)下列哪个装置可防止铁棒被腐蚀

(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如右:

请回答:
①A电极对应的金属是
②若电镀前铁、铜两电极的质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为51.2 g,则电镀时电路中通过的电子物质的量为
您最近一年使用:0次
9-10高二下·福建福州·期末
5 . 保护地下钢管不受腐蚀,可使它与
| A.直流电源负极相连 | B.铜板相连 |
| C.碳棒相连 | D.直流电源正极相连 |
您最近一年使用:0次
2016-12-09更新
|
1012次组卷
|
3卷引用:2010年福建省福州八中高二第二学期期末考试化学试题



