1 . 利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产。下列说法中正确的是
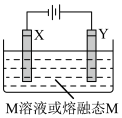

| A.电流由电源正极经导线流向Y极,再经电解质溶液或熔融态电解质流到X极,最后X极经导线流回电源负极 |
| B.铜电解精炼中,X是粗铜,Y是纯铜,M是CuSO4溶液 |
| C.X、Y均为石墨电极,电解熔融氯化铝制备金属铝 |
| D.外加电流的阴极保护法中,Y是待保护金属 |
您最近一年使用:0次
2023-12-11更新
|
94次组卷
|
2卷引用:福建省南平市高级中学2023-2024学年高二上学期期中考试化学试题
名校
2 . 下列关于金属腐蚀和保护的说法正确的是
| A.牺牲阳极保护法利用的是电解池原理 |
| B.金属的化学腐蚀的实质是M-ne-=Mn+,即氧化剂失去电子 |
| C.外加电流阴极保护法,被保护的金属与电源负极相连 |
| D.铜碳合金的铜像在酸雨中发生电化学腐蚀时,负极的电极反应式为O2+4e-+4H+=2H2O |
您最近一年使用:0次
2022-11-08更新
|
150次组卷
|
2卷引用:福建省南平市高级中学2022-2023学年高二上学期期中考试化学(选考)试题
3 . 对金属制品进行抗腐蚀处理可延长其使用寿命。
(1)以下为铝材表面处理的一种方法:

以铝材为阳极,在 溶液中电解,铝材表面形成氧化膜,阳极电极反应式为
溶液中电解,铝材表面形成氧化膜,阳极电极反应式为_______ 。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是_______ 。
(3)利用下图装置可以模拟铁的两种电化学防护的方法:若X为碳棒,为减缓铁的腐蚀,开关K应置于_______ (填“M”或“N”)处。若X为锌,开关K置于_______ (同上)处,该电化学保护法称为_______ 。

(1)以下为铝材表面处理的一种方法:

以铝材为阳极,在
 溶液中电解,铝材表面形成氧化膜,阳极电极反应式为
溶液中电解,铝材表面形成氧化膜,阳极电极反应式为(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是
(3)利用下图装置可以模拟铁的两种电化学防护的方法:若X为碳棒,为减缓铁的腐蚀,开关K应置于

您最近一年使用:0次
4 . 下列实验装置符合实验目的是
| 选项 | A | B |
| 目的 | 验证铁的析氢腐蚀 | 构成原电池 |
| 装置 |  |  |
| 选项 | C | D |
| 目的 | 在铁制品上镀铜 | 减缓锌的锈蚀 |
| 装置 | 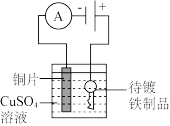 | 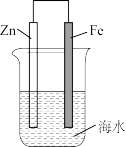 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . “孔蚀”是一种集中于金属表面极小范围并能深入到金属内部的电化学腐蚀。某铁合金表面钝化膜破损后,发生“孔蚀”的电化学腐蚀过程如题图所示。下列有关说法正确的是
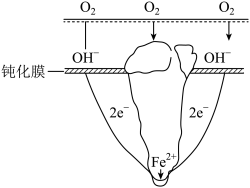

| A.负极反应:Fe-3e-=Fe3+ |
| B.氧化0.2 mol Fe,需消耗3.36 LO2 |
| C.铁合金腐蚀的最终产物为Fe(OH)3 |
| D.为防止孔蚀发生可以将外接电源负极与金属相连 |
您最近一年使用:0次
2022-09-06更新
|
733次组卷
|
4卷引用:福建省南平市建阳第二中学2022-2023学年高二上学期第一次月考化学试题
福建省南平市建阳第二中学2022-2023学年高二上学期第一次月考化学试题江苏省徐州市2021--2022学年高二上学期期末抽测化学试题(已下线)4.3 金属的腐蚀与防护-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)江苏省苏州市吴江中学2023-2024学年高二上学期10月月考化学试题
6 . 化学与生活生产密切相关。下列做法错误的是
| A.生活中可用热纯碱溶液去除油污 |
| B.铵态氮肥和草木灰(含K2CO3)混合施用 |
| C.“84”消毒液不能与洁厕剂混合使用 |
| D.河道中的钢铁闸门与外加直流电源负极相连保护其不受腐蚀 |
您最近一年使用:0次
7 . 完成下列各小题
(1)已知在25℃、101kPa时,4g H2完全燃烧生成液态水,放出571.6kJ的热量,写出表示H2摩尔燃烧焓的热化学方程式:______________________ 。
(2)金属腐蚀一般可分为化学腐蚀和电化学腐蚀。炒过菜的铁锅未及时清洗容易发生___________ 腐蚀而生锈。请写出铁锅生锈过程的正极反应式:_______________________ 。
(3)图中甲池的总反应式为N2H4+O2=N2+2H2O。
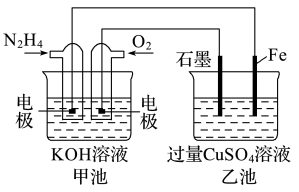
①甲池中负极上发生的是____________________ (填“氧化反应”或“还原反应”),乙池中SO 向
向_________ 移动(填“左”或“右”)。
②乙池中电解反应的离子方程为_________________________ 。
③要使乙池恢复到电解前的状态,应向溶液中加入_____________ (填化学式)。
(1)已知在25℃、101kPa时,4g H2完全燃烧生成液态水,放出571.6kJ的热量,写出表示H2摩尔燃烧焓的热化学方程式:
(2)金属腐蚀一般可分为化学腐蚀和电化学腐蚀。炒过菜的铁锅未及时清洗容易发生
(3)图中甲池的总反应式为N2H4+O2=N2+2H2O。

①甲池中负极上发生的是
 向
向②乙池中电解反应的离子方程为
③要使乙池恢复到电解前的状态,应向溶液中加入
您最近一年使用:0次
名校
8 . 自嗨锅的发热包主要成分有:硅藻土、铁粉、铝粉、焦炭粉、食盐、生石灰,使用时使发热包里面的物质与水接触即可。下列说法错误的是
| A.铁粉发生析氢腐蚀,缓慢放出热量,延长放热时间 |
| B.硅藻土可增大反应物的接触面积 |
| C.过程中形成微小原电池,正极反应为:O2+2H2O+4e-=4OH- |
| D.使用后的发热包含有熟石灰属于有害垃圾 |
您最近一年使用:0次
2021-11-08更新
|
123次组卷
|
3卷引用:福建省南平市高级中学2021-2022学年高二上学期期中考试化学(选考)试题
名校
解题方法
9 . 化学与人们的生活息息相关,下列说法错误的是
| A.农村推广风力发电、光伏发电有利于“碳达峰、碳中和” |
| B.可将港珠澳大桥钢骨架与外加直流电源的正极相连以保护它不受腐蚀 |
| C.升高温度,可使活化分子的百分数增大,反应速率加快 |
| D.合成氨工业采用700K是因为该温度下速率较快且催化剂活性大 |
您最近一年使用:0次
2021-11-08更新
|
83次组卷
|
2卷引用:福建省南平市高级中学2021-2022学年高二上学期期中考试化学(选考)试题
名校
解题方法
10 . 下列与金属腐蚀有关的说法正确的是
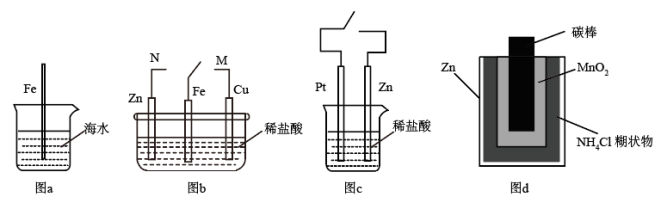

| A.图a中,插入海水中的铁棒(含碳量为10.8%)越靠近水面发生电化学腐蚀就越严重 |
| B.图b中,开关由N改置于M时,金属铁的腐蚀速率减小 |
| C.图c中,接通开关时Zn腐蚀速率减小,Pt电极上放出气体的速率增大 |
| D.图d中,Zn-MnO2酸性干电池自放电反应主要是由MnO2的催化作用引起的 |
您最近一年使用:0次
2021-04-30更新
|
186次组卷
|
3卷引用:福建省南平市浦城县2022-2023学年高二上学期11月期中化学试题



