解题方法
1 . 下列实验能达到实验目的的是
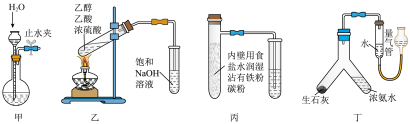
| A.图甲:检查装置的气密性 | B.图乙:实验室制取乙酸乙酯 |
| C.图丙:研究铁的析氢腐蚀 | D.图丁: 测量产生 N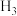 的体积 的体积 |
您最近一年使用:0次
名校
解题方法
2 . 下列离子方程式正确的是
A.碱性锌锰电池的负极反应: |
B. 通入 通入 溶液无现象,再通入 溶液无现象,再通入 后产生白色沉淀 后产生白色沉淀 |
C.往 溶液滴加少量的氨水: 溶液滴加少量的氨水: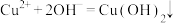 |
D.钢铁在潮湿的空气腐蚀:负极反应为: |
您最近一年使用:0次
3 . 利用 溶液可以进行多种电化学实验或医药生产,完成下列题目。
溶液可以进行多种电化学实验或医药生产,完成下列题目。
I.某同学在实验室中组装下列实验装置并进行实验探究。
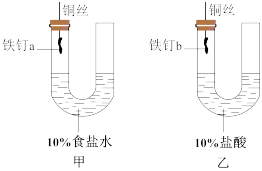
(1)该同学观察到甲装置中的左边液面___________ (填“升高”或“降低”),装置中铁主要发生了___________ (填“析氢”或“吸氧”)腐蚀,该腐蚀过程中正极的电极反应式为___________ 。
(2)反应过程中观察到乙装置中左边液面降低,右边液面升高,这是因为装置铁也发生原电池反应,发生原电池反应方程式为___________ 。
Ⅱ.如图所示为实验室模拟工业电解饱和食盐水装置图。
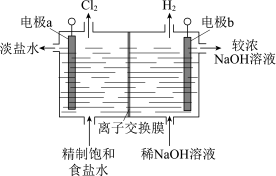
(3)电解饱和食盐水的离子方程式___________  是在
是在___________ (阴或阳)极产生。
(4)电极 接电源的
接电源的___________ (填“正”或“负”)极。
(5)离子交换膜主要允许___________ 离子通过。
(6)当两极产生的气体质量和为 时,电子转移的数目为
时,电子转移的数目为___________ 。
 溶液可以进行多种电化学实验或医药生产,完成下列题目。
溶液可以进行多种电化学实验或医药生产,完成下列题目。I.某同学在实验室中组装下列实验装置并进行实验探究。

(1)该同学观察到甲装置中的左边液面
(2)反应过程中观察到乙装置中左边液面降低,右边液面升高,这是因为装置铁也发生原电池反应,发生原电池反应方程式为
Ⅱ.如图所示为实验室模拟工业电解饱和食盐水装置图。

(3)电解饱和食盐水的离子方程式
 是在
是在(4)电极
 接电源的
接电源的(5)离子交换膜主要允许
(6)当两极产生的气体质量和为
 时,电子转移的数目为
时,电子转移的数目为
您最近一年使用:0次
名校
4 . 下列有关化学用语表示正确的是
A. 水解: 水解: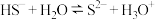 |
B. 电离: 电离: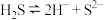 |
C. 的沉淀溶解平衡: 的沉淀溶解平衡: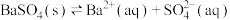 |
D.钢铁发生电化学腐蚀的负极反应式: |
您最近一年使用:0次
5 . 下列实验设计或所选装置合理的是
 | 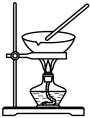 |  |  |
A.通过注射器活塞右移,验证 与 与 反应放热 反应放热 | B.由 制无水 制无水 固体 固体 | C.电解 溶液,制备金属 溶液,制备金属 | D.模拟钢铁的吸氧腐蚀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 下列说法正确的是
| A.华为自主研发的Mate60系列5G手机,充电时负极发生还原反应 |
| B.钢铁水闸与电源负极相连接可减缓其腐蚀,该法称为牺牲阳极的阴极保护法 |
| C.电解精炼铜的阳极泥中可回收锌、金和银等贵金属 |
| D.电镀过程中,待镀金属与电源正极相连 |
您最近一年使用:0次
7 . 化学能与电能的相互转化在生产和生活中有着广泛的应用。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。
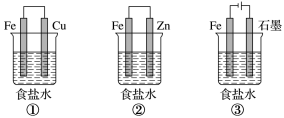
在相同条件下,三组装置中铁电极腐蚀最快的是___________ (填装置序号);装置③中 电极的电极反应式为
电极的电极反应式为___________ 。
(2)温室气体 转化为甲酸或CO,可实现资源化利用。电还原
转化为甲酸或CO,可实现资源化利用。电还原 制甲酸的装置如图所示。
制甲酸的装置如图所示。

①HCOOH在___________ 极产生,其电极反应式为___________ 。
② 的移动方向是
的移动方向是___________ (填“向左”或“向右”)。
③理论上,电路中每转移 电子,生成标准状况下的
电子,生成标准状况下的 体积为
体积为___________ L。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

在相同条件下,三组装置中铁电极腐蚀最快的是
 电极的电极反应式为
电极的电极反应式为(2)温室气体
 转化为甲酸或CO,可实现资源化利用。电还原
转化为甲酸或CO,可实现资源化利用。电还原 制甲酸的装置如图所示。
制甲酸的装置如图所示。
①HCOOH在
②
 的移动方向是
的移动方向是③理论上,电路中每转移
 电子,生成标准状况下的
电子,生成标准状况下的 体积为
体积为
您最近一年使用:0次
名校
解题方法
8 . 化学与社会、生活、生产密切相关,下列有关说法错误的是
| A.洗涤油污常用热的Na2CO3溶液,这是利用了盐类水解的原理 |
| B.航天员所穿航天服的主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它是一种新型无机非金属材料 |
| C.“闽鹭”是我国制造的第四艘LNG船,船底镶嵌锌块,锌作负极,以防船体被腐蚀 |
| D.高纯硅是制备光导纤维的原料 |
您最近一年使用:0次
名校
9 . 电化学在实际生活生产中十分常见,如金属的腐蚀及防护,利用电化学合成物质、处理废水等等。
(1)按图1进行实验,测得锥形瓶内气压和空气中氧气的体积分数随时间变化如图2所示,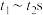 之间主要发生
之间主要发生___________ (填“吸氧”或“析氢”)腐蚀,其正极反应式为___________ 。
(2)金属阳极钝化是一种电化学防护方法。将 作阳极置于一定浓度的
作阳极置于一定浓度的 溶液中,一定条件下,
溶液中,一定条件下, 钝化形成致密
钝化形成致密 氧化膜,试写出该阳极的电极反应
氧化膜,试写出该阳极的电极反应___________ 。
(3)氯碱工业能耗大,通过如图改进的设计可大幅度降低能耗。
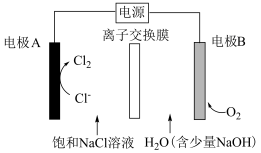
①离子交换膜应选择___________ 离子交换膜(填“阴”或“阳”)
②反应的总化学方程式为___________ 。
③当电路中通过 电子时,右侧溶液质量
电子时,右侧溶液质量______ (填“增加”或“减少”)_____  。
。
(1)按图1进行实验,测得锥形瓶内气压和空气中氧气的体积分数随时间变化如图2所示,
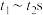 之间主要发生
之间主要发生
(2)金属阳极钝化是一种电化学防护方法。将
 作阳极置于一定浓度的
作阳极置于一定浓度的 溶液中,一定条件下,
溶液中,一定条件下, 钝化形成致密
钝化形成致密 氧化膜,试写出该阳极的电极反应
氧化膜,试写出该阳极的电极反应(3)氯碱工业能耗大,通过如图改进的设计可大幅度降低能耗。

①离子交换膜应选择
②反应的总化学方程式为
③当电路中通过
 电子时,右侧溶液质量
电子时,右侧溶液质量 。
。
您最近一年使用:0次
名校
解题方法
10 . 回答下列问题
(1)某公司开发了一种以甲醇为原料,以KOH为电解质的用于手机可充电的高效燃料电池,充一次电可连续使用一个月。其中B电极的电极材料为碳,如图是一个电化学过程的示意图。请填空:
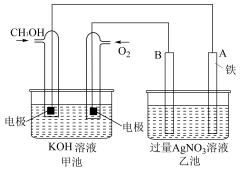
①放电时,甲醇在___________ (填“正”或“负”)极发生反应,正极的电极反应为___________ 。
②工作时,B极的电极反应式为___________ ,A极的电极反应式为___________ 。
(2)某同学设计了一种用电解法制取Fe(OH)2的实验装置(如图所示)通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法不正确的是___________(填序号)。

(3)如图所示将铁棒和石墨棒插入盛有饱和NaCl溶液的 型管中。
型管中。
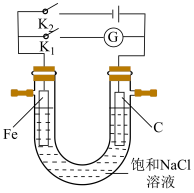
①K1闭合,铁电极的反应为___________ 。
②K2闭合,铁棒不会被腐蚀,属于___________ 保护法。
(1)某公司开发了一种以甲醇为原料,以KOH为电解质的用于手机可充电的高效燃料电池,充一次电可连续使用一个月。其中B电极的电极材料为碳,如图是一个电化学过程的示意图。请填空:

①放电时,甲醇在
②工作时,B极的电极反应式为
(2)某同学设计了一种用电解法制取Fe(OH)2的实验装置(如图所示)通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法不正确的是___________(填序号)。

A. 为电源正极, 为电源正极, 为电源负极 为电源负极 | B.可以用NaCl溶液作为电解质溶液 |
| C.A、B两端都必须用铁作电极 | D.阴极发生的反应为2H2O+2e-=2OH-+H2↑ |
(3)如图所示将铁棒和石墨棒插入盛有饱和NaCl溶液的
 型管中。
型管中。
①K1闭合,铁电极的反应为
②K2闭合,铁棒不会被腐蚀,属于
您最近一年使用:0次



