名校
1 . 下列电极反应式与出现的环境相匹配的是
| 电极反应式 | 出现的环境 | |
| A | C2H5OH-12e-+3H2O=CO2↑+12H+ | 碱性环境下乙醇燃料电池的负极反应 |
| B | O2+2H2O-4e-=4OH- | 钢铁吸氧腐蚀的正极反应 |
| C | CO-2e-+CO =2CO2 =2CO2 | 熔融碳酸盐环境下的CO燃料电池负极 |
| D | 2H++2e-=H2↑ | 用惰性电极电解H2SO4溶液的阳极反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
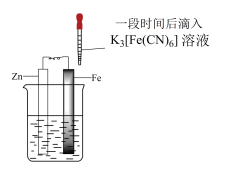
2 . 实验小组研究金属电化学腐蚀,实验如下:
实验Ⅰ

5min时的现象:铁钉表面及周边未见明显变化。
25min时的现象:铁钉周边零星、随机出现极少量红色和蓝色区域,有少量红棕色铁锈生成。
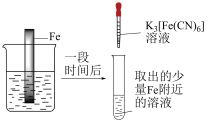
实验Ⅱ
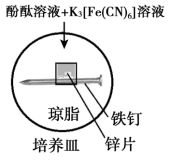
5min时的现象:铁钉周边出现红色区域,未见蓝色出现,锌片周边未见明显变化。
25min时的现象:铁钉周边红色加深,区域变大,未见蓝色出现,锌片周边未见明显变化。
下列说法不正确的是
实验Ⅰ

5min时的现象:铁钉表面及周边未见明显变化。
25min时的现象:铁钉周边零星、随机出现极少量红色和蓝色区域,有少量红棕色铁锈生成。
实验Ⅱ

5min时的现象:铁钉周边出现红色区域,未见蓝色出现,锌片周边未见明显变化。
25min时的现象:铁钉周边红色加深,区域变大,未见蓝色出现,锌片周边未见明显变化。
下列说法不正确的是
| A.实验Ⅱ中Zn保护了Fe,使铁的腐蚀速率比实验Ⅰ慢 |
B.实验Ⅱ中正极的电极反应式: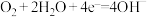 |
C.实验Ⅰ的现象说明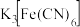 溶液与Fe反应生成了 溶液与Fe反应生成了 |
| D.若将Zn片换成Cu片,推测Cu片周边会出现红色,铁钉周边会出现蓝色 |
您最近一年使用:0次
2022-09-04更新
|
1372次组卷
|
13卷引用:北京市第十二中学2021-2022学年高一下学期6月月考化学试题
北京市第十二中学2021-2022学年高一下学期6月月考化学试题北京十二中2021-2022学年高一下学期六月月考(等级考)化学试题(已下线)【教材实验热点】17 金属的腐蚀与防护第四章 综合拔高练北京市海淀实验中学2022-2023学年高三上学期10月学科展示化学试题北京市北京师范大学燕化附中2022-2023学年高二上学期10月月考化学试题福建省莆田第二十四中学2021-2022学年高二下学期开学摸底考试化学(2卷)试题山东省枣庄市第一中学2022-2023学年高二上学期期末达标化学试题北京市朝阳区2021届高三上学期期末考试化学试题(已下线)2021年高考化学押题预测卷(辽宁卷)(03)(已下线)北京市第四中学2021-2022学年高二上学期期中考试化学试题福建省龙岩市连城县第一中学2023-2024学年高二上学期8月月考化学试题山东省滨州市2023-2024学年高三上学期11月期中考试化学试题
名校
解题方法
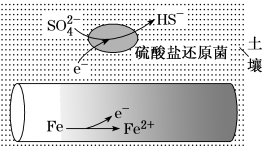
3 . 潮湿土壤中的铁管道在硫酸盐还原菌(最佳生存环境 为7~8)作用下,能被硫酸根腐蚀,其电化学腐蚀原理如图所示。下列说法错误的是
为7~8)作用下,能被硫酸根腐蚀,其电化学腐蚀原理如图所示。下列说法错误的是
 为7~8)作用下,能被硫酸根腐蚀,其电化学腐蚀原理如图所示。下列说法错误的是
为7~8)作用下,能被硫酸根腐蚀,其电化学腐蚀原理如图所示。下列说法错误的是
| A.铁作负极发生氧化反应 |
B.正极反应为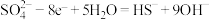 |
| C.将管道连接废锌块可防止腐蚀 |
| D.酸性环境下铁管道不易被硫酸根腐蚀 |
您最近一年使用:0次
2022-07-07更新
|
800次组卷
|
5卷引用:山东省潍坊2021-2022学年高一下学期期末测试化学试题
解题方法
4 . 工业废水中的六价铬[Cr(VI)]常采用还原沉淀法、离子交换法和微生物法等方法进行处理。
(1)室温下,含Cr(VI)的微粒在水溶液中存在如下平衡:
H2CrO4⇌H++HCrO ΔH1
ΔH1
HCrO ⇌H++CrO
⇌H++CrO ΔH2
ΔH2
2HCrO ⇌
⇌ +H2O ΔH3
+H2O ΔH3
室温下,反应2CrO +2H+⇌
+2H+⇌ +H2O的ΔH=
+H2O的ΔH=_______ (用含ΔH1、ΔH2或ΔH3的代数式表示)。
(2)还原沉淀法:使用Na2SO3将Cr(VI)还原为Cr3+,再将Cr3+转化为沉淀除去。
①酸性条件下Cr(VI)具有很强的氧化能力, 将
将 还原为Cr3+的离子方程式为
还原为Cr3+的离子方程式为_______ 。
②其他条件相同,用Na2SO3处理不同初始pH的含Cr(VI)废水相同时间,当pH<2时,Cr(VI)的去除率随pH降低而降低的原因是_______ 。
(3)微生物法:
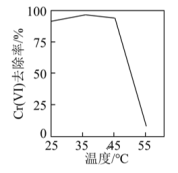
①用硫酸盐还原菌(SRB)处理含Cr(VI)废水时,Cr(VI)去除率随温度的变化如图所示。55℃时,Cr(VI)的去除率很低的原因是_______ 。
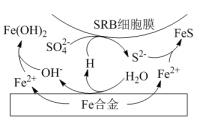
②水体中,Fe合金在SRB存在条件下腐蚀的机理如图所示。Fe腐蚀后生成FeS的过程可描述为:Fe失去电子转化为Fe2+,_______ 。
(4)离子交换法:用强碱性离子交换树脂(ROH)与 和HCrO
和HCrO 等发生离子交换,交换过程中发生如下反应:
等发生离子交换,交换过程中发生如下反应:
ROH(s)+HCrO (aq)⇌ RHCrO4(s)+OH-(aq)
(aq)⇌ RHCrO4(s)+OH-(aq)
2ROH(s)+ (aq)⇌ R2CrO4(s)+2OH-(aq)
(aq)⇌ R2CrO4(s)+2OH-(aq)
其他条件相同,当pH>4时,Cr(VI)去除率随pH升高而下降的原因是_______ 。
(1)室温下,含Cr(VI)的微粒在水溶液中存在如下平衡:
H2CrO4⇌H++HCrO
 ΔH1
ΔH1HCrO
 ⇌H++CrO
⇌H++CrO ΔH2
ΔH22HCrO
 ⇌
⇌ +H2O ΔH3
+H2O ΔH3室温下,反应2CrO
 +2H+⇌
+2H+⇌ +H2O的ΔH=
+H2O的ΔH=(2)还原沉淀法:使用Na2SO3将Cr(VI)还原为Cr3+,再将Cr3+转化为沉淀除去。
①酸性条件下Cr(VI)具有很强的氧化能力,
 将
将 还原为Cr3+的离子方程式为
还原为Cr3+的离子方程式为②其他条件相同,用Na2SO3处理不同初始pH的含Cr(VI)废水相同时间,当pH<2时,Cr(VI)的去除率随pH降低而降低的原因是
(3)微生物法:
①用硫酸盐还原菌(SRB)处理含Cr(VI)废水时,Cr(VI)去除率随温度的变化如图所示。55℃时,Cr(VI)的去除率很低的原因是

②水体中,Fe合金在SRB存在条件下腐蚀的机理如图所示。Fe腐蚀后生成FeS的过程可描述为:Fe失去电子转化为Fe2+,

(4)离子交换法:用强碱性离子交换树脂(ROH)与
 和HCrO
和HCrO 等发生离子交换,交换过程中发生如下反应:
等发生离子交换,交换过程中发生如下反应:ROH(s)+HCrO
 (aq)⇌ RHCrO4(s)+OH-(aq)
(aq)⇌ RHCrO4(s)+OH-(aq)2ROH(s)+
 (aq)⇌ R2CrO4(s)+2OH-(aq)
(aq)⇌ R2CrO4(s)+2OH-(aq)其他条件相同,当pH>4时,Cr(VI)去除率随pH升高而下降的原因是
您最近一年使用:0次
名校
5 . 用如图所示装置及试剂进行铁的电化学腐蚀实验探究,测定具支锥形瓶中压强随时间变化关系以及溶解氧随时间变化关系的曲线如下。下列说法不正确的是
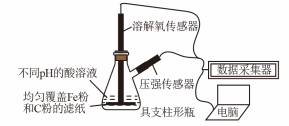
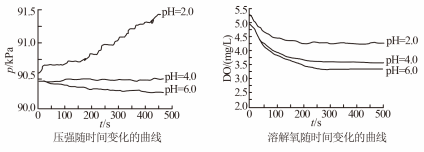


| A.压强增大主要是因为产生了H2 |
| B.整个过程中,负极电极反应式均为:Fe–2e- = Fe2+ |
| C.pH= 4.0时,体系为弱酸性,同时发生析氢腐蚀和吸氧腐蚀 |
| D.pH= 2.0时,体系为强酸性,正极只发生析氢腐蚀,电极方程式为:2H+ + 2e- = H2↑ |
您最近一年使用:0次
2021-11-26更新
|
1446次组卷
|
6卷引用:重庆南开中学2021-2022学年高一下学期4月第一次月考化学试题
重庆南开中学2021-2022学年高一下学期4月第一次月考化学试题湖北省武汉市华中师范大学第一附属中学2021-2022学年高一下学期期中考试化学试题福建省厦门市厦门双十中学2021-2022学年上学期期中考试化学试题(已下线)4.3 金属的腐蚀和防护-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)周末培优4 新型电池的电化学原理问题-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)第四单元培优练-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)
6 . 验证牺牲阳极的阴极保护法,实验如下(烧杯内均为经过酸化的3%NaCl溶液)。
下列说法不正确 的是
| ① | ② | ③ |
|
|
|
| 在Fe表面生成蓝色沉淀 | 试管内无明显变化 | 试管内生成蓝色沉淀 |
| A.对比②③,可以判定Zn保护了Fe |
| B.对比①②,K3[Fe(CN)6]可能将Fe氧化 |
| C.验证Zn保护Fe时不能用①的方法 |
| D.将Zn换成Cu,用①的方法可判断Fe比Cu活泼 |
您最近一年使用:0次
2018-06-09更新
|
11500次组卷
|
78卷引用:山东省泰安市泰安一中2021-2022学年高一下学期6月学情诊断化学试题
山东省泰安市泰安一中2021-2022学年高一下学期6月学情诊断化学试题重庆市西南大学附属中学校2021-2022学年高一广延班下学期期末考试化学试题安徽省阜阳市第三中学竞培中心2017-2018学年高一年级第二学期第三次调研考试化学试题浙江省东阳中学2018-2019学年高一下学期期中考试化学试题河南省中原名校联盟2021-2022学年高二上学期第三次适应性联考化学试题广东省东莞市七校2021-2022学年高二下学期期中联考化学试题(已下线)考点20 金属的腐蚀与防护-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点18 原电池 化学电源-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第17讲 电解池 金属的腐蚀与防护 (练)-2023年高考化学一轮复习讲练测(新教材新高考)北京市清华大学附属中学2022-2023学年高二上学期期中考试化学试题山东省枣庄市第三中学(实验班)2022-2023学年高二11月线上测试化学试题2018年全国普通高等学校招生统一考试化学(北京卷)(已下线)2018年高考题及模拟题汇编 专题11 化学实验基础【全国百强校】河南省信阳市高级中学2018-2019学年高二上学期10月月考化学试题1(已下线)2019高考备考二轮复习精品资料-专题10 电化学及其应用(教学案)四川省攀枝花市2018-2019学年高二下学期期末调研检测化学试题四川省树德中学2020届高三11月月考化学试题(已下线)【南昌新东方】江西省南昌市第三中学2019-2020学年度高三上学期11月月考化学试题四川省成都市龙泉第二中学2019-2020学年高三上学期1月月考理科综合化学试题(已下线)专题十 化学能与电能(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训江西省宜春市宜丰县宜丰中学2019-2020学年高二下学期开学考试化学试题(已下线)专题6.3 电解池 金属的腐蚀与防护(练)——2020年高考化学一轮复习讲练测江西省宜春市2020届高三5月模拟理科综合-化学试题(已下线)专题6.3 电解池 金属的腐蚀与防护(讲)——2020年高考化学一轮复习讲练测北京市通州区2019-2020学年高二下学期期末考试化学试题河南省驻马店市2018-2019学年高二上学期期末考试化学试题鲁科版(2019)选择性必修1 第1章 化学反应与能量转化 第4节 金属的腐蚀与防护高中必刷题高二选择性必修1第四章 化学反应与电能 第四章素养检测河南省漯河市临颍县南街高级中学2020届高三阶段性测试化学试题人教版(2019)高二选择性必修第一册 第四章 化学反应与电能 第三节 金属的腐蚀与防护1(已下线)第21讲 电解池 金属的电化学腐蚀与防护 (精讲)——2021年高考化学一轮复习讲练测人教版(2019)高二化学选择性必修1第四章 化学反应与电能 过高考 3年真题强化闯关(已下线)第四章 化学反应与电能(B卷能力提高篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)河南省郑州市郑州中学2020-2021学年高二上学期期中考试化学试题(已下线)【浙江新东方】【2020】【高二上】【期中】【HD-LP406】【化学】河南省鹤壁市高级中学2020-2021学年高二上学期尖子生联赛调研化学试题(已下线)小题必刷26 电解池原理及其应用——2021年高考化学一轮复习小题必刷(通用版本)福建省平和县第一中学2021届高三年上学期第二次月考化学试题江苏省泰州中学2020-2021学年高二上学期期中考试化学试题(已下线)练习16 金属的电化学腐蚀-2020-2021学年【补习教材·寒假作业】高二化学(人教版)辽宁省丹东市2020-2021学年高二上学期期末考试化学试题甘肃省陇南市徽县第二中学2020-2021学年高二上学期期末考试化学试题四川省三台中学实验学校2020-2021学年高二下学期开学考试理综化学试题陕西省咸阳市2021届高考五月检测三模理综化学试题(已下线)课时34 金属的腐蚀与防护-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点22 电解池 金属的腐蚀与防护-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点21 原电池 化学电源-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点21 原电池 化学电源-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点22 电解池 金属的腐蚀与防护-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第17讲 电解池 金属的腐蚀与防护(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)江苏省泰州中学2021-2022学年高二上学期第一次月度检测化学试题山东省实验中学2022届高三第一次诊断考试化学试题河南省南阳市第一中学校2021-2022学年高二上学期第二次月考化学试题福建省厦门市厦门双十中学2021-2022学年上学期期中考试化学试题山东省泰安第二中学2021-2022学年高二上学期期中考试化学试题(已下线)4.3 金属的腐蚀和防护-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)河南省重点高中2021-2022学年高二上学期阶段性调研联考二化学试题(已下线)2020年江苏卷化学高考真题变式题11-15山东省济南外国语学校2021-2022学年高三上学期11月月考化学试题黑龙江省牡丹江市第三高级中学2021-2022学年高三上学期第四次月考化学试题北京师范大学附属中学2021-2022学年高二上学期期末考试化学试题内蒙古包头市第四中学2021-2022学年高二上学期期中考试化学试题河南省洛阳市2022-2023学年高二上学期期末考试化学试题(已下线)题型107 电化学原理在金属防腐蚀中的应用辽宁省凌源市高中2022-2023学年高二下学期3月联考化学试题(已下线)专题六 金属的化学腐蚀与防护(练习)天津市第一中学2022-2023学年高二上学期期末考试化学试题作业(二十六) 金属的腐蚀与防护云南省普洱市第一中学2022-2023学年高二下学期期末考试化学试题第四章 化学反应与电能 第三节 金属的腐蚀与防护山东省泰安新泰市第一中学(实验部)2023-2024学年高二上学期第一次质量检测化学试题北京市第一○一中学2023-2024学年高二上学期12月统练四化学试题北京市第一○一中学2023-2024学年高二上学期12月统练四化学试题(已下线)不定项选择题福建省泉州市泉港区第一中学2023-2024学年高二上学期12月月考化学试题北京师范大学第二附属中学2023-2024学年高三上学期期中考试化学试题山东省百师联盟2023-2024学年高二上学期12月大联考化学试题 陕西省安康市2023-2024学年高二上学期12月联考化学试题