1 . 下列实验装置(部分夹持装置已略去)能达到对应实验目的是
| A | B | C | D | |
| 实验目的 | 测定锌与稀硫酸反应速率 | 测定中和反应的反应热 | 比较 AgCl和 Ag2S 溶度积大小 | 探究铁的析氢腐蚀 |
| 实验装置 | 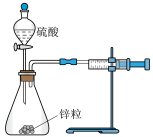 | 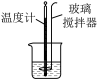 | 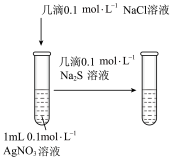 | 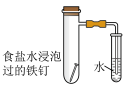 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-01-03更新
|
127次组卷
|
11卷引用:北京市西城区2021—2022学年高二上学期期末化学试题
北京市西城区2021—2022学年高二上学期期末化学试题吉林省德惠市实验中学2022-2023学年高二上学期第三次月考化学试题广东省广州市协和中学等3校2022-2023学年高二上学期(12月)期末考试化学试题北京师范大学第二附属中学2023-2024学年高二上学期期中考试化学试题北京师范大学附属实验中学顺义学校2023-2024学年高二上学期12月月考化学试题吉林省长春市实验中学2022-2023学年高二上学期期末考试化学试题湖南省宁乡市2022-2023学年高二上学期期末考试化学试题 重庆市杨家坪中学2023-2024学年高二上学期第三次月考化学试题天津市南开区2023-2024学年高二上学期期末测试化学试题四川省射洪中学校2023-2024学年高二上学期第三次月考化学试题天津市重点校2023-2024学年高二上学期期末考试化学试题
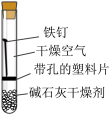
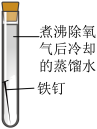
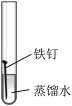
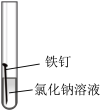
2 . 某小组同学对不同条件下铁钉的锈蚀进行了实验。
(1)一周后观察,铁钉被腐蚀程度最大的是___________ (填实验序号)。
(2)实验小组将实验④中氯化钠溶液分别替换为pH=2和pH=4的盐酸溶液。在密闭容器中,分别用压强传感器记录实验过程中的压强变化,如图所示。___________ (填字母,下同)。
a.两容器中负极反应均为Fe-2e⁻=Fe2+
b.曲线a记录的是pH=2的盐酸中压强的变化
c.在弱酸性溶液中,铁钉能发生吸氧腐蚀
d.曲线b记录的容器中正极反应是O2+4e⁻+2H2O=4OH⁻
(3)电化学原理在保护海水中钢闸门中有广泛应用。______ 。
a.牺牲阳极法 b.外加电流法
②为了减缓海水对钢闸门A的腐蚀,图1中材料B可以选择______ 。
a.碳棒 b.锌板 c.铜板
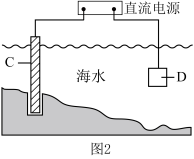
③图2中,钢闸门C应连接直流电源的___________ (填“正”或“负”)极。
| 序号 | ① | ② | ③ | ④ |
| 实验 |
|
|
|
|
(1)一周后观察,铁钉被腐蚀程度最大的是
(2)实验小组将实验④中氯化钠溶液分别替换为pH=2和pH=4的盐酸溶液。在密闭容器中,分别用压强传感器记录实验过程中的压强变化,如图所示。

a.两容器中负极反应均为Fe-2e⁻=Fe2+
b.曲线a记录的是pH=2的盐酸中压强的变化
c.在弱酸性溶液中,铁钉能发生吸氧腐蚀
d.曲线b记录的容器中正极反应是O2+4e⁻+2H2O=4OH⁻
(3)电化学原理在保护海水中钢闸门中有广泛应用。
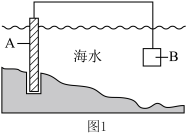
a.牺牲阳极法 b.外加电流法
②为了减缓海水对钢闸门A的腐蚀,图1中材料B可以选择
a.碳棒 b.锌板 c.铜板
③图2中,钢闸门C应连接直流电源的
您最近半年使用:0次
2023-12-25更新
|
159次组卷
|
2卷引用:北京市第十五中学2022-2023学年高二上学期期中考试 化学试题
名校
解题方法
3 . 化学与社会生活密切相关,下列说法正确的是
| A.加“洁厕灵”增强“84消毒液”消毒效果 |
| B.补铁口服液不能与维生素C一起服用 |
| C.马口铁(镀锡铁皮)比白铁皮(镀锌铁皮)破损铁更容易腐蚀 |
| D.“汽车限行”措施不会减轻碳排放 |
您最近半年使用:0次
名校
4 . 用滴有酚酞的氯化钠溶液湿润的滤纸分别做甲、乙两个实验,如图所示,下列判断正确的是
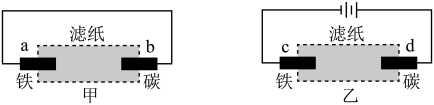

| A.b极附近有气泡冒出 | B.d极附近先出现红色 |
| C.a、c极上都发生氧化反应 | D.甲中铁棒比乙中铁棒更易腐蚀 |
您最近半年使用:0次
2023-09-23更新
|
181次组卷
|
3卷引用:北京市八一学校2022-2023学年高二上学期期中考试化学试题
5 . 下列铁制品防护的装置或方法中,不正确 的是
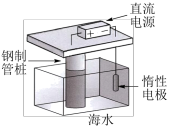 | 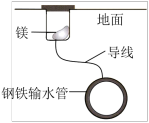 | 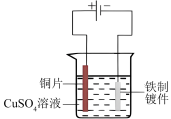 |
不锈钢 |
| A | B | C | D |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
6 . 验证牺牲阳极法,实验如下(烧杯内均为经过酸化的3%NaCl溶液)。
下列说法不正确 的是
| ① | ② | ③ |
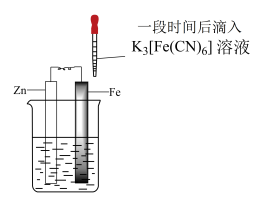 | 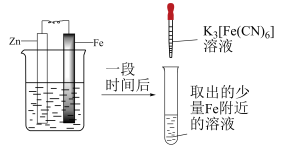 | 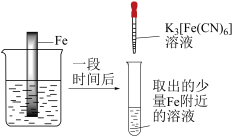 |
| 在Fe表面生成蓝色沉淀 | 试管内无明显变化 | 试管内生成蓝色沉淀 |
A.对比①②, 可能将Fe氧化 可能将Fe氧化 |
| B.对比②③,可以判定Zn保护了Fe |
C.用 酸性溶液代替 酸性溶液代替 溶液,也可验证牺牲阳极法 溶液,也可验证牺牲阳极法 |
| D.将Zn换成Cu,用①的方法无法判断Fe比Cu活泼 |
您最近半年使用:0次
2023-01-07更新
|
596次组卷
|
3卷引用:北京师范大学附属中学2022-2023学年上学期高二化学期末试题
7 . 天然气是一种清洁能源,但其中大多含有 、
、 等酸性气体和水汽,会腐蚀管道设备。已知:
等酸性气体和水汽,会腐蚀管道设备。已知: 时氢硫酸和碳酸的电离常数如下表:
时氢硫酸和碳酸的电离常数如下表:
(1)碳钢材质管道发生电化学腐蚀,作负极的物质是_______ 。
(2)用化学用语表示 溶液显酸性的原因
溶液显酸性的原因_______ 。
(3) 溶液可以去除
溶液可以去除 ,写出反应的离子方程式
,写出反应的离子方程式_______ 。
(4)用热碱液( 溶液)吸收天然气中的
溶液)吸收天然气中的 ,可将其转化为可溶性的
,可将其转化为可溶性的 ,反应的化学方程式为
,反应的化学方程式为_______ 。
(5)我国科学家设计了一种 协同转化装置,实现对天然气中
协同转化装置,实现对天然气中 和
和 的高效去除,装置如下图所示。其中电极分别为
的高效去除,装置如下图所示。其中电极分别为 石墨烯(石墨烯包裹的
石墨烯(石墨烯包裹的 )和石墨烯。
)和石墨烯。

① 石墨烯是
石墨烯是_______ 极(填“阳”或“阴”)。
②石墨烯电极区发生反应为:
ⅰ.
ⅱ._______ 。
③ 协同转化总反应的化学方程式为
协同转化总反应的化学方程式为_______ , 在其中所起的作用是
在其中所起的作用是_______ 。
④工作时, 石墨烯电极区的
石墨烯电极区的 基本保持不变,结合化学用语解释原因
基本保持不变,结合化学用语解释原因_______ 。
 、
、 等酸性气体和水汽,会腐蚀管道设备。已知:
等酸性气体和水汽,会腐蚀管道设备。已知: 时氢硫酸和碳酸的电离常数如下表:
时氢硫酸和碳酸的电离常数如下表: | 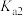 | |
 | 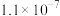 | 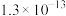 |
 | 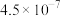 | 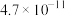 |
(1)碳钢材质管道发生电化学腐蚀,作负极的物质是
(2)用化学用语表示
 溶液显酸性的原因
溶液显酸性的原因(3)
 溶液可以去除
溶液可以去除 ,写出反应的离子方程式
,写出反应的离子方程式(4)用热碱液(
 溶液)吸收天然气中的
溶液)吸收天然气中的 ,可将其转化为可溶性的
,可将其转化为可溶性的 ,反应的化学方程式为
,反应的化学方程式为(5)我国科学家设计了一种
 协同转化装置,实现对天然气中
协同转化装置,实现对天然气中 和
和 的高效去除,装置如下图所示。其中电极分别为
的高效去除,装置如下图所示。其中电极分别为 石墨烯(石墨烯包裹的
石墨烯(石墨烯包裹的 )和石墨烯。
)和石墨烯。
①
 石墨烯是
石墨烯是②石墨烯电极区发生反应为:
ⅰ.

ⅱ.
③
 协同转化总反应的化学方程式为
协同转化总反应的化学方程式为 在其中所起的作用是
在其中所起的作用是④工作时,
 石墨烯电极区的
石墨烯电极区的 基本保持不变,结合化学用语解释原因
基本保持不变,结合化学用语解释原因
您最近半年使用:0次
8 . 实验小组研究金属电化学腐蚀,实验如下:
下列说法不正确 的是
| 序号 | 实验 |  | 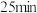 |
| 实验Ⅰ | 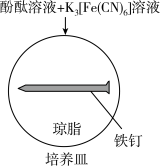 | 铁钉表面及周边未见明显变化 | 铁钉周边零星、随机出现极少量红色和蓝色区域,有少量红棕色铁锈生成 |
| 实验Ⅱ | 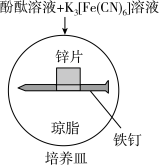 | 铁钉周边出现红色区域,未见蓝色出现 锌片周边未见明显变化 | 铁钉周边红色加深,区域变大,未见蓝色出现 锌片周边未见明显变化 |
| A.实验Ⅰ中铁钉发生了吸氧腐蚀 |
| B.实验Ⅱ中锌片未发生反应 |
C.实验Ⅱ中正极的电极反应式: |
D.若将 片换成 片换成 片,推测 片,推测 片周边会出现红色,铁钉周边会出现蓝色 片周边会出现红色,铁钉周边会出现蓝色 |
您最近半年使用:0次
2023-01-06更新
|
282次组卷
|
4卷引用:北京市丰台区2022-2023学年高二上学期期末考试化学试题
北京市丰台区2022-2023学年高二上学期期末考试化学试题北京市清华大学附属中学2023-2024学年高二上学期(G22级)统练二化学试题河南省实验中学2023-2024学年高二上学期期中考试化学试题(已下线)专题10 电解池 金属的腐蚀与防护-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)
名校
9 . 钢铁腐蚀现象在生产、生活中普遍存在,也是科学研究的关注点之一
(1)碳钢管发生电化学腐蚀是因为形成了原电池,其负极的电极反应式为_______ 。
(2)外加电流的阴极保护法是防止钢铁腐蚀的常用方法之一,该方法中,需将被保护的碳钢管与直流电源的_______ (填“正极”或“负极”)相连。
(3)在铁制品表面镀锌可防止铁制品被腐蚀,镀锌层即使局部破损,仍可防止破损部位被腐蚀,原因是_______ 。
(4)研究人员就大气环境对碳钢腐蚀的影响进行了研究。其中,A、B两个城市的气候环境和碳钢腐蚀速率数据如下:
①研究人员认为,A、B两城市中碳钢同时发生吸氧腐蚀和析氢腐蚀。碳钢发生析氢腐蚀时,正极的电极反应式为_______ 。
②结合化学用语解释A、B两城市中碳钢能发生析氢腐蚀的原因:_______ 。
③用电化学原理分析B城市碳钢腐蚀速率高于A城市的主要原因:_______ 。
(1)碳钢管发生电化学腐蚀是因为形成了原电池,其负极的电极反应式为
(2)外加电流的阴极保护法是防止钢铁腐蚀的常用方法之一,该方法中,需将被保护的碳钢管与直流电源的
(3)在铁制品表面镀锌可防止铁制品被腐蚀,镀锌层即使局部破损,仍可防止破损部位被腐蚀,原因是
(4)研究人员就大气环境对碳钢腐蚀的影响进行了研究。其中,A、B两个城市的气候环境和碳钢腐蚀速率数据如下:
| 城市 | 年均温度℃ | 年均湿度% |  的浓度( 的浓度(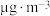 ) ) | 大气 沉积速率( 沉积速率( ) ) | 腐蚀速率(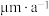 ) ) |
| A | 17.0 | 76 | 61 | 29 | 58 |
| B | 12.3 | 72 | 54 | 420 | 79 |
②结合化学用语解释A、B两城市中碳钢能发生析氢腐蚀的原因:
③用电化学原理分析B城市碳钢腐蚀速率高于A城市的主要原因:
您最近半年使用:0次
2023-01-06更新
|
472次组卷
|
4卷引用:北京海淀区2022-2023学年高二上学期期末考试化学试题
10 . 化学小组研究金属的电化学腐蚀,实验如下:
下列说法不正确 的是
| 序号 | 实验Ⅰ | 实验Ⅱ |
| 实验 | 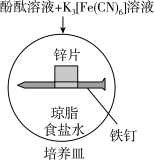 | 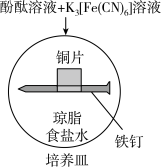 |
| 现象 | 铁钉周边出现_________色 锌片周边未见明显变化 | 铁钉周边出现蓝色 铜片周边略显红色 |
| A.实验Ⅰ中铁钉周边出现红色 |
B.实验I中负极的电极反应式: |
C.实验Ⅱ中正极的电极反应式: |
| D.对比实验I、Ⅱ可知,生活中镀锌铁板比镀铜铁板在镀层破损后更耐腐蚀 |
您最近半年使用:0次
2023-01-06更新
|
391次组卷
|
9卷引用:北京市朝阳区2022-2023学年高二上学期期末考试化学试题