名校
解题方法
1 . 根据原电池的构成、原理、以及原电池反应的快慢等知识,结合图中装置填空:
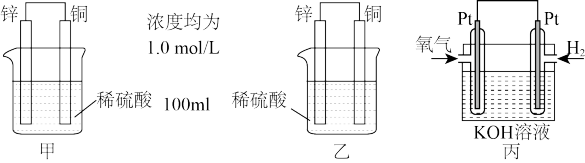
(1)在装置甲和乙中属于原电池装置的是_______ ;(选“甲、乙”作答)
(2)当同时将铜和锌分别按照图示插入甲、乙烧杯中,描述甲、乙烧杯中铜棒上的现象_______ ;乙中锌棒参与反应的离子反应方程式为_______ ;
(3)在图甲装置中,铜(棒)电极上的电极反应式为_______ ,5分钟后甲中溶液质量增重31.5 g,此时转移电子数目为_______ ;
(4)装置丙为氢氧燃料电池的构造图,电解质溶液的溶质是KOH。通入氧气一极的电极反应式为_______ ;当线路中转移4NA个电子时,理论上应消耗H2在标准状况下的体积为_______ 。

(1)在装置甲和乙中属于原电池装置的是
(2)当同时将铜和锌分别按照图示插入甲、乙烧杯中,描述甲、乙烧杯中铜棒上的现象
(3)在图甲装置中,铜(棒)电极上的电极反应式为
(4)装置丙为氢氧燃料电池的构造图,电解质溶液的溶质是KOH。通入氧气一极的电极反应式为
您最近一年使用:0次
20-21高二上·江西南昌·期中
解题方法
2 . 电解工作原理的实际应用非常广泛。
(1)工业上为了处理含有 的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的
的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的____ (填字母)。
A.阳极反应:Fe-2e-=Fe2+
B.阴极反应:2H++2e-=H2↑
C.在电解过程中工业废水由酸性变为碱性
D.可以将铁电极改为石墨电极
(2)某同学设计了如图装置进行以下电化学实验。

①当开关K与a连接时,两极均有气泡产生,则阴极为____ 电极。
②一段时间后,使开关K与a断开,与b连接时,虚线框内的装置可称为_______ ,请写出此时Cu电极上的电极反应______ 。
(3)1 L某溶液中含有的离子如下表:
用惰性电极电解该溶液,当电路中有3 mol e-通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),下列说法正确的是___________ (填字母)。
A.电解后溶液呈酸性 B.a=3
C.阳极生成1.5 mol Cl2 D.阴极析出的金属是铜与铝
(1)工业上为了处理含有
 的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的
的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的A.阳极反应:Fe-2e-=Fe2+
B.阴极反应:2H++2e-=H2↑
C.在电解过程中工业废水由酸性变为碱性
D.可以将铁电极改为石墨电极
(2)某同学设计了如图装置进行以下电化学实验。

①当开关K与a连接时,两极均有气泡产生,则阴极为
②一段时间后,使开关K与a断开,与b连接时,虚线框内的装置可称为
(3)1 L某溶液中含有的离子如下表:
| 离子 | Cu2+ | Al3+ |  | Cl- |
| 物质的量浓度(mol/L) | 1 | 1 | a | 1 |
A.电解后溶液呈酸性 B.a=3
C.阳极生成1.5 mol Cl2 D.阴极析出的金属是铜与铝
您最近一年使用:0次
填空题
|
适中(0.65)
|
名校
3 . 某课外小组分别用如图所示装置对原电池和电解原理进行实验探究。
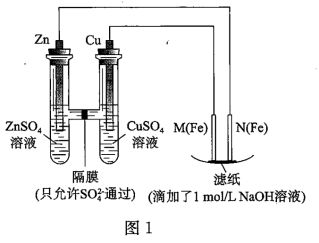
请回答:
I.用图1所示装置进行第一组实验。
(1)在保证电极反应不变的情况下,不能替代Cu做电极的是___ (填字母序号)。
A.铂 B.石墨 C.银 D.铝
(2)M极发生反应的电极反应式为___ 。
(3)实验过程中,SO
___ (填“从左向右”、“从右向左”或“不”)移动;滤纸上能观察到的现象有___ 。
II.用图2所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO )在溶液中呈紫红色。
)在溶液中呈紫红色。
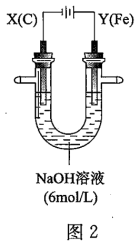
(4)电解过程中,X极区溶液的pH___ (填“增大”、“减小”或“不变”)。
(5)电解过程中,Y极发生的电极反应为Fe-6e-+8OH-=FeO +4H2O和
+4H2O和___ 。
(6)若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少___ g。
(7)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为:2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2。该电池正极发生的反应的电极反应式为___ 。

请回答:
I.用图1所示装置进行第一组实验。
(1)在保证电极反应不变的情况下,不能替代Cu做电极的是
A.铂 B.石墨 C.银 D.铝
(2)M极发生反应的电极反应式为
(3)实验过程中,SO

II.用图2所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO
 )在溶液中呈紫红色。
)在溶液中呈紫红色。
(4)电解过程中,X极区溶液的pH
(5)电解过程中,Y极发生的电极反应为Fe-6e-+8OH-=FeO
 +4H2O和
+4H2O和(6)若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少
(7)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为:2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2。该电池正极发生的反应的电极反应式为
您最近一年使用:0次
解题方法
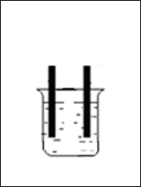
4 . 原电池是将化学能转化为电能的装置。如图,烧杯中是稀硫酸溶液
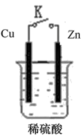
(1)当开关K断开时产生的现象为___________ 。
A.铜片不断溶解B.锌片不断溶解C.铜片上产生气泡D.锌片上产生气泡E.溶液逐渐变蓝
(2)闭合开关K,经过一段时间后,若导线中转移了0.4mol电子,则产生的气体在标况下的体积为___________ 。
(3)如果反应太剧烈,为了减缓反应速率而又不减少产生氢气的量,该同学在烧杯中分别加入等体积的下列液体,你认为可行的是___________ (填序号)。
A.蒸馏水 B.NaCl溶液 C. 溶液 D.
溶液 D. 溶液
溶液
(4)FeCl3常用于腐蚀印刷电路铜板(2FeCl3+Cu=2FeCl2+CuCl2)请将此反应设计成原电池并画在框中___________ ,该原电池负极的电极材料为___________ ,负极的电极反应式为___________ 。

(1)当开关K断开时产生的现象为
A.铜片不断溶解B.锌片不断溶解C.铜片上产生气泡D.锌片上产生气泡E.溶液逐渐变蓝
(2)闭合开关K,经过一段时间后,若导线中转移了0.4mol电子,则产生的气体在标况下的体积为
(3)如果反应太剧烈,为了减缓反应速率而又不减少产生氢气的量,该同学在烧杯中分别加入等体积的下列液体,你认为可行的是
A.蒸馏水 B.NaCl溶液 C.
 溶液 D.
溶液 D. 溶液
溶液(4)FeCl3常用于腐蚀印刷电路铜板(2FeCl3+Cu=2FeCl2+CuCl2)请将此反应设计成原电池并画在框中

您最近一年使用:0次
名校
解题方法
5 . 为了探究原电池和电解池的工作原理,某研究性学习小组分别用如图所示的装置进行实验,回答下列问题。
Ⅰ.用甲装置进行第一组实验:
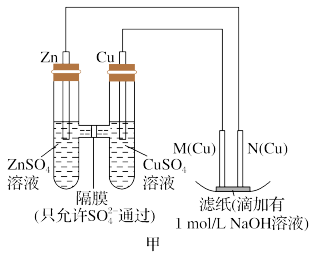
(1)在保证电极反应不变的情况下,下列材料不能代替插入硫酸铜溶液中的Cu电极的是___________ (填序号)。
A.石墨 B.镁 C.银 D.铂
(2)实验过程中,SO (填“从左向右”、“从右向左”或“不”)移动;滤纸上能观察到的现象有
(填“从左向右”、“从右向左”或“不”)移动;滤纸上能观察到的现象有___________ 。
Ⅱ.该小组同学用乙装置进行第二组实验时发现,两极均有气体产生,Y极溶液逐渐变成紫红色,停止实验后观察到铁电极明显变细,电解液仍澄清。查阅资料知,高铁酸根离子(FeO )在溶液中呈紫红色。请根据实验现象及所查信息,填写下列空白:
)在溶液中呈紫红色。请根据实验现象及所查信息,填写下列空白:
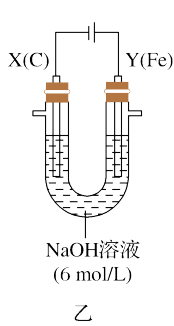
(3)电解过程中,X极溶液的pH___________ (填“增大”、“减小”或者“不变”)。
(4)电解过程中,Y极发生的电极反应为___________ 和___________ 。
(5)另一小组同学将乙装置中6 mol/L NaOH溶液换成1 mol/L NaCl溶液,发现铁电极附近逐渐变成浅绿色,该小组同学认为铁电极附近溶液中生成了Fe2+,为了验证这一猜测,应使用___________ (填试剂名称)来检验,现象为___________ ,则证明该小组同学猜想正确。
(6)下图中,Ⅰ是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图。
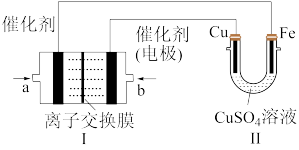
①该同学想在Ⅱ中实现铁上镀铜,a处电极上发生的电极反应为___________ 。
②Ⅱ中电解前CuSO4溶液的浓度为3 mol/L,若维持电流强度为1 A,电池工作十分钟,理论上消耗Ⅰ中的CH4___________ g(计算结果保留两位有效数字,已知F=96500 C·mol-1),此时电解池中CuSO4溶液的浓度为___________ 。
Ⅰ.用甲装置进行第一组实验:

(1)在保证电极反应不变的情况下,下列材料不能代替插入硫酸铜溶液中的Cu电极的是
A.石墨 B.镁 C.银 D.铂
(2)实验过程中,SO
 (填“从左向右”、“从右向左”或“不”)移动;滤纸上能观察到的现象有
(填“从左向右”、“从右向左”或“不”)移动;滤纸上能观察到的现象有Ⅱ.该小组同学用乙装置进行第二组实验时发现,两极均有气体产生,Y极溶液逐渐变成紫红色,停止实验后观察到铁电极明显变细,电解液仍澄清。查阅资料知,高铁酸根离子(FeO
 )在溶液中呈紫红色。请根据实验现象及所查信息,填写下列空白:
)在溶液中呈紫红色。请根据实验现象及所查信息,填写下列空白:
(3)电解过程中,X极溶液的pH
(4)电解过程中,Y极发生的电极反应为
(5)另一小组同学将乙装置中6 mol/L NaOH溶液换成1 mol/L NaCl溶液,发现铁电极附近逐渐变成浅绿色,该小组同学认为铁电极附近溶液中生成了Fe2+,为了验证这一猜测,应使用
(6)下图中,Ⅰ是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图。

①该同学想在Ⅱ中实现铁上镀铜,a处电极上发生的电极反应为
②Ⅱ中电解前CuSO4溶液的浓度为3 mol/L,若维持电流强度为1 A,电池工作十分钟,理论上消耗Ⅰ中的CH4
您最近一年使用:0次
解题方法
6 . 某课外化学兴趣小组设计两组实验,探究KI的性质。

Ⅰ.探究KI与FeCl3的反应,设计方案如图1所示:
(1) 请用离子方程式表示上述实验现象所得的结论:_____________________________________ 。
(2) 小组成员经过讨论,认为还有必要补充做FeCl2溶液与碘水的实验,则该实验操作和相应的现象是____________________________________________________________________ 。
Ⅱ.为了探究KBrO3溶液与KI溶液的反应。该小组查阅资料,得知氧化性强弱顺序为
BrO >IO
>IO >Br2>Fe3+,并设计如图2所示装置。电极均为碳电极,盐桥中的电解质为硫酸钾。在右池中加入100 mL 0.6 mol·L-1 KI溶液及少许淀粉溶液,左池中先加入足量的稀硫酸,再通过滴定管逐滴滴加0.1 mol·L-1 KBrO3溶液,观察到以下现象:当滴加KBrO3溶液时,电流计的指针发生偏转,同时右池中的溶液变蓝,继续滴加KBrO3溶液时,发现滴加过程中有一段时间电流计的指针不再偏转,再继续滴加,发现电流计的指针又开始发生偏转。
>Br2>Fe3+,并设计如图2所示装置。电极均为碳电极,盐桥中的电解质为硫酸钾。在右池中加入100 mL 0.6 mol·L-1 KI溶液及少许淀粉溶液,左池中先加入足量的稀硫酸,再通过滴定管逐滴滴加0.1 mol·L-1 KBrO3溶液,观察到以下现象:当滴加KBrO3溶液时,电流计的指针发生偏转,同时右池中的溶液变蓝,继续滴加KBrO3溶液时,发现滴加过程中有一段时间电流计的指针不再偏转,再继续滴加,发现电流计的指针又开始发生偏转。

(3) 当开始滴加KBrO3溶液时,右池中的电极反应式为___________________________ 。
(4) 在电流计指针不再发生偏转的这段时间里,滴加的KBrO3溶液的体积为_____________ mL。
(5) 当电流计的指针重新发生偏转时,右池中的现象是________________________________ ,左池中的电极反应式为_____________________________________________________ 。

Ⅰ.探究KI与FeCl3的反应,设计方案如图1所示:
(1) 请用离子方程式表示上述实验现象所得的结论:
(2) 小组成员经过讨论,认为还有必要补充做FeCl2溶液与碘水的实验,则该实验操作和相应的现象是
Ⅱ.为了探究KBrO3溶液与KI溶液的反应。该小组查阅资料,得知氧化性强弱顺序为
BrO
 >IO
>IO >Br2>Fe3+,并设计如图2所示装置。电极均为碳电极,盐桥中的电解质为硫酸钾。在右池中加入100 mL 0.6 mol·L-1 KI溶液及少许淀粉溶液,左池中先加入足量的稀硫酸,再通过滴定管逐滴滴加0.1 mol·L-1 KBrO3溶液,观察到以下现象:当滴加KBrO3溶液时,电流计的指针发生偏转,同时右池中的溶液变蓝,继续滴加KBrO3溶液时,发现滴加过程中有一段时间电流计的指针不再偏转,再继续滴加,发现电流计的指针又开始发生偏转。
>Br2>Fe3+,并设计如图2所示装置。电极均为碳电极,盐桥中的电解质为硫酸钾。在右池中加入100 mL 0.6 mol·L-1 KI溶液及少许淀粉溶液,左池中先加入足量的稀硫酸,再通过滴定管逐滴滴加0.1 mol·L-1 KBrO3溶液,观察到以下现象:当滴加KBrO3溶液时,电流计的指针发生偏转,同时右池中的溶液变蓝,继续滴加KBrO3溶液时,发现滴加过程中有一段时间电流计的指针不再偏转,再继续滴加,发现电流计的指针又开始发生偏转。
(3) 当开始滴加KBrO3溶液时,右池中的电极反应式为
(4) 在电流计指针不再发生偏转的这段时间里,滴加的KBrO3溶液的体积为
(5) 当电流计的指针重新发生偏转时,右池中的现象是
您最近一年使用:0次
名校
解题方法
7 . 甲烷燃料电池体积小巧、燃料使用便利、洁净环保、理论能量比高,用甲烷燃料电池为下图电解装置供电,工作一段时间后,A池中左右试管收集到的气体体积比为2:1,则:


(1)甲烷燃料电池中通入甲烷的电极为______ 极,该电极反应式为_________________ ,通入O2的电极反应式为________________________________ 。
(2)甲烷燃料电池中导线A与电解池中的________ (填M或N)导线连接。
(3)B池中一段时间后实验现象为______________________ 。
(4)C池反应的总方程式为__________________ ;D池反应的总方程式为_________________ 。
(5)相同条件下,电解质足量的A、B、C、D池中生成气体的总体积由大到小的顺序为_________________ 。
(6)D池电解一段时间后,若要使电解质溶液恢复到电解前的状态,可加入____ 。


(1)甲烷燃料电池中通入甲烷的电极为
(2)甲烷燃料电池中导线A与电解池中的
(3)B池中一段时间后实验现象为
(4)C池反应的总方程式为
(5)相同条件下,电解质足量的A、B、C、D池中生成气体的总体积由大到小的顺序为
(6)D池电解一段时间后,若要使电解质溶液恢复到电解前的状态,可加入
您最近一年使用:0次
8 . 钢铁工业是国家工业的基础,钢铁生锈现象却随处可见,为此每年国家损失大量资金。
(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的正极电极反应式为:_____________
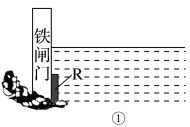
(2)为了降低某水库的铁闸门被腐蚀的速率,可以采用图①所示的方案,其中焊接在铁闸门上的固体材料R可以采用________ 。
A.铜 B.钠 C.锌 D.石墨
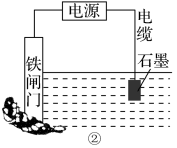
(3)图②所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的__________ 极。
(4)钢铁的防护除了用电化学保护方法之外,在钢铁制品表面镀铜也可以有效地防止其腐蚀,电镀的装置如图所示:
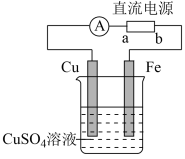
①电镀装置图的“直流电源”中,______  填“a”或“b”
填“a”或“b” 是正极。Fe电极反应式为
是正极。Fe电极反应式为_________ ;
②接通电源前,装置图中的铜、铁两个电极质量相等,电镀完成后,将两个电极取出,用水小心冲洗干净、烘干,然后称量,二者质量之差为5.12g,由此计算电镀过程中电路中通过电子的物质的量为________ 。
③上述铁镀件破损后,铁更容易被腐蚀。请简要说明镀铜铁镀件破损后,铁更容易被腐蚀的原因:______ 。


(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的正极电极反应式为:
(2)为了降低某水库的铁闸门被腐蚀的速率,可以采用图①所示的方案,其中焊接在铁闸门上的固体材料R可以采用
A.铜 B.钠 C.锌 D.石墨
(3)图②所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的
(4)钢铁的防护除了用电化学保护方法之外,在钢铁制品表面镀铜也可以有效地防止其腐蚀,电镀的装置如图所示:

①电镀装置图的“直流电源”中,
 填“a”或“b”
填“a”或“b”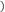 是正极。Fe电极反应式为
是正极。Fe电极反应式为②接通电源前,装置图中的铜、铁两个电极质量相等,电镀完成后,将两个电极取出,用水小心冲洗干净、烘干,然后称量,二者质量之差为5.12g,由此计算电镀过程中电路中通过电子的物质的量为
③上述铁镀件破损后,铁更容易被腐蚀。请简要说明镀铜铁镀件破损后,铁更容易被腐蚀的原因:
您最近一年使用:0次
名校
解题方法
9 . 在如图所示的装置中,若通入直流电5min时,铜电极质量增加2.16g,试回答:

(1)电源电极X名称为______ 。
(2)pH变化:A_______ ,B_______ ,C_______ (填“增大”“减小”或“不变”)。
(3)A中左边Pt电极现象__________ ,C中银电极反应式__________ 。
(4)通电5min时,B中共收集224mL气体(标准状况),溶液体积为200mL,则通电前CuSO4溶液的物质的量浓度为__________ (设电解前后溶液体积无变化)。
(5)若A中饱和KCl溶液的体积也是200mL,电解后,溶液的OH-浓度为________ (设电解前后溶液体积无变化)。

(1)电源电极X名称为
(2)pH变化:A
(3)A中左边Pt电极现象
(4)通电5min时,B中共收集224mL气体(标准状况),溶液体积为200mL,则通电前CuSO4溶液的物质的量浓度为
(5)若A中饱和KCl溶液的体积也是200mL,电解后,溶液的OH-浓度为
您最近一年使用:0次
10 . 按如图所示装置进行下列不同的操作,请回答有关问题:操作:①只接通K1;②只接通K2;③只接通K3;④都断开。

(1)铁棒的腐蚀速率由大到小的顺序是____ (填操作序号)。
(2)原料粗盐中常含有泥沙和Ca2+、SO42-等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)③BaCl2,这3种试剂添加的合理顺序是_____ (填序号)。
(3)若把U形管中的NaCl溶液换成100mL0.1mol/L的CuSO4溶液,且只进行操作②,则当电路中通过0.01mol电子时:(填“铁”或“石墨”)____ 电极增重_____ g,此时溶液的pH=_____ (忽略溶液体积变化)。
(4)若把U形管中的NaCl溶液换成加入了2molAgNO3、1molNa2SO4和1molBaCl2后的溶液,且只进行操作②,则装置中可观察到的现象为:____ 。通电一段时间后,氧化产物与还原产物的质量比为_____ 。

(1)铁棒的腐蚀速率由大到小的顺序是
(2)原料粗盐中常含有泥沙和Ca2+、SO42-等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)③BaCl2,这3种试剂添加的合理顺序是
(3)若把U形管中的NaCl溶液换成100mL0.1mol/L的CuSO4溶液,且只进行操作②,则当电路中通过0.01mol电子时:(填“铁”或“石墨”)
(4)若把U形管中的NaCl溶液换成加入了2molAgNO3、1molNa2SO4和1molBaCl2后的溶液,且只进行操作②,则装置中可观察到的现象为:
您最近一年使用:0次
2020-05-06更新
|
101次组卷
|
2卷引用:四川省成都外国语学校2019-2020学年高二下学期开学考试化学试题



