名校
解题方法
1 . 下列过程的化学方程式或离子方程式书写正确的是
A.用石英砂制粗硅: |
B.电解饱和的 溶液: 溶液: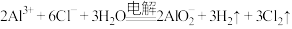 |
C.乙醛的银镜反应: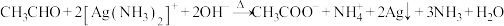 |
D.铅酸蓄电池放电时的正极反应: |
您最近一年使用:0次
名校
解题方法
2 . I.化学反应中伴随着能量变化,根据相关知识回答下列问题:
(1)下列过程吸热的是___________ (填序号)。
a.生石灰溶于水 b.浓硫酸稀释 c.硝酸铵溶于水 d.铜溶于浓硝酸
e.氯化铵固体与氢氧化钡晶体混合搅拌
(2)已知H2和O2反应放热, 且断开1molH-H键、1molO=O键、1molO-H键需吸收的能量分别为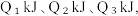 由此可以推知下列关系正确的是
由此可以推知下列关系正确的是___________ (填序号)。
①.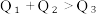 ②.
②. 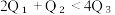 ③.
③. 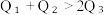 ④.
④. 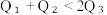
Ⅱ.某同学用导线将电流表与Zn片、Cu片相连接,插入盛有稀硫酸的烧杯中进行实验,如图所示。___________ 。
(4)从构成原电池的基本要素来看,稀硫酸的作用是(选填以下序号)___________ 。
a.反应物 b.电极材料 c.离子导体 d.电子导体
(5)该原电池的负极反应式为___________ ,___________ (填“电子”或“电流”)是由锌片经导线流向铜片。标准状况下,若反应过程中溶解了6.5g锌,则生成的氢气的体积为___________ L。
(6)某同学想利用反应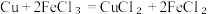 设计一个原电池请在下图
设计一个原电池请在下图___________ (共2处)标出使用的用品。
(1)下列过程吸热的是
a.生石灰溶于水 b.浓硫酸稀释 c.硝酸铵溶于水 d.铜溶于浓硝酸
e.氯化铵固体与氢氧化钡晶体混合搅拌
(2)已知H2和O2反应放热, 且断开1molH-H键、1molO=O键、1molO-H键需吸收的能量分别为
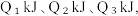 由此可以推知下列关系正确的是
由此可以推知下列关系正确的是①.
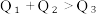 ②.
②. 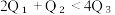 ③.
③. 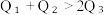 ④.
④. 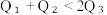
Ⅱ.某同学用导线将电流表与Zn片、Cu片相连接,插入盛有稀硫酸的烧杯中进行实验,如图所示。
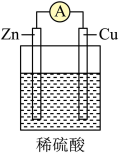
(4)从构成原电池的基本要素来看,稀硫酸的作用是(选填以下序号)
a.反应物 b.电极材料 c.离子导体 d.电子导体
(5)该原电池的负极反应式为
(6)某同学想利用反应
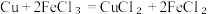 设计一个原电池请在下图
设计一个原电池请在下图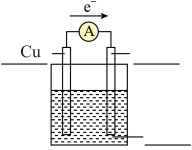
您最近一年使用:0次
解题方法
3 . 在2L恒温恒容密闭容器中投入2molSO2和1molO2在一定条件下充分反应,如图是SO2和SO3随时间的变化曲线。___________ ;平衡时,SO2的转化率为___________ 。
(2)下列叙述能判断该反应达到平衡状态的是___________ (填序号)。
①容器中压强不再改变
②容器中气体密度不再改变
③SO3的质量不再改变
④O2的物质的量浓度不再改变
⑤SO2的消耗速率和SO3的生成速率相等
(3)以下操作会引起化学反应速率变快的是___________ (填字母)。
A.向容器中通入氦气 B.升高温度 C.扩大容器的容积 D.向容器中通入O2 E.使用催化剂
(4)25min时,正反应速率___________ 逆反应速率(填“>”“<”或“=”)。
(5)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:___________ 。(填“正极”或“负极”)
②电解质溶液中OH-离子向___________ 移动(填“电极a”或“电极b”)。
③电极b的电极反应式为___________ 。

(2)下列叙述能判断该反应达到平衡状态的是
①容器中压强不再改变
②容器中气体密度不再改变
③SO3的质量不再改变
④O2的物质的量浓度不再改变
⑤SO2的消耗速率和SO3的生成速率相等
(3)以下操作会引起化学反应速率变快的是
A.向容器中通入氦气 B.升高温度 C.扩大容器的容积 D.向容器中通入O2 E.使用催化剂
(4)25min时,正反应速率
(5)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:
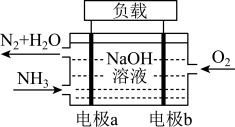
②电解质溶液中OH-离子向
③电极b的电极反应式为
您最近一年使用:0次
名校
解题方法
4 . 按要求写出下列反应的方程式:
(1)实验室制氨气的化学方程式:___________ 。
(2)浓硝酸久置呈黄色的原因用化学方程式解释:___________ 。
(3)工业制粗硅的化学方程式:___________ 。
(4)往硅酸钠溶液中通入过量二氧化碳的离子方程式:___________ 。
(5) 与稀硫酸反应的离子方程式:
与稀硫酸反应的离子方程式:___________ 。
(6)澄清石灰水中通入少量 的离子方程式:
的离子方程式:___________ 。
(7)银锌电池是一种常见的化学电源,其反应原理: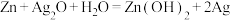 ,其工作原理如图所示。
,其工作原理如图所示。 电极反应式为
电极反应式为___________ 。
(8)将用导线相连的两个铂电极插入 溶液中,然后向两极分别通入
溶液中,然后向两极分别通入 和
和 ,则发生了原电池反应,该原电池中的负极反应式为
,则发生了原电池反应,该原电池中的负极反应式为___________ 。
(1)实验室制氨气的化学方程式:
(2)浓硝酸久置呈黄色的原因用化学方程式解释:
(3)工业制粗硅的化学方程式:
(4)往硅酸钠溶液中通入过量二氧化碳的离子方程式:
(5)
 与稀硫酸反应的离子方程式:
与稀硫酸反应的离子方程式:(6)澄清石灰水中通入少量
 的离子方程式:
的离子方程式:(7)银锌电池是一种常见的化学电源,其反应原理:
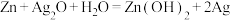 ,其工作原理如图所示。
,其工作原理如图所示。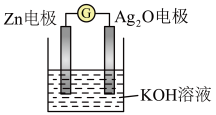
 电极反应式为
电极反应式为(8)将用导线相连的两个铂电极插入
 溶液中,然后向两极分别通入
溶液中,然后向两极分别通入 和
和 ,则发生了原电池反应,该原电池中的负极反应式为
,则发生了原电池反应,该原电池中的负极反应式为
您最近一年使用:0次
名校
解题方法
5 . 流动电池是一种新型电池。其主要特点是可以通过电解质溶液的循环流动,在电池外部调节电解质溶液,以保持电池内部电极周围溶液浓度的稳定。北京化工大学新开发的一种流动电池如图所示,电池总反应为 。
。
 。
。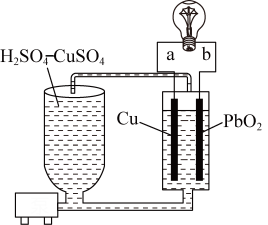
A. 为负极,a为正极 为负极,a为正极 |
B.该电池工作时,电流由电极a流向电极 |
C. 极的电极反应式为 极的电极反应式为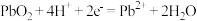 |
D.调节电解质溶液的方法是补充 |
您最近一年使用:0次
名校
解题方法
6 . 下列说法不正确的是
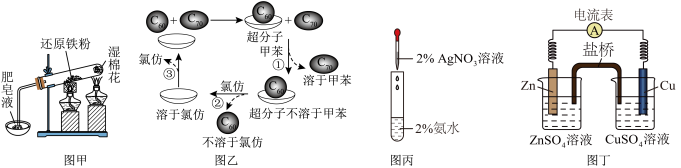
| A.装置甲可以用于探究铁与水蒸气反应,并点燃肥皂泡检验氢气 |
B.图乙用 (杯酚)识别 (杯酚)识别 和 和 ,操作①②为过滤,操作③为蒸馏 ,操作①②为过滤,操作③为蒸馏 |
| C.装置丙可用于实验室配制银氨溶液 |
D.装置丁中若将 溶液替换成 溶液替换成 溶液,仍然形成原电池 溶液,仍然形成原电池 |
您最近一年使用:0次
名校
7 . 某学习小组用如下图所示装置A、B分别探究金属锌与稀硫酸的反应,实验过程中A烧杯内的溶液温度升高,B烧杯的电流计指针发生偏转,请回答以下问题。___________ 。
(2)在B烧杯中
①Zn电极为原电池的_______ 极(填“正”或“负”),该电极反应式为_______ 。发生的电极反应类型是________ 反应(填氧化或还原)。
②Cu电极上的现象是________ ,该电极反应式为_______ 发生的电极反应类型是_______ 反应(填氧化或还原)。
(3)从能量转化的角度来看,A、B中反应物的总能量___________ (填“大于”、“小于”或“等于”)生成物总能量,A中是将化学能转变为___________ ,B中主要是将化学能转变为___________ 。
(4)该小组同学反思原电池的原理,其中观点不正确的是___________ (填字母序号)。
A.电极一定不能参加反应
B.在原电池装置的内电路中阴离子向正极移动
C.原电池反应的过程中一定有电子转移
D.氧化反应和还原反应可以拆开在两极发生
E.化学能与其他形式的能相互转化的途径是化学反应
F.原电池中电子通过导线由正极极流向负极
(5)在上面的原电池装置中,如果Zn电极溶解了0.65 g,则在Cu电极上产生 的体积约为
的体积约为___________ L(标准状况下)

(2)在B烧杯中
①Zn电极为原电池的
②Cu电极上的现象是
(3)从能量转化的角度来看,A、B中反应物的总能量
(4)该小组同学反思原电池的原理,其中观点不正确的是
A.电极一定不能参加反应
B.在原电池装置的内电路中阴离子向正极移动
C.原电池反应的过程中一定有电子转移
D.氧化反应和还原反应可以拆开在两极发生
E.化学能与其他形式的能相互转化的途径是化学反应
F.原电池中电子通过导线由正极极流向负极
(5)在上面的原电池装置中,如果Zn电极溶解了0.65 g,则在Cu电极上产生
 的体积约为
的体积约为
您最近一年使用:0次
8 . 回答下列问题:
(1)如图为以惰性电极进行电解的装置:写出A、B、C、D各电极上的电极反应式和总反应方程式: 溶液
溶液  溶液
溶液
A:__________ ,B:__________ ,总反应方程式:__________ ,
C:__________ ,D:__________ ,总反应方程式:__________ 。
(2)两个烧杯中电解质溶液足量,则A、B、C、D四个电极产物的物质的量之比为__________ 。
(3)氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀了一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:__________ 。
②正极上消耗 (标准状况)气体时,转移电子的物质的量为
(标准状况)气体时,转移电子的物质的量为__________ 。
(1)如图为以惰性电极进行电解的装置:写出A、B、C、D各电极上的电极反应式和总反应方程式:

 溶液
溶液  溶液
溶液A:
C:
(2)两个烧杯中电解质溶液足量,则A、B、C、D四个电极产物的物质的量之比为
(3)氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀了一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:

②正极上消耗
 (标准状况)气体时,转移电子的物质的量为
(标准状况)气体时,转移电子的物质的量为
您最近一年使用:0次
名校
解题方法
9 . 科学家称他们正在研制的铝电池未来有望取代锂电池。银铝电池具有能量密度高的优点,电池装置如图;电池放电时的反应为: 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是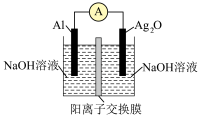
A. 电极发生还原反应 电极发生还原反应 |
| B.阳离子交换膜允许阳离子和电子通过 |
C.当导线中通过 电子时,负极区溶液质量减小 电子时,负极区溶液质量减小 |
D.正极电极反应式为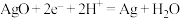 |
您最近一年使用:0次
2024-04-23更新
|
876次组卷
|
3卷引用:天津市河北区2024届高三总复习质量检测(一)化学试题
天津市河北区2024届高三总复习质量检测(一)化学试题(已下线)题型8 反应热 电化学的综合考查(25题)-2024年高考化学常考点必杀300题(新高考通用)2024届陕西省西安中学高三下学期第七次模拟考试理综试题-高中化学
名校
解题方法
10 . 将用导线连接的电极X、Y插入装有稀 的烧杯中(外电路中电子流向如图所示)。根据下图判断并回答下列问题:
的烧杯中(外电路中电子流向如图所示)。根据下图判断并回答下列问题:________ 极(填“正”或“负”,电极反应式为:________ 。当转移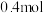 电子时,则生成标况下的氢气体积是
电子时,则生成标况下的氢气体积是________ L。
(2)若电极材料都是金属棒,则金属活动性:X________ Y(填“大于”或“小于”或“等于”)
(3)化学反应速率受到很多因素的影响,例如:实验室制取氢气时一般用粗锌(含铁)代替纯锌和稀硫酸反应,这是利用________ 原理加快了氢气生成的速率。
 的烧杯中(外电路中电子流向如图所示)。根据下图判断并回答下列问题:
的烧杯中(外电路中电子流向如图所示)。根据下图判断并回答下列问题:
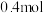 电子时,则生成标况下的氢气体积是
电子时,则生成标况下的氢气体积是(2)若电极材料都是金属棒,则金属活动性:X
(3)化学反应速率受到很多因素的影响,例如:实验室制取氢气时一般用粗锌(含铁)代替纯锌和稀硫酸反应,这是利用
您最近一年使用:0次



