解题方法
1 . 镁锰电池的结构如图所示,放电时总反应为 ,如果给镁锰电池充电,则会发生爆炸.下列说法错误的是
,如果给镁锰电池充电,则会发生爆炸.下列说法错误的是
 ,如果给镁锰电池充电,则会发生爆炸.下列说法错误的是
,如果给镁锰电池充电,则会发生爆炸.下列说法错误的是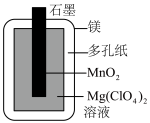
| A.负极为镁 | B.工作时,电子由镁电极流出,经过 溶液后进入石墨电极 溶液后进入石墨电极 |
| C.镁锰电池为一次电池 | D. 溶液中有自由移动的离子 溶液中有自由移动的离子 |
您最近一年使用:0次
解题方法
2 . 电池在许多领域中扮演着重要角色,从移动设备到太空探索,从医疗设备到军事科技,无处不在.
(1)伏打电池是意大利教授伏打发明的电池组,开创了电学发展的新时代.一种伏打电池结构如图1所示,银片和锌片间隔有浸渍 溶液的纸板.伏打电池的正极为
溶液的纸板.伏打电池的正极为_________ (填“a”或“b”),若将银片换成__________ (填标号),则电流计中没有电子流过.
A.陶瓷片 B.锌片 C.铜片 D.镁片
(2)1859年,法国物理学家普兰特发明了铅酸蓄电池,其结构如图2所示.放电时,负极的质量________ (填“增大”“减小”或“不变”),正极上的电极反应式为________________ .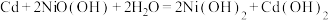 ,下列说法正确的是_______(填标号).
,下列说法正确的是_______(填标号).
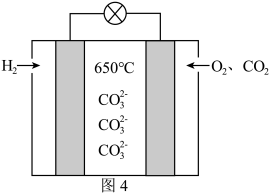
(4)近年来,采用非贵重金属作为催化剂的节能环保的熔融碳酸盐燃料电池备受青睐,其工作原理如图4.该电池负极上的电极反应式为_______ ,相同条件下,正、负极消耗的气体的体积之比为_______ .
(1)伏打电池是意大利教授伏打发明的电池组,开创了电学发展的新时代.一种伏打电池结构如图1所示,银片和锌片间隔有浸渍
 溶液的纸板.伏打电池的正极为
溶液的纸板.伏打电池的正极为A.陶瓷片 B.锌片 C.铜片 D.镁片
(2)1859年,法国物理学家普兰特发明了铅酸蓄电池,其结构如图2所示.放电时,负极的质量
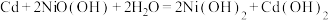 ,下列说法正确的是_______(填标号).
,下列说法正确的是_______(填标号).| A.镍镉电池充电时,化学能转化为电能 | B.放电时,负极发生了氧化反应 |
| C.电解质溶液为稀硫酸 | D.镍镉电池为二次电池 |
(4)近年来,采用非贵重金属作为催化剂的节能环保的熔融碳酸盐燃料电池备受青睐,其工作原理如图4.该电池负极上的电极反应式为
您最近一年使用:0次
名校
解题方法
3 . 根据原电池原理,回答下列问题:
(1)铜锌原电池的装置如图所示:___________ (填“正极”或“负极”),溶液中的 向
向___________ (填“铁”或“铜”)电极方向移动。
②负极的电极反应式为___________ 。
③若反应过程中有 电子的转移,则生成标准状况下氢气的体积为
电子的转移,则生成标准状况下氢气的体积为___________  。
。
(2)某兴趣小组为了探究铝电极在电池中的作用,设计并进行了以下实验,实验结果记录如下:
已知:实验均为常温下完成;电流计指针偏转方向为正极方向。
①实验3中, 为
为___________ 极,电极反应式为___________ 。
②实验4中, 为
为___________ 极,电池总反应的离子方程式是___________ 。
③根据实验结果总结出影响铝在电池中做正极或负极的因素有___________ 。
(1)铜锌原电池的装置如图所示:

 向
向②负极的电极反应式为
③若反应过程中有
 电子的转移,则生成标准状况下氢气的体积为
电子的转移,则生成标准状况下氢气的体积为 。
。(2)某兴趣小组为了探究铝电极在电池中的作用,设计并进行了以下实验,实验结果记录如下:
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| 1 | 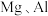 | 稀盐酸 | 偏向 |
| 2 | 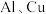 | 稀盐酸 | 偏向 |
| 3 | 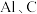 (石墨) (石墨) | 稀盐酸 | 偏向石墨 |
| 4 | 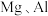 |  溶液 溶液 | 偏向 |
| 5 | 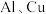 | 浓硝酸 | 偏向 |
①实验3中,
 为
为②实验4中,
 为
为③根据实验结果总结出影响铝在电池中做正极或负极的因素有
您最近一年使用:0次
解题方法
4 . 原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)将纯锌片和纯铜片按图中方式插入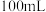 相同浓度的稀硫酸中一段时间,回答下列问题:
相同浓度的稀硫酸中一段时间,回答下列问题:___________ 。
A.甲、乙均为化学能转变为电能的装置
B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少
D.两烧杯中溶液的 均增大
均增大
②相同时间内,甲、乙中产生气泡的速度:甲___________ 乙(填“ ”“
”“ ”或“
”或“ ”)。
”)。
③请写出图中构成原电池的负极电极反应式:___________ 。 构成原电池的装置工作时,溶液中 向
向 ___________ 极移动。
④当乙中产生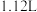 (标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至
(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至 ,测得溶液中
,测得溶液中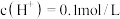 (设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为
(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为___________ 。
(2)当甲中产生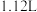 (标准状况)气体时,理论上通过导线的电子数目为
(标准状况)气体时,理论上通过导线的电子数目为___________ 。
(3)若将反应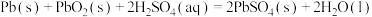 设计成原电池。用导线连接金属
设计成原电池。用导线连接金属 和
和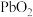 ,电解质为稀硫酸。
,电解质为稀硫酸。
①正极为___________ (填“ ”或“
”或“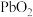 ”)极。
”)极。
(1)将纯锌片和纯铜片按图中方式插入
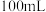 相同浓度的稀硫酸中一段时间,回答下列问题:
相同浓度的稀硫酸中一段时间,回答下列问题: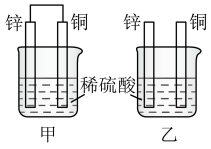
A.甲、乙均为化学能转变为电能的装置
B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少
D.两烧杯中溶液的
 均增大
均增大②相同时间内,甲、乙中产生气泡的速度:甲
 ”“
”“ ”或“
”或“ ”)。
”)。③请写出图中构成原电池的负极电极反应式:
 向
向 ④当乙中产生
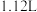 (标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至
(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至 ,测得溶液中
,测得溶液中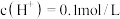 (设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为
(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为(2)当甲中产生
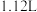 (标准状况)气体时,理论上通过导线的电子数目为
(标准状况)气体时,理论上通过导线的电子数目为(3)若将反应
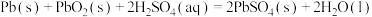 设计成原电池。用导线连接金属
设计成原电池。用导线连接金属 和
和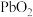 ,电解质为稀硫酸。
,电解质为稀硫酸。①正极为
 ”或“
”或“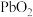 ”)极。
”)极。
您最近一年使用:0次
名校
解题方法
5 . 化学反应在发生物质变化的同时伴随有能量的变化,是人类获取能量的重要途径,请回答下列问题。
(1)硅是太阳能电池的重要材料。“精炼硅”反应历程中的能量变化如下图所示:___________ (选填“吸热”或“放热)反应。
(2)在容积为 的恒容密闭容器中投入等物质的量的
的恒容密闭容器中投入等物质的量的 和
和 ,进行反应:
,进行反应: 。
。 、
、 的物质的量随时间变化关系如下图所示。
的物质的量随时间变化关系如下图所示。___________ (填“a”、“b”、“c”或“d”);用同一物质表示反应速率时,a、c两点的正反应速率: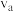
___________ 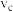 。(填“大于”、“小于”或“等于”,下同),该反应达到平衡时,
。(填“大于”、“小于”或“等于”,下同),该反应达到平衡时, 的转化率
的转化率___________ 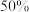 。
。
(3)甲烷燃料电池装置如图所示,通入 的电极为电池的
的电极为电池的___________ (填“正极”或“负极”),通入氧气一端电极反应方程式为___________ ,当有 电子转移时,消耗
电子转移时,消耗 的物质的量是
的物质的量是___________ 。
(1)硅是太阳能电池的重要材料。“精炼硅”反应历程中的能量变化如下图所示:

(2)在容积为
 的恒容密闭容器中投入等物质的量的
的恒容密闭容器中投入等物质的量的 和
和 ,进行反应:
,进行反应: 。
。 、
、 的物质的量随时间变化关系如下图所示。
的物质的量随时间变化关系如下图所示。
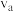
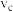 。(填“大于”、“小于”或“等于”,下同),该反应达到平衡时,
。(填“大于”、“小于”或“等于”,下同),该反应达到平衡时, 的转化率
的转化率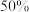 。
。(3)甲烷燃料电池装置如图所示,通入
 的电极为电池的
的电极为电池的 电子转移时,消耗
电子转移时,消耗 的物质的量是
的物质的量是
您最近一年使用:0次
名校
6 . 银锌电池是一种常见化学电源,其反应原理为 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是A. 发生氧化反应 发生氧化反应 | B.电子从 电极经外电路流向 电极经外电路流向 电极 电极 |
C.溶液中 向负极移动 向负极移动 | D. 发生的电极反应式为 发生的电极反应式为 |
您最近一年使用:0次
名校
解题方法
7 . 某兴趣小组想利用原电池的原理判断a、b、c、d四种金属的活动性顺序,具体实验如下:
①将金属a、b用导线连接浸入盛有稀硫酸的烧杯中,电流从b流向a;
②将金属c、b用导线连接浸入CuSO4溶液中,发现c极质量增加;
③将金属a、d用导线连接浸入稀硫酸中,金属d不断溶解。
则四种金属的活动性顺序由强到弱的顺序为
①将金属a、b用导线连接浸入盛有稀硫酸的烧杯中,电流从b流向a;
②将金属c、b用导线连接浸入CuSO4溶液中,发现c极质量增加;
③将金属a、d用导线连接浸入稀硫酸中,金属d不断溶解。
则四种金属的活动性顺序由强到弱的顺序为
A. | B.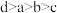 | C.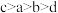 | D.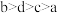 |
您最近一年使用:0次
名校
8 . 回答下列问题:
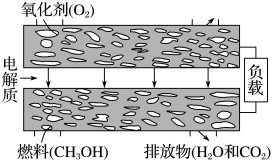
(1)新型固体燃料电池的电解质是体氧化锆和氧化钇,高温下允许氧离子( )在其间通过。如图所示,其中多孔电极不参与电极反应。写出该反应的负极电极反应式:
)在其间通过。如图所示,其中多孔电极不参与电极反应。写出该反应的负极电极反应式:____________ ,当有16g甲醇发生反应时,则理论上提供的电量表达式为______ (1个电子的电量为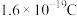 )。
)。____________ ,若过程中产生 ,则消耗标准状况下
,则消耗标准状况下 的体积为
的体积为______ L。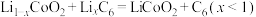 。负极电极反应式:
。负极电极反应式:____________ 。
(4)以 为燃料可以设计甲烷燃料电池,该电池以稀
为燃料可以设计甲烷燃料电池,该电池以稀 作电解质溶液,写出该电池正极电极反应式:
作电解质溶液,写出该电池正极电极反应式:____________ 。
(1)新型固体燃料电池的电解质是体氧化锆和氧化钇,高温下允许氧离子(
 )在其间通过。如图所示,其中多孔电极不参与电极反应。写出该反应的负极电极反应式:
)在其间通过。如图所示,其中多孔电极不参与电极反应。写出该反应的负极电极反应式: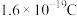 )。
)。
 ,则消耗标准状况下
,则消耗标准状况下 的体积为
的体积为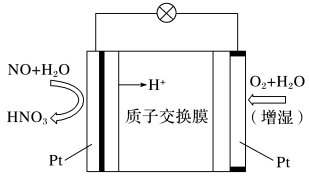
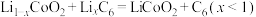 。负极电极反应式:
。负极电极反应式:(4)以
 为燃料可以设计甲烷燃料电池,该电池以稀
为燃料可以设计甲烷燃料电池,该电池以稀 作电解质溶液,写出该电池正极电极反应式:
作电解质溶液,写出该电池正极电极反应式:
您最近一年使用:0次
名校
解题方法
9 . 某原电池装置的总反应为 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是| A.电池工作时负极上发生还原反应 |
| B.可改用Fe做正极材料 |
C.装置工作时,溶液中的 向负极移动 向负极移动 |
| D.装置工作时每转移1mol电子,将消耗64gCu |
您最近一年使用:0次
名校
解题方法
10 . 一种硝酸盐还原制 的装置如图,初始时离子交换膜两侧溶液质量相同,查阅资料得知阴离子交换膜只允许阴离子通过,不允许阳离子和其他分子通过。下列说法正确的是
的装置如图,初始时离子交换膜两侧溶液质量相同,查阅资料得知阴离子交换膜只允许阴离子通过,不允许阳离子和其他分子通过。下列说法正确的是
 的装置如图,初始时离子交换膜两侧溶液质量相同,查阅资料得知阴离子交换膜只允许阴离子通过,不允许阳离子和其他分子通过。下列说法正确的是
的装置如图,初始时离子交换膜两侧溶液质量相同,查阅资料得知阴离子交换膜只允许阴离子通过,不允许阳离子和其他分子通过。下列说法正确的是
A.石墨电极发生的反应为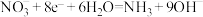 |
B.锌电极表面的电极反应式为 |
C.电路中每转移 的同时有1mol阴离子通过离子交换膜 的同时有1mol阴离子通过离子交换膜 |
| D.电路中转移0.8mol电子时,负极增加26g |
您最近一年使用:0次
2024-03-27更新
|
175次组卷
|
3卷引用:甘肃省白银市2023-2024学年高一下学期期中考试化学试题



