名校
1 . 观察图所示甲乙两个装置图,下列说法错误的是
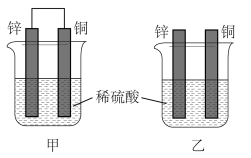
| A.甲为原电池,能将化学能转变为电能,锌为负极 |
| B.甲中电子由锌电极经外电路流向铜电极 |
| C.反应一段时间后,不考虑温度变化,两烧杯中溶液的pH均增大 |
D.两个装置的总反应均为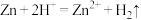 ,当锌溶解了6.5g时,均有2.24L氢气生成 ,当锌溶解了6.5g时,均有2.24L氢气生成 |
您最近一年使用:0次
名校
2 . 回答下列问题
(1)向某体积固定的密闭容器中加入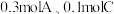 和
和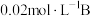 三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。请回答:
三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。请回答:
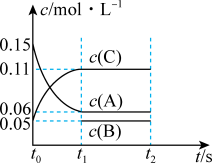
①该密闭容器的体积为_______ 升;若 ,则
,则 内用
内用 表示反应速率
表示反应速率
_______ ;
②写出该反应的化学方程式:_______ 。
③能使该反应的速率增大的是_______ 。
A.及时分离出C气体 B.适当升高温度
C.充入He气增大压强 D.选择高效催化剂
④下列物质表示该反应的化学反应速率最快的是_______ 。
A.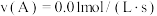
B.
C.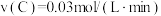
(2)已知断裂几种化学键要吸收的能量如下:
已知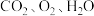 的结构式分别为
的结构式分别为 ,
, ,
, 。
。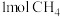 在
在 中完全燃烧生成气态
中完全燃烧生成气态 和气态水时放出
和气态水时放出_______  热量。
热量。
(3)燃料电池是一种高效、环境友好的供电装置,如图为氢气燃料电池的工作原理示意图, 均为惰性电极。
均为惰性电极。

①使用时,氢气从_______ 口通入(填“ ”或“B”)
”或“B”)
② 极的电极反应为:
极的电极反应为:_______ 。
(1)向某体积固定的密闭容器中加入
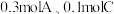 和
和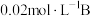 三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。请回答:
三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。请回答:
①该密闭容器的体积为
 ,则
,则 内用
内用 表示反应速率
表示反应速率
②写出该反应的化学方程式:
③能使该反应的速率增大的是
A.及时分离出C气体 B.适当升高温度
C.充入He气增大压强 D.选择高效催化剂
④下列物质表示该反应的化学反应速率最快的是
A.
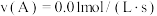
B.

C.
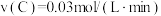
(2)已知断裂几种化学键要吸收的能量如下:
| 化学键 |
|
|
|
|
断裂 键吸收的能量 键吸收的能量 | 415 | 497 | 745 | 463 |
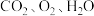 的结构式分别为
的结构式分别为 ,
, ,
, 。
。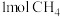 在
在 中完全燃烧生成气态
中完全燃烧生成气态 和气态水时放出
和气态水时放出 热量。
热量。(3)燃料电池是一种高效、环境友好的供电装置,如图为氢气燃料电池的工作原理示意图,
 均为惰性电极。
均为惰性电极。
①使用时,氢气从
 ”或“B”)
”或“B”)②
 极的电极反应为:
极的电极反应为:
您最近一年使用:0次
3 . 如图是锌-铜原电池的示意图,下列说法错误的是


A. 作原电池的负极 作原电池的负极 |
B. 电极上有气泡冒出 电极上有气泡冒出 |
C.溶液中的 向 向 电极方向移动 电极方向移动 |
D.每生成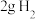 就有 就有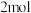 电子从 电子从 经导线流向 经导线流向 再经溶液流回 再经溶液流回 |
您最近一年使用:0次
名校
4 . 现代社会活动需要利用化学反应中的物质和能量变化。
Ⅰ.化学能与热能
下表中的数据是破坏1mol物质中的化学键所消耗的能量,回答下列问题:
(1)以上物质中最不稳定的是___________ 。
(2)按照反应 ,生成2mol HCl
,生成2mol HCl_________ (填“吸收”或“放出”)的热量为_________ kJ。根据能量守恒定律,反应物的总能量应该___________ 其生成物的总能量(填“大于”或“小于”)。
Ⅱ.化学能与电能
(3)把A、B、C、D四种金属按表中装置进行实验。
根据表中信息判断四种金属活动性由大到小的顺序是________________ 。
(4)“乙醇燃料电池”的工作原理为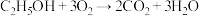 ,装置如图所示。
,装置如图所示。 的移动方向为由
的移动方向为由_______ (填“A到B”或“B到A”)。写出A电极的电极反应式:_____________ 。
②若标况下有11.2L 参与反应,理论上通过质子交换膜的
参与反应,理论上通过质子交换膜的 数目为
数目为_______ 。
Ⅰ.化学能与热能
下表中的数据是破坏1mol物质中的化学键所消耗的能量,回答下列问题:
物质 |
|
|
|
| HCl |
键能/kJ | 243 | 193 | 151 | 436 | 432 |
(1)以上物质中最不稳定的是
(2)按照反应
 ,生成2mol HCl
,生成2mol HClⅡ.化学能与电能
(3)把A、B、C、D四种金属按表中装置进行实验。
装置 |
|
|
|
A表面有气泡 | B电极的质量增加 | 电子由A到D |
(4)“乙醇燃料电池”的工作原理为
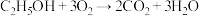 ,装置如图所示。
,装置如图所示。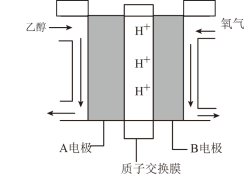
 的移动方向为由
的移动方向为由②若标况下有11.2L
 参与反应,理论上通过质子交换膜的
参与反应,理论上通过质子交换膜的 数目为
数目为
您最近一年使用:0次
名校
解题方法
5 . 以废旧锌锰干电池的炭包(含炭粉、 、
、 和少量
和少量 、
、 等物质)为原料,从中回收
等物质)为原料,从中回收 的工艺流程如下:
的工艺流程如下:
(1)“酸浸”时需将结块的炭包粉碎,目的是_______ 。
(2)“酸浸”过程中, 与稀硝酸反应的离子方程式为
与稀硝酸反应的离子方程式为_______ ,该反应中氧化剂和还原剂的物质的量之比为_______ 。
(3)“溶解”时加入 的作用是
的作用是_______ , 的实际消耗量比理论值高的原因
的实际消耗量比理论值高的原因_______ 。
(4)写出“焙烧”过程的化学反应方程式为_______ 。
(5)碱性锌锰干电池是一种使用广泛的便携式电源,结构如图所示。其电池总反应为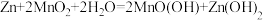 。
。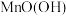 中
中 的化合价为
的化合价为_______ 。
②该电池工作时,负极的反应式为_______ 。
 、
、 和少量
和少量 、
、 等物质)为原料,从中回收
等物质)为原料,从中回收 的工艺流程如下:
的工艺流程如下: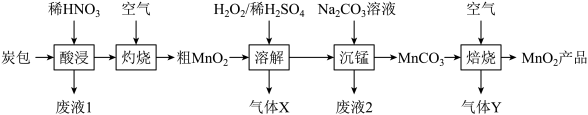
(1)“酸浸”时需将结块的炭包粉碎,目的是
(2)“酸浸”过程中,
 与稀硝酸反应的离子方程式为
与稀硝酸反应的离子方程式为(3)“溶解”时加入
 的作用是
的作用是 的实际消耗量比理论值高的原因
的实际消耗量比理论值高的原因(4)写出“焙烧”过程的化学反应方程式为
(5)碱性锌锰干电池是一种使用广泛的便携式电源,结构如图所示。其电池总反应为
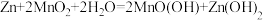 。
。
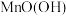 中
中 的化合价为
的化合价为②该电池工作时,负极的反应式为
您最近一年使用:0次
名校
6 . 燃料电池是将燃料和氧化剂(如 )反应所放出的化学能直接转化为电能。下图为
)反应所放出的化学能直接转化为电能。下图为 燃料电池的工作示意图(电极A、B为多孔碳棒)。下列说法正确的是
燃料电池的工作示意图(电极A、B为多孔碳棒)。下列说法正确的是
 )反应所放出的化学能直接转化为电能。下图为
)反应所放出的化学能直接转化为电能。下图为 燃料电池的工作示意图(电极A、B为多孔碳棒)。下列说法正确的是
燃料电池的工作示意图(电极A、B为多孔碳棒)。下列说法正确的是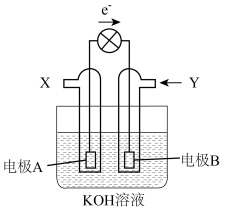
| A.电极A为正极,发生还原反应 |
B.电极B的电极反应式为: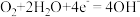 |
C.电子移动方向:电极A→导线→电极B→ 溶液→电极A 溶液→电极A |
| D.电极A附近溶液的碱性增强 |
您最近一年使用:0次
解题方法
7 . NO和NO2都是有毒气体,氨气可作为脱硝剂,如NO和 ,在一定条件下发生反应:6NO(g)+4NH3(g)
,在一定条件下发生反应:6NO(g)+4NH3(g) 5N2(g)+6H2O(g)。
5N2(g)+6H2O(g)。
(1)在恒温恒容的条件下,下列能说明该反应已达到平衡状态的是___________ (填字母)。
a.反应速率
b.容器内压强不再随时间而发生变化
c.容器内N2的物质的量分数不再随时间而发生变化
d.容器内n(NO)∶n(NH3)∶n(N2)∶n(H2O)=6∶4∶5∶6
e.有12molN-H键断裂的同时生成5molN≡N键
f.混合气体的密度不随时间的变化而变化
(2)利用该原理,设计如下原电池,除掉NO的同时,还可以提供电能。
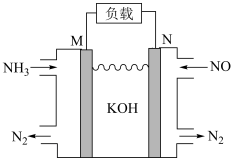
N电极上发生的电极反应为___________ 。
(3)已知拆开1molH-H键、1molN≡N键、1molN-H键需要的能量依次为436kJ、946kJ、391kJ,在该温度下,制备所需NH3时,取1molN2和3molH2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量总小于92kJ(理论消耗1molN2放出92kJ的热量),其原因是___________ 。
(4)一定条件下,在2L密闭容器内,反应2NO2(g) N2O4(g),n(NO2)随时间变化如下表:
N2O4(g),n(NO2)随时间变化如下表:
①用N2O4表示0~2s内该反应的平均速率v(N2O4)=___________ ,在第5s时,NO2的转化率为___________ 。(转化率是指某一反应物转化量占及其总量的百分比)
②根据上表可以看出,随着反应的进行,反应速率逐渐减小,其原因是___________ 。
 ,在一定条件下发生反应:6NO(g)+4NH3(g)
,在一定条件下发生反应:6NO(g)+4NH3(g) 5N2(g)+6H2O(g)。
5N2(g)+6H2O(g)。(1)在恒温恒容的条件下,下列能说明该反应已达到平衡状态的是
a.反应速率

b.容器内压强不再随时间而发生变化
c.容器内N2的物质的量分数不再随时间而发生变化
d.容器内n(NO)∶n(NH3)∶n(N2)∶n(H2O)=6∶4∶5∶6
e.有12molN-H键断裂的同时生成5molN≡N键
f.混合气体的密度不随时间的变化而变化
(2)利用该原理,设计如下原电池,除掉NO的同时,还可以提供电能。

N电极上发生的电极反应为
(3)已知拆开1molH-H键、1molN≡N键、1molN-H键需要的能量依次为436kJ、946kJ、391kJ,在该温度下,制备所需NH3时,取1molN2和3molH2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量总小于92kJ(理论消耗1molN2放出92kJ的热量),其原因是
(4)一定条件下,在2L密闭容器内,反应2NO2(g)
 N2O4(g),n(NO2)随时间变化如下表:
N2O4(g),n(NO2)随时间变化如下表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO2)/mol | 0.040 | 0.0140 | 0.008 | 0.005 | 0.005 | 0.005 |
②根据上表可以看出,随着反应的进行,反应速率逐渐减小,其原因是
您最近一年使用:0次
解题方法
8 . 乙醇燃料电池广泛应用于微型电源、能源汽车、家用电源、国防等领域,工作原理如图所示,电池总反应为: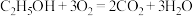 ,下列说法错误的是
,下列说法错误的是

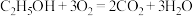 ,下列说法错误的是
,下列说法错误的是
A. 和 和 通入的一极为负极 通入的一极为负极 |
B.正极反应式为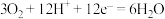 |
C.负极反应式为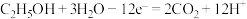 |
D. 从正极经传导质子的固体膜移向负极 从正极经传导质子的固体膜移向负极 |
您最近一年使用:0次
解题方法
9 . I. 可转化成有机物实现碳循环。在体积为1L的恒温恒容密闭容器中,充入
可转化成有机物实现碳循环。在体积为1L的恒温恒容密闭容器中,充入 和
和 ,一定条件下反应:
,一定条件下反应: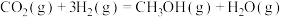 ,测得
,测得 和
和 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。

(1)从3min到9min, =
=___________ 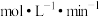 (计算保留2位有效数字)。
(计算保留2位有效数字)。
(2)能说明上述反应达到平衡状态的是___________(填字母)。
(3)平衡时 的转化率为
的转化率为___________ 。
Ⅱ.
(4)如图所示是可逆反应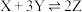 的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是___________(填字母)。
的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是___________(填字母)。

Ⅲ.原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(5)现有如下两个反应:a. ;B.
;B.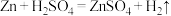 。判断上述两个反应中能设计成原电池的是
。判断上述两个反应中能设计成原电池的是___________ (填“A”或“B”或“AB”)
(6)将纯锌片和纯铜片按图中方式插入100mL相同浓度的稀硫酸中一段时间后,对该装置的有关说法正确的是___________(填序号)。

 可转化成有机物实现碳循环。在体积为1L的恒温恒容密闭容器中,充入
可转化成有机物实现碳循环。在体积为1L的恒温恒容密闭容器中,充入 和
和 ,一定条件下反应:
,一定条件下反应: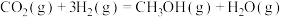 ,测得
,测得 和
和 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。
(1)从3min到9min,
 =
=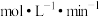 (计算保留2位有效数字)。
(计算保留2位有效数字)。(2)能说明上述反应达到平衡状态的是___________(填字母)。
A.反应中 与 与 的物质的量浓度之比为1:1(即图中交叉点) 的物质的量浓度之比为1:1(即图中交叉点) |
| B.混合气体的压强不随时间的变化而变化 |
C.单位时间内生成 ,同时生成 ,同时生成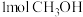 |
| D.混合气体的平均相对分子质量不随时间的变化而变化 |
 的转化率为
的转化率为Ⅱ.
(4)如图所示是可逆反应
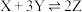 的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是___________(填字母)。
的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是___________(填字母)。
A. 时,只有正方向反应在进行 时,只有正方向反应在进行 | B. 时,反应达到最大限度 时,反应达到最大限度 |
C.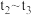 ,反应不再进行 ,反应不再进行 | D.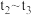 ,各物质的浓度不再发生变化 ,各物质的浓度不再发生变化 |
Ⅲ.原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(5)现有如下两个反应:a.
 ;B.
;B.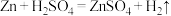 。判断上述两个反应中能设计成原电池的是
。判断上述两个反应中能设计成原电池的是(6)将纯锌片和纯铜片按图中方式插入100mL相同浓度的稀硫酸中一段时间后,对该装置的有关说法正确的是___________(填序号)。

| A.甲、乙均为化学能转变为电能的装置 |
| B.乙中铜片上没有明显变化 |
| C.甲中铜片质量增加、乙中锌片质量减少 |
| D.两烧杯中溶液的pH均增大 |
您最近一年使用:0次
解题方法
10 . 微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理如图所示,下列说法正确的是
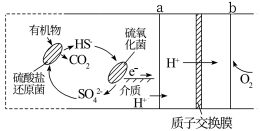

| A.a正极,b为负极 |
| B.电子从电极b流出,经外电路流向电极a |
C. 转化为 转化为 的反应为 的反应为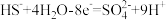 |
D.若该电池中有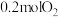 参加反应,则有 参加反应,则有 通过质子交换膜 通过质子交换膜 |
您最近一年使用:0次