名校
解题方法
1 . 科学家利用氧化锆锌作催化剂,在一定温度下将 和
和 转化为重要有机原料甲醇
转化为重要有机原料甲醇 ,其原理为:
,其原理为:
 (即正反应为放热反应)。在容积为
(即正反应为放热反应)。在容积为 的恒温密闭容器中,充入
的恒温密闭容器中,充入 和
和 发生上述反应。
发生上述反应。 和
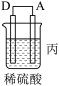
和 的物质的量随时间变化如图所示。回答下列问题:
的物质的量随时间变化如图所示。回答下列问题:
_____ 。
(2)0- 内,
内, 的反应速率为
的反应速率为_______ 。
(3)下列叙述正确的是_______ (填序号)。
a. 时
时 的生成速率等于其分解速率
的生成速率等于其分解速率
b.由 保持不变,可判断该反应达到平衡状态
保持不变,可判断该反应达到平衡状态
c.当 时,该反应一定达到平衡状态
时,该反应一定达到平衡状态
d.当 的体积分数不再变化,可判断该反应达到平衡状态
的体积分数不再变化,可判断该反应达到平衡状态
(4)该温度下达到平衡时,混合气体中 的体积分数为
的体积分数为________ ,此时体系压强与开始时的压强之比为_____ 。
(5)其他条件不变时,下列措施不能使生成 的反应速率增大的是
的反应速率增大的是_______ (填序号)。
a.增大 的浓度 b.将容器的容积变为
的浓度 b.将容器的容积变为
c.恒容条件下充入一定量 d.将恒温恒容容器改为绝热恒容容器
d.将恒温恒容容器改为绝热恒容容器
(6)已知升高温度,平衡向吸热方向移动。降低温度,此反应再次达到平衡时体系中混合气体的平均摩尔质量____ (填“增大”“减小”或“不变”)。
(7) 燃料电池的工作原理如图所示,a、b均为铂电极, A、B为燃料或氧气入口。
燃料电池的工作原理如图所示,a、b均为铂电极, A、B为燃料或氧气入口。____ 。
 和
和 转化为重要有机原料甲醇
转化为重要有机原料甲醇 ,其原理为:
,其原理为:
 (即正反应为放热反应)。在容积为
(即正反应为放热反应)。在容积为 的恒温密闭容器中,充入
的恒温密闭容器中,充入 和
和 发生上述反应。
发生上述反应。 和
和 的物质的量随时间变化如图所示。回答下列问题:
的物质的量随时间变化如图所示。回答下列问题:

(2)0-
 内,
内, 的反应速率为
的反应速率为(3)下列叙述正确的是
a.
 时
时 的生成速率等于其分解速率
的生成速率等于其分解速率b.由
 保持不变,可判断该反应达到平衡状态
保持不变,可判断该反应达到平衡状态c.当
 时,该反应一定达到平衡状态
时,该反应一定达到平衡状态d.当
 的体积分数不再变化,可判断该反应达到平衡状态
的体积分数不再变化,可判断该反应达到平衡状态(4)该温度下达到平衡时,混合气体中
 的体积分数为
的体积分数为(5)其他条件不变时,下列措施不能使生成
 的反应速率增大的是
的反应速率增大的是a.增大
 的浓度 b.将容器的容积变为
的浓度 b.将容器的容积变为
c.恒容条件下充入一定量
 d.将恒温恒容容器改为绝热恒容容器
d.将恒温恒容容器改为绝热恒容容器(6)已知升高温度,平衡向吸热方向移动。降低温度,此反应再次达到平衡时体系中混合气体的平均摩尔质量
(7)
 燃料电池的工作原理如图所示,a、b均为铂电极, A、B为燃料或氧气入口。
燃料电池的工作原理如图所示,a、b均为铂电极, A、B为燃料或氧气入口。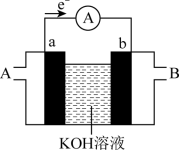
您最近一年使用:0次
名校
2 . 关于如图所示装置的叙述,不正确的是
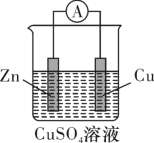
| A.该装置能将化学能转化为电能 |
| B.锌是负极,锌片质量逐渐减小 |
C.电子的移动方向:  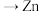 |
D.原电池发生的总反应为 |
您最近一年使用:0次
7日内更新
|
114次组卷
|
2卷引用:湖南省岳阳市平江县第三中学等多校联考2023年高一普通高中学业水平合格性考试仿真模拟(专家卷一)化学试题
名校
解题方法
3 . 某小组按如下步骤探究二氧化硫与铜单质、Cu2+的反应:
ⅰ.按图示连接好装置。
ⅲ.关闭活塞b,打开活塞a.光亮的紫红色铜片很快变暗,并有黑色的Cu2S生成,同时溶液变为棕色,此时溶液中的铜元素以[CuCl3]2-(棕黄色)的形式存在。
ⅳ.静置后,取上层棕色的清液于试管中,加入一定量蒸馏水稀释,溶液中有白色沉淀CuCl析出。
(1)装置A中发生反应的化学方程式为___________ ,该反应中硫酸体现出的化学性质为___________ ;装置C的作用是___________ ,试剂m可选择___________ (填标号)。
a.饱和NaCl溶液 b.浓硫酸 c.NaOH浓溶液
(2)步骤ⅲ中,SO2在盐酸中与Cu反应的离子方程式为___________ ;步骤ⅳ中发生反应的离子方程式为[CuCl3]2-⇌CuCl↓+2Cl-,下列有关该反应的说法正确的是___________ (填标号)。
A.该反应中有电子的转移
B.反应经过足够长的时间后,[CuCl3]2-中的Cu元素能全部沉淀
C.溶液中,[CuCl3]2-和Cl-能同时存在
D.其他条件不变,当溶液的颜色不再改变时,表明该反应在该条件下达到最大限度
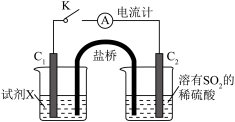
(3)在通风橱中利用如下装置进一步探究SO2与Cu2+的反应,盐桥(内有琼脂和饱和氯化钾溶液)用于连接两电极的电解质溶液。实验②中,闭合K后,C2电极上发生的电极反应为___________ ;不考虑其他副反应及Cu2+进入盐桥,实验②中,电路中转移0.02mole-时,左侧烧杯溶液中Cu2+的质量减少___________ g。
ⅰ.按图示连接好装置。
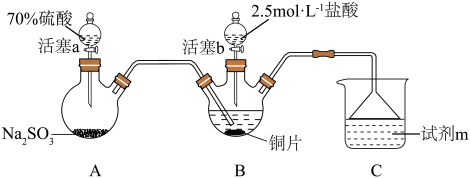
ⅲ.关闭活塞b,打开活塞a.光亮的紫红色铜片很快变暗,并有黑色的Cu2S生成,同时溶液变为棕色,此时溶液中的铜元素以[CuCl3]2-(棕黄色)的形式存在。
ⅳ.静置后,取上层棕色的清液于试管中,加入一定量蒸馏水稀释,溶液中有白色沉淀CuCl析出。
(1)装置A中发生反应的化学方程式为
a.饱和NaCl溶液 b.浓硫酸 c.NaOH浓溶液
(2)步骤ⅲ中,SO2在盐酸中与Cu反应的离子方程式为
A.该反应中有电子的转移
B.反应经过足够长的时间后,[CuCl3]2-中的Cu元素能全部沉淀
C.溶液中,[CuCl3]2-和Cl-能同时存在
D.其他条件不变,当溶液的颜色不再改变时,表明该反应在该条件下达到最大限度
(3)在通风橱中利用如下装置进一步探究SO2与Cu2+的反应,盐桥(内有琼脂和饱和氯化钾溶液)用于连接两电极的电解质溶液。实验②中,闭合K后,C2电极上发生的电极反应为
| 实验装置图 |
| ||
| 序号 | 试剂X | 实验现象 | |
| 电流计 | C1附近溶液 | ||
| ① | 0.1mol·L-1CuSO4溶液 | 指针几乎不偏转 | 无明显现象 |
| ② | 0.1mol·L-1NaCl和0.1mol·L-1CuSO4的混合溶液(足量) | 指针明显偏转 | 溶液变棕黄色 |
您最近一年使用:0次
名校
4 . 石家庄二中实验学校某化学兴趣小组设计了一个如图所示的水果电池,下列有关该电池的说法正确的是
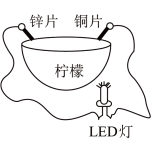
| A.锌片作正极 |
| B.电子流向:锌片→导线→LED灯→铜片→柠檬→锌片 |
| C.铜片上发生还原反应,质量一定增加 |
| D.水果种类会影响LED灯的亮度 |
您最近一年使用:0次
名校
解题方法
5 . 回答下列问题。
(1)理论上不能设计为原电池的化学反应是___________ 。
a.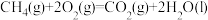
b.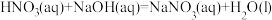
c.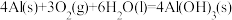
d.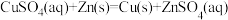
(2)某小组为探究 与
与 能否发生氧化还原反应,设计如下图所示双液原电池(盐桥中为饱和
能否发生氧化还原反应,设计如下图所示双液原电池(盐桥中为饱和 溶液的琼脂)。该装置石墨棒上发生的电极反应式为
溶液的琼脂)。该装置石墨棒上发生的电极反应式为___________ ,盐桥中 向
向___________ 烧杯移动(填“甲”或“乙”)。___________ ,B电极的电极反应方程式为___________ 。 为电解质。工作时负极的电极反应式
为电解质。工作时负极的电极反应式___________ 。
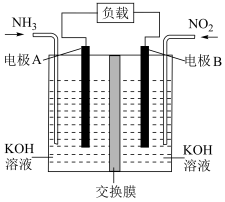
(5)汽车尾气中含有的 是造成城市空气污染的主要因素之一,通过
是造成城市空气污染的主要因素之一,通过 传感器可监测汽车尾气史
传感器可监测汽车尾气史 含量,其工作原理如图所示:
含量,其工作原理如图所示: 电极为
电极为___________ (填“正极”或“负极), 电极上发生的电极反应式为
电极上发生的电极反应式为___________ 。
(1)理论上不能设计为原电池的化学反应是
a.
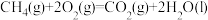
b.
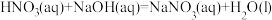
c.
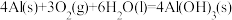
d.
(2)某小组为探究
 与
与 能否发生氧化还原反应,设计如下图所示双液原电池(盐桥中为饱和
能否发生氧化还原反应,设计如下图所示双液原电池(盐桥中为饱和 溶液的琼脂)。该装置石墨棒上发生的电极反应式为
溶液的琼脂)。该装置石墨棒上发生的电极反应式为 向
向
 为电解质。工作时负极的电极反应式
为电解质。工作时负极的电极反应式(5)汽车尾气中含有的
 是造成城市空气污染的主要因素之一,通过
是造成城市空气污染的主要因素之一,通过 传感器可监测汽车尾气史
传感器可监测汽车尾气史 含量,其工作原理如图所示:
含量,其工作原理如图所示:
 电极为
电极为 电极上发生的电极反应式为
电极上发生的电极反应式为
您最近一年使用:0次
6 . 能量、速率与限度是认识和研究化学反应的重要视角。
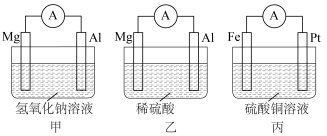
Ⅰ.为了探究原电池的工作原理,设计如下装置。________ 。
(2)当乙装置中的负极质量减少1.8g时,正极产生气体________ L(标准状况下); 向
向________ (填“Mg”或“Al”)电极移动。
Ⅱ. 、
、 都是重要的能源物质,也是重要的化工原料。利用
都是重要的能源物质,也是重要的化工原料。利用 还原
还原 能有效促进“碳中和”,反应的化学方程式为
能有效促进“碳中和”,反应的化学方程式为 。
。
(3)反应过程中的能量变化如图所示:________ (填“放热”或“吸热”)反应。
(4)300℃时,向容积为2L的恒容密闭容器中,充入 和
和 ,反应过程中测得各物质的物质的量浓度随时间变化如图所示。回答下列问题:
,反应过程中测得各物质的物质的量浓度随时间变化如图所示。回答下列问题: 的浓度随时间变化曲线为
的浓度随时间变化曲线为________ (填“a”、“b”或“c”);在M点,
________  (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
②2min时,反应速率改变的原因可能是________ 。
A.升高温度 B.降低温度 C.充入一定量的 D.加入催化剂
D.加入催化剂
③下列叙述不能说明该反应达到平衡状态的是________ 。
A.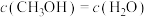
B.混合气体的密度不再变化
C.混合气体的平均摩尔质量不再变化
D.单位时间内生成 ,同时消耗
,同时消耗
Ⅰ.为了探究原电池的工作原理,设计如下装置。
(2)当乙装置中的负极质量减少1.8g时,正极产生气体
 向
向Ⅱ.
 、
、 都是重要的能源物质,也是重要的化工原料。利用
都是重要的能源物质,也是重要的化工原料。利用 还原
还原 能有效促进“碳中和”,反应的化学方程式为
能有效促进“碳中和”,反应的化学方程式为 。
。(3)反应过程中的能量变化如图所示:

(4)300℃时,向容积为2L的恒容密闭容器中,充入
 和
和 ,反应过程中测得各物质的物质的量浓度随时间变化如图所示。回答下列问题:
,反应过程中测得各物质的物质的量浓度随时间变化如图所示。回答下列问题: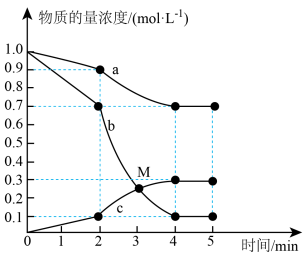
 的浓度随时间变化曲线为
的浓度随时间变化曲线为
 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。②2min时,反应速率改变的原因可能是
A.升高温度 B.降低温度 C.充入一定量的
 D.加入催化剂
D.加入催化剂③下列叙述不能说明该反应达到平衡状态的是
A.
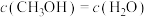
B.混合气体的密度不再变化
C.混合气体的平均摩尔质量不再变化
D.单位时间内生成
 ,同时消耗
,同时消耗
您最近一年使用:0次
7 . 某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图示:________ 。
(2)若上述反应中X、Y、Z分别为 、
、 、
、 ,某温度下,在容积恒定为2.0L的密闭容器中充入
,某温度下,在容积恒定为2.0L的密闭容器中充入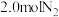 和
和 ,一段时间后反应达平衡状态,实验数据如表所示:
,一段时间后反应达平衡状态,实验数据如表所示:
0~50s内的平均反应速率
________ 。
(3)已知:键能指在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g)、B(g)所需的能量,用符号E表示,单位为kJ/mol。H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,生成 过程中放出46kJ的热量。则N≡N的键能为
过程中放出46kJ的热量。则N≡N的键能为________ kJ/mol。
(4)CO与 反应可制备
反应可制备 ,由
,由 和
和 构成的质子交换膜燃料电池的结构示意图如下。
构成的质子交换膜燃料电池的结构示意图如下。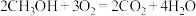 ,则c电极是
,则c电极是________ (填“正极”或“负极”)。若外电路中转移2mol电子,则上述燃料电池所消耗的 在标准状况下的体积为
在标准状况下的体积为________ L。
(5)下列反应中,属于吸热反应的是________ (填序号)
①物质燃烧 ②炸药爆炸 ③酸碱中和反应 ④二氧化碳通过炽热的碳 ⑤食物因氧化而腐败
⑥ 与
与 反应 ⑦铁粉与稀盐酸反应
反应 ⑦铁粉与稀盐酸反应

(2)若上述反应中X、Y、Z分别为
 、
、 、
、 ,某温度下,在容积恒定为2.0L的密闭容器中充入
,某温度下,在容积恒定为2.0L的密闭容器中充入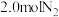 和
和 ,一段时间后反应达平衡状态,实验数据如表所示:
,一段时间后反应达平衡状态,实验数据如表所示:t/s | 0 | 50 | 150 | 250 | 350 |
| 0 | 0.36 | 0.48 | 0.50 | 0.50 |

(3)已知:键能指在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g)、B(g)所需的能量,用符号E表示,单位为kJ/mol。H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,生成
 过程中放出46kJ的热量。则N≡N的键能为
过程中放出46kJ的热量。则N≡N的键能为(4)CO与
 反应可制备
反应可制备 ,由
,由 和
和 构成的质子交换膜燃料电池的结构示意图如下。
构成的质子交换膜燃料电池的结构示意图如下。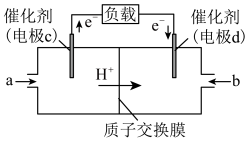
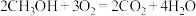 ,则c电极是
,则c电极是 在标准状况下的体积为
在标准状况下的体积为(5)下列反应中,属于吸热反应的是
①物质燃烧 ②炸药爆炸 ③酸碱中和反应 ④二氧化碳通过炽热的碳 ⑤食物因氧化而腐败
⑥
 与
与 反应 ⑦铁粉与稀盐酸反应
反应 ⑦铁粉与稀盐酸反应
您最近一年使用:0次
名校
8 . 观察图所示甲乙两个装置图,下列说法错误的是
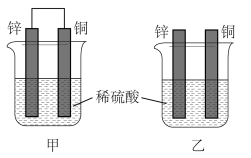
| A.甲为原电池,能将化学能转变为电能,锌为负极 |
| B.甲中电子由锌电极经外电路流向铜电极 |
| C.反应一段时间后,不考虑温度变化,两烧杯中溶液的pH均增大 |
D.两个装置的总反应均为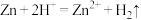 ,当锌溶解了6.5g时,均有2.24L氢气生成 ,当锌溶解了6.5g时,均有2.24L氢气生成 |
您最近一年使用:0次
名校
9 . 现代社会活动需要利用化学反应中的物质和能量变化。
Ⅰ.化学能与热能
下表中的数据是破坏1mol物质中的化学键所消耗的能量,回答下列问题:
(1)以上物质中最不稳定的是___________ 。
(2)按照反应 ,生成2mol HCl
,生成2mol HCl_________ (填“吸收”或“放出”)的热量为_________ kJ。根据能量守恒定律,反应物的总能量应该___________ 其生成物的总能量(填“大于”或“小于”)。
Ⅱ.化学能与电能
(3)把A、B、C、D四种金属按表中装置进行实验。
根据表中信息判断四种金属活动性由大到小的顺序是________________ 。
(4)“乙醇燃料电池”的工作原理为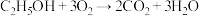 ,装置如图所示。
,装置如图所示。 的移动方向为由
的移动方向为由_______ (填“A到B”或“B到A”)。写出A电极的电极反应式:_____________ 。
②若标况下有11.2L 参与反应,理论上通过质子交换膜的
参与反应,理论上通过质子交换膜的 数目为
数目为_______ 。
Ⅰ.化学能与热能
下表中的数据是破坏1mol物质中的化学键所消耗的能量,回答下列问题:
物质 |
|
|
|
| HCl |
键能/kJ | 243 | 193 | 151 | 436 | 432 |
(1)以上物质中最不稳定的是
(2)按照反应
 ,生成2mol HCl
,生成2mol HClⅡ.化学能与电能
(3)把A、B、C、D四种金属按表中装置进行实验。
装置 |
|
|
|
A表面有气泡 | B电极的质量增加 | 电子由A到D |
(4)“乙醇燃料电池”的工作原理为
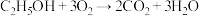 ,装置如图所示。
,装置如图所示。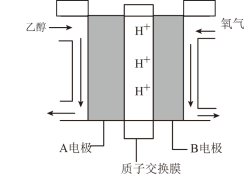
 的移动方向为由
的移动方向为由②若标况下有11.2L
 参与反应,理论上通过质子交换膜的
参与反应,理论上通过质子交换膜的 数目为
数目为
您最近一年使用:0次
10 . 关于原电池原理示意图错误的是
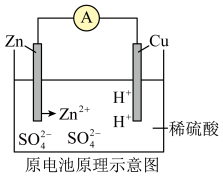
| A.锌片溶解 | B.铜得到电子,被还原 |
| C.锌失去电子,被氧化 | D.电子从锌片经导线流向铜片 |
您最近一年使用:0次