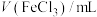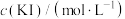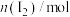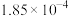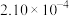名校
1 . 汽车的启动电源常用铅酸蓄电池,其结构如下图所示。放电时的电池反应: 。下列说法中,不正确的是
。下列说法中,不正确的是
 。下列说法中,不正确的是
。下列说法中,不正确的是
A. 得电子,被还原 得电子,被还原 |
| B.Pb作电池的负极 |
C.负极的电极反应为: |
| D.电池放电时,溶液酸性增强 |
您最近一年使用:0次
名校
解题方法
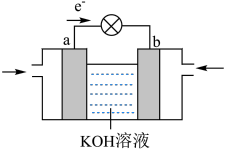
2 . 甲烷燃料电池的工作原理如图所示,下列说法正确的是
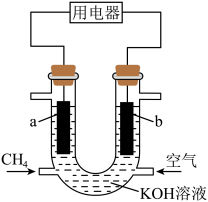
| A.a极为正极 |
B.a极的电极反应式为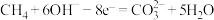 |
| C.K+从a极区经溶液流向b极区 |
| D.工作一段时间后,b极附近的pH会减小 |
您最近一年使用:0次
名校
3 . 化学反应同时伴随着能量变化,是人类获取能量的重要途径。以下是常见的化学反应,回答(1)和(2)。 晶体与
晶体与 晶体反应
晶体反应
c.氢氧化钠与盐酸反应 d.盐酸与碳酸氢钠反应
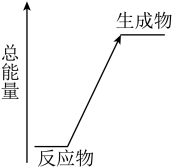
(1)以上化学反应中能用上图表示其能量变化的是______ (填字母),此类反应中有能量变化的原因是:断开反应物的化学键吸收的总能量______ (填“>”或“<”)形成生成物的化学键释放的总能量。
(2)从以上反应中选择一个反应设计原电池。
①将如图原电池装置补充完整______ 。
②证实化学能转化为电能的实验现象是______ .
③正极的电极反应式是______ .______ .
(4) 还原
还原 电化学法制备
电化学法制备 (甲醇)的工作原理如图所示。通入
(甲醇)的工作原理如图所示。通入 的一端是电池的
的一端是电池的______ 极(填“正”或“负”),通入 的一端发生的电极反应式为
的一端发生的电极反应式为______ 。生成 甲醇时,转移
甲醇时,转移______  电子。
电子。
 晶体与
晶体与 晶体反应
晶体反应c.氢氧化钠与盐酸反应 d.盐酸与碳酸氢钠反应
(1)以上化学反应中能用上图表示其能量变化的是
(2)从以上反应中选择一个反应设计原电池。
①将如图原电池装置补充完整
②证实化学能转化为电能的实验现象是
③正极的电极反应式是
(4)
 还原
还原 电化学法制备
电化学法制备 (甲醇)的工作原理如图所示。通入
(甲醇)的工作原理如图所示。通入 的一端是电池的
的一端是电池的 的一端发生的电极反应式为
的一端发生的电极反应式为 甲醇时,转移
甲醇时,转移 电子。
电子。
您最近一年使用:0次
名校
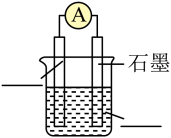
4 . 锌-空气电池(原理如图)适宜用作城市电动车的动力电源。该电池放电时 转化为
转化为 。该电池工作时,下列说法不正确的是
。该电池工作时,下列说法不正确的是
 转化为
转化为 。该电池工作时,下列说法不正确的是
。该电池工作时,下列说法不正确的是
A. 是该电池的负极 是该电池的负极 |
B.石墨电极的电极反应: |
C. 向石墨电极移动 向石墨电极移动 |
D.电子由 极流出到石墨电极,再经溶液回到 极流出到石墨电极,再经溶液回到 极,形成回路 极,形成回路 |
您最近一年使用:0次
5 . 一定温度下,在2L的密闭容器中,M、N两种气体的物质的量随时间变化的曲线如图所示:_______ 。
(2)反应达到化学平衡时,化学反应速率
______ ,N的转化率为______ 。
(3)下列可作为判断该反应达到平衡状态的依据是_______。
(4)能加快反应速率的措施是_____。
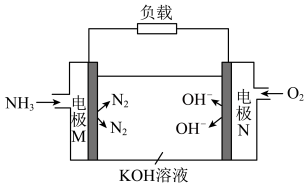
(5)潜艇中使用的液氨—液氧燃料电池工作原理如图所示: 离子向
离子向_____ (填“电极a”或“电极b”)移动。
②电极a的电极反应式为_____ 。
③可通过 与
与 反应来制得火箭燃料肼(
反应来制得火箭燃料肼( )。该反应的化学反应方程式是
)。该反应的化学反应方程式是_____ 。

(2)反应达到化学平衡时,化学反应速率

(3)下列可作为判断该反应达到平衡状态的依据是_______。
| A.该条件下,正、逆反应速率都为零 |
| B.该条件下,混合气体的密度不再发生变化 |
| C.该条件下,混合气体的压强不再发生变化 |
D.该条件下,单位时间内消耗 的同时,消耗 的同时,消耗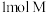 |
(4)能加快反应速率的措施是_____。
| A.升高温度 | B.容器容积不变,充入惰性气体 |
C.容器压强不变,充入惰性气体 | D.使用催化剂 |
(5)潜艇中使用的液氨—液氧燃料电池工作原理如图所示:

 离子向
离子向②电极a的电极反应式为
③可通过
 与
与 反应来制得火箭燃料肼(
反应来制得火箭燃料肼( )。该反应的化学反应方程式是
)。该反应的化学反应方程式是
您最近一年使用:0次
名校
6 . 煤化工产品在工业领域中有广泛的应用前景。
I.煤的气化有助于得到更清洁的燃料和化工产品。煤与水蒸气生产水煤气的化学方程式为: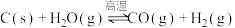 ,反应的能量变化如图所示:
,反应的能量变化如图所示:___________ (填“吸热反应”或“放热反应”)
(2)在体积固定的密闭容器中发生上述反应,下列措施能加快反应速率的是___________(填序号)
Ⅱ.二甲醚( )是一种重要的精细化工产品,利用水煤气可以直接合成二甲醚。一定温度下,在
)是一种重要的精细化工产品,利用水煤气可以直接合成二甲醚。一定温度下,在 的密闭容器中,CO、和产物
的密闭容器中,CO、和产物 (部分产物未标出)的物质的量随时间变化的曲线如图所示:
(部分产物未标出)的物质的量随时间变化的曲线如图所示: 反应生成二甲醚的化学方程式
反应生成二甲醚的化学方程式___________ 。
(4)从反应开始到 ,用CO表示的反应速率为
,用CO表示的反应速率为___________ (填字母)。
(5)在体积固定的密闭容器中发生上述反应,能说明反应达到平衡状态的是___________。
Ⅲ.可将二甲醚设计成燃料电池。图为某二甲醚燃料电池的工作原理示意图。a、b均为多孔性Pt电极。请填空:___________ (填“正”或“负”)极。
(7)b电极上反应为___________ 。
I.煤的气化有助于得到更清洁的燃料和化工产品。煤与水蒸气生产水煤气的化学方程式为:
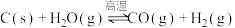 ,反应的能量变化如图所示:
,反应的能量变化如图所示:
(2)在体积固定的密闭容器中发生上述反应,下列措施能加快反应速率的是___________(填序号)
| A.充入氩气增大压强 | B.加入固体碳 | C.增大水蒸气浓度 | D.分离CO |
Ⅱ.二甲醚(
 )是一种重要的精细化工产品,利用水煤气可以直接合成二甲醚。一定温度下,在
)是一种重要的精细化工产品,利用水煤气可以直接合成二甲醚。一定温度下,在 的密闭容器中,CO、和产物
的密闭容器中,CO、和产物 (部分产物未标出)的物质的量随时间变化的曲线如图所示:
(部分产物未标出)的物质的量随时间变化的曲线如图所示:
 反应生成二甲醚的化学方程式
反应生成二甲醚的化学方程式(4)从反应开始到
 ,用CO表示的反应速率为
,用CO表示的反应速率为(5)在体积固定的密闭容器中发生上述反应,能说明反应达到平衡状态的是___________。
| A.CO的含量保持不变 | B.混合气体的密度不变 |
| C.混合气体的平均相对分子质量不变 | D.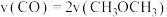 |
Ⅲ.可将二甲醚设计成燃料电池。图为某二甲醚燃料电池的工作原理示意图。a、b均为多孔性Pt电极。请填空:

(7)b电极上反应为
您最近一年使用:0次
名校
7 . 汽车尾气中含有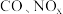 等有害气体。
等有害气体。
(1) 能形成酸雨,写出
能形成酸雨,写出 转化为
转化为 的化学方程式:
的化学方程式:______ .
(2)汽车尾气中 生成过程的能量变化示意图如下:
生成过程的能量变化示意图如下:____________ .
(3)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示: 电极上发生的是
电极上发生的是______ 反应(填“氧化”或“还原”)。
②外电路中,电子的流动方向是从______ 电极流出(填 或Pt);Pt电极上的电极反应式为
或Pt);Pt电极上的电极反应式为______ .
(4)一种新型催化剂能使 和
和 发生反应:
发生反应: 。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下表中。
。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下表中。
①请将表中数据补充完整:A______ ;B______ .
②能验证温度对化学反应速率影响规律的实验是______ (填实验编号)。
③实验Ⅰ和实验Ⅱ中,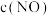 随时间
随时间 的变化曲线如图所示,其中表示实验Ⅱ的曲线是
的变化曲线如图所示,其中表示实验Ⅱ的曲线是______ (填“甲”或“乙”)。 。一定温度下,在容积不变的密闭容器中,下列可以说明该反应达到平衡状态的是
。一定温度下,在容积不变的密闭容器中,下列可以说明该反应达到平衡状态的是______ 。(从A-D项中选择)
A.容器内 的质量分数不再变化。
的质量分数不再变化。
B.相同时间内,消耗 同时生成
同时生成
C.容器内压强不再变化
D.容器内气体的平均密度不再发生变化
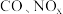 等有害气体。
等有害气体。(1)
 能形成酸雨,写出
能形成酸雨,写出 转化为
转化为 的化学方程式:
的化学方程式:(2)汽车尾气中
 生成过程的能量变化示意图如下:
生成过程的能量变化示意图如下:
(3)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示:

 电极上发生的是
电极上发生的是②外电路中,电子的流动方向是从
 或Pt);Pt电极上的电极反应式为
或Pt);Pt电极上的电极反应式为(4)一种新型催化剂能使
 和
和 发生反应:
发生反应: 。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下表中。
。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下表中。| 实验编号 | 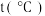 |  初始浓度 初始浓度 |  初始浓度 初始浓度 | 催化剂的比表面积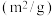 |
| Ⅰ | 280 |  |  | 82 |
| Ⅱ | 280 |  |  | 124 |
| Ⅲ | 350 |  |  | 82 |
②能验证温度对化学反应速率影响规律的实验是
③实验Ⅰ和实验Ⅱ中,
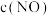 随时间
随时间 的变化曲线如图所示,其中表示实验Ⅱ的曲线是
的变化曲线如图所示,其中表示实验Ⅱ的曲线是
 。一定温度下,在容积不变的密闭容器中,下列可以说明该反应达到平衡状态的是
。一定温度下,在容积不变的密闭容器中,下列可以说明该反应达到平衡状态的是A.容器内
 的质量分数不再变化。
的质量分数不再变化。B.相同时间内,消耗
 同时生成
同时生成
C.容器内压强不再变化
D.容器内气体的平均密度不再发生变化
您最近一年使用:0次
名校
解题方法
8 . 氯化铁溶液与碘化钾溶液反应是高中阶段常见的氧化还原反应且反应现象较为明显,某实验小组通过实验探究发现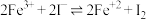 为可逆反应。已知
为可逆反应。已知 是一种常见的溶剂,与水互不相溶,碘单质在该溶剂中溶解后溶液呈紫红色。回答下列问题:
是一种常见的溶剂,与水互不相溶,碘单质在该溶剂中溶解后溶液呈紫红色。回答下列问题:
(1)已知该反应的能量变化如下图所示,则该反应为________ (填“吸热”或“放热”)反应。
(3)为了证实氯化铁与碘化钾反应为可逆反应,该实验小组还设计了如下实验方案:取少量氯化铁溶液于试管中,再往试管中加入过量的等物质的量浓度的碘化钾溶液,充分反应后加入适量的 振荡且静置,发现下层形成了紫红色的溶液,若要证明该反应存在限度,请补充实验操作及现象:
振荡且静置,发现下层形成了紫红色的溶液,若要证明该反应存在限度,请补充实验操作及现象:__________ 。
(4)为了探究在可逆反应中增大某种反应物的浓度是否能提高生成物的产量,在一定温度下,该实验小组通过测定相同时间t min内产生I2的量来进行验证,实验记录如下表,混合后溶液体积变化忽略不计:
①利用实验Ⅰ的数据,计算该反应在0~t min FeCl3的平均反应速率为________  。
。
②利用表格数据计算t min时实验Ⅱ中 的转化率为
的转化率为________ %。
(5)若将 的正反应设计为原电池,用石墨作电极材料,其中,正极发生
的正反应设计为原电池,用石墨作电极材料,其中,正极发生________ 反应(填“氧化”或“还原”),负极电极反应式为________________ 。
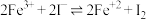 为可逆反应。已知
为可逆反应。已知 是一种常见的溶剂,与水互不相溶,碘单质在该溶剂中溶解后溶液呈紫红色。回答下列问题:
是一种常见的溶剂,与水互不相溶,碘单质在该溶剂中溶解后溶液呈紫红色。回答下列问题:(1)已知该反应的能量变化如下图所示,则该反应为
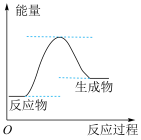
| A.氧化钙与水反应 | B.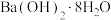 晶体和NH4Cl晶体反应 晶体和NH4Cl晶体反应 |
| C.碳酸氢钠与盐酸反应 | D.甲烷在氧气中燃烧 |
(3)为了证实氯化铁与碘化钾反应为可逆反应,该实验小组还设计了如下实验方案:取少量氯化铁溶液于试管中,再往试管中加入过量的等物质的量浓度的碘化钾溶液,充分反应后加入适量的
 振荡且静置,发现下层形成了紫红色的溶液,若要证明该反应存在限度,请补充实验操作及现象:
振荡且静置,发现下层形成了紫红色的溶液,若要证明该反应存在限度,请补充实验操作及现象:(4)为了探究在可逆反应中增大某种反应物的浓度是否能提高生成物的产量,在一定温度下,该实验小组通过测定相同时间t min内产生I2的量来进行验证,实验记录如下表,混合后溶液体积变化忽略不计:
实验编号 |
|
|
|
|
|
Ⅰ | 0.1 | 5 | 0.1 | 5 |
|
Ⅱ | 0.2 | 5 | 0.1 | 5 |
|
Ⅲ | 0.3 | 5 | 0.1 | 5 |
|
 。
。②利用表格数据计算t min时实验Ⅱ中
 的转化率为
的转化率为(5)若将
 的正反应设计为原电池,用石墨作电极材料,其中,正极发生
的正反应设计为原电池,用石墨作电极材料,其中,正极发生
您最近一年使用:0次
名校
解题方法
9 . 研究化学能与热能、电能的转化具有重要价值。回答下列问题:
(1)下列化学反应过程中的能量变化符合图示的是___________ (填序号)。
①酸碱中和反应 ②碳酸钙分解 ③金属钠与水反应 ④酒精燃烧 ⑤灼热的碳与二氧化碳反应 ⑥ 与
与 反应
反应 的反应过程如图所示:
的反应过程如图所示: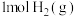 和
和 充分反应,则反应物中旧键断裂共吸收
充分反应,则反应物中旧键断裂共吸收___________ kJ能量,生成物中新键形成共放出___________ kJ能量,该反应为___________ (填“吸热”或“放热”)反应。
原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(3)现有如下两个反应:A ;B.
;B.  ,判断上述两个反应中能设计成原电池的是
,判断上述两个反应中能设计成原电池的是___________ (填“A”或“B”)。
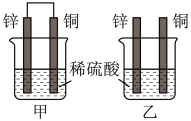
(4)将纯锌片和纯铜片按图中方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:___________ 。
A 甲、乙均为化学能转变为电能的装置 B. 乙中铜片上没有明显变化
C. 甲中铜片质量减少、乙中锌片质量减少 D. 两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲___________ 乙(填“>”“<”或“=”)。
③请写出图中构成原电池的负极电极反应式:___________ 。
(5)若利用反应 设计一个原电池,请完善实验装置,负极材料:
设计一个原电池,请完善实验装置,负极材料:___________ ;正极材料:___________ ;电解质溶液:___________ 。
__________________ ___________ 。
(1)下列化学反应过程中的能量变化符合图示的是
①酸碱中和反应 ②碳酸钙分解 ③金属钠与水反应 ④酒精燃烧 ⑤灼热的碳与二氧化碳反应 ⑥
 与
与 反应
反应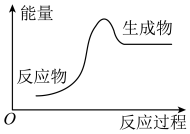
 的反应过程如图所示:
的反应过程如图所示: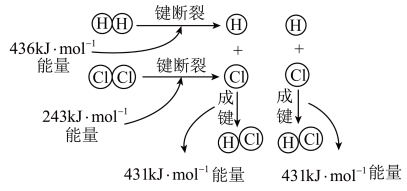
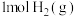 和
和 充分反应,则反应物中旧键断裂共吸收
充分反应,则反应物中旧键断裂共吸收原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(3)现有如下两个反应:A
 ;B.
;B.  ,判断上述两个反应中能设计成原电池的是
,判断上述两个反应中能设计成原电池的是(4)将纯锌片和纯铜片按图中方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:
A 甲、乙均为化学能转变为电能的装置 B. 乙中铜片上没有明显变化
C. 甲中铜片质量减少、乙中锌片质量减少 D. 两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲
③请写出图中构成原电池的负极电极反应式:
(5)若利用反应
 设计一个原电池,请完善实验装置,负极材料:
设计一个原电池,请完善实验装置,负极材料: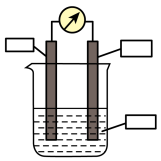
您最近一年使用:0次
名校
解题方法
10 . 如图所示装置中,可观察到检流计指针偏转,M棒变细,N棒变粗。下列说法正确的是
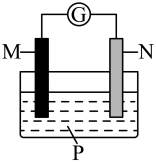
| A.M为Zn、N为Cu、P为稀硫酸,M为负极 |
B.M为Fe、N为石墨、P为 溶液, 溶液, 移向M极 移向M极 |
C.M为Fe、N为石墨、P为 溶液,电子由N沿导线流向M 溶液,电子由N沿导线流向M |
D.M为Cu、N为Fe、P为 溶液,N电极上发生还原反应 溶液,N电极上发生还原反应 |
您最近一年使用:0次