1 . 回答下列问题
(1)氨分解反应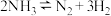 在容积为
在容积为 的密闭容器内进行。已知起始时氨气的物质的量为
的密闭容器内进行。已知起始时氨气的物质的量为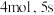 末为
末为 ,则用氨气表示该反应的速率为
,则用氨气表示该反应的速率为______ 氨分解反应的逆反应为合成氨,当消耗 时,放出
时,放出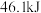 的热量,写出该反应的热化学方程式
的热量,写出该反应的热化学方程式______ 。
(2)如图所示,将锌、铜通过导线连接,置于稀硫酸中。
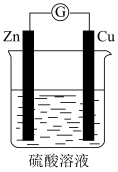
①负极电极反应式为______ 。
②正极电极反应式为______ 。
③溶液中 由
由______ (填“锌”或者“铜”下同)向_______ 移动。
④若反应过程中有 电子发生转移,则生成的氢气在标准状况下的体积为
电子发生转移,则生成的氢气在标准状况下的体积为______ 。
(1)氨分解反应
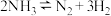 在容积为
在容积为 的密闭容器内进行。已知起始时氨气的物质的量为
的密闭容器内进行。已知起始时氨气的物质的量为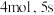 末为
末为 ,则用氨气表示该反应的速率为
,则用氨气表示该反应的速率为 时,放出
时,放出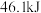 的热量,写出该反应的热化学方程式
的热量,写出该反应的热化学方程式(2)如图所示,将锌、铜通过导线连接,置于稀硫酸中。

①负极电极反应式为
②正极电极反应式为
③溶液中
 由
由④若反应过程中有
 电子发生转移,则生成的氢气在标准状况下的体积为
电子发生转移,则生成的氢气在标准状况下的体积为
您最近一年使用:0次
解题方法
2 . 回答下列问题:
(1)现有如下两个反应: A. ;B.
;B. 。判断上述两个反应中能设计成原电池的是
。判断上述两个反应中能设计成原电池的是_______ (填“A”或“B”)。
(2)将纯锌片和纯铜片按图中方式插入 相同浓度的稀硫酸中一段时间,回答下列问题:
相同浓度的稀硫酸中一段时间,回答下列问题:

①下列说法正确的是_______ 。
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的 均增大
均增大
②在相同时间内,两烧杯中产生气泡的速度:甲_______ 乙(填“>”“<”或“=”)。
③请写出图中构成原电池的负极电极反应式:_______ 。
(3)在反应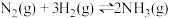 中,若以
中,若以 表示的该反应的化学反应速率为
表示的该反应的化学反应速率为 ,则以
,则以 表示此反应的化学反应速率为
表示此反应的化学反应速率为_______ 
(4)在 的恒容密闭容器中,充入
的恒容密闭容器中,充入 和
和 ,在一定条件下发生反应,
,在一定条件下发生反应, 后测得
后测得 的物质的量为
的物质的量为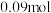 ,则以
,则以 的浓度变化表示的反应速率为
的浓度变化表示的反应速率为_______ 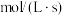
(5)将 充入容积为
充入容积为 的恒容密闭容器中,某温度下发生反应
的恒容密闭容器中,某温度下发生反应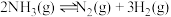 ,在
,在 内,消耗
内,消耗 的平均速率为
的平均速率为 ,则在
,则在 时,容器中生成
时,容器中生成_______ 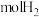 ,此时
,此时 的物质的量浓度为
的物质的量浓度为_______  。
。
(1)现有如下两个反应: A.
 ;B.
;B. 。判断上述两个反应中能设计成原电池的是
。判断上述两个反应中能设计成原电池的是(2)将纯锌片和纯铜片按图中方式插入
 相同浓度的稀硫酸中一段时间,回答下列问题:
相同浓度的稀硫酸中一段时间,回答下列问题:
①下列说法正确的是
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的
 均增大
均增大②在相同时间内,两烧杯中产生气泡的速度:甲
③请写出图中构成原电池的负极电极反应式:
(3)在反应
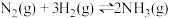 中,若以
中,若以 表示的该反应的化学反应速率为
表示的该反应的化学反应速率为 ,则以
,则以 表示此反应的化学反应速率为
表示此反应的化学反应速率为
(4)在
 的恒容密闭容器中,充入
的恒容密闭容器中,充入 和
和 ,在一定条件下发生反应,
,在一定条件下发生反应, 后测得
后测得 的物质的量为
的物质的量为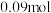 ,则以
,则以 的浓度变化表示的反应速率为
的浓度变化表示的反应速率为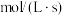
(5)将
 充入容积为
充入容积为 的恒容密闭容器中,某温度下发生反应
的恒容密闭容器中,某温度下发生反应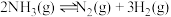 ,在
,在 内,消耗
内,消耗 的平均速率为
的平均速率为 ,则在
,则在 时,容器中生成
时,容器中生成 ,此时
,此时 的物质的量浓度为
的物质的量浓度为 。
。
您最近一年使用:0次
名校
3 . Ⅰ.在一定条件下A与B反应可生成C和D,其能量变化如图:

(1)若E1>E2,反应体系的总能量_______ (填“升高”或“降低”),为_______ (填“吸热”或“放热”)反应。原因是_______ 。
Ⅱ.2020年第七十五届联合国大会上,中国向世界郑重承诺在2030年前实现碳达峰,在2060年前实现碳中和。大力发展绿色能源、清洁能源是实现碳中和的最有效方法。
(2)原电池反应能够提供电能而不产生CO2气体,如图是某原电池装置图。

①Zn棒是原电池的_______ 极,发生_______ (填“氧化”或“还原”)反应。
②Cu棒上发生的电极反应式为_______ 。
③溶液中H+向_______ (填“Zn”或“Cu”)电极定向移动。
(3)将上述装置中电解质稀H2SO4换为足量AgNO3溶液,灯泡也变亮,电流表指针偏转,无色溶液颜色没有变化。
①原电池的负极是_______ (填“Zn”或“Cu”),正极的电极反应式为_______ 。
②若更换电解质时称量两个电极,质量恰好相等,放电一段时间后再称量两个电极,发现质量相差2.81g,则导线上通过的n(e-)=_______ mol。
(4)碱性锌锰电池是日常生活中常用电池,原电池反应是:Zn+2MnO2+2H2O=Zn(OH)2+2MnOOH。该原电池电解质是KOH溶液,写出正极的电极反应_______ 。

(1)若E1>E2,反应体系的总能量
Ⅱ.2020年第七十五届联合国大会上,中国向世界郑重承诺在2030年前实现碳达峰,在2060年前实现碳中和。大力发展绿色能源、清洁能源是实现碳中和的最有效方法。
(2)原电池反应能够提供电能而不产生CO2气体,如图是某原电池装置图。

①Zn棒是原电池的
②Cu棒上发生的电极反应式为
③溶液中H+向
(3)将上述装置中电解质稀H2SO4换为足量AgNO3溶液,灯泡也变亮,电流表指针偏转,无色溶液颜色没有变化。
①原电池的负极是
②若更换电解质时称量两个电极,质量恰好相等,放电一段时间后再称量两个电极,发现质量相差2.81g,则导线上通过的n(e-)=
(4)碱性锌锰电池是日常生活中常用电池,原电池反应是:Zn+2MnO2+2H2O=Zn(OH)2+2MnOOH。该原电池电解质是KOH溶液,写出正极的电极反应
您最近一年使用:0次
名校
解题方法
4 . 下列关于原电池的叙述正确的是
| A.构成原电池的正极和负极的材料必须是两种不同的金属 |
| B.原电池是将化学能转化为电能的装置 |
| C.在原电池中,电子流出的一极是正极 |
| D.原电池工作时,正极发生氧化反应 |
您最近一年使用:0次
2024-03-01更新
|
294次组卷
|
2卷引用:北京九中2023-2024学年高一下学期开学测试化学试题
名校
解题方法
5 . 近年来甲醇用途日益广泛,越来越引起商家的关注。工业上甲醇的合成途径多种多样。现在实验室中模拟甲醇合成反应,在2L密闭容器内,400℃时发生反应CO(g)+2H2(g) CH3OH(g),体系中n(CO)随时间的变化如表:
CH3OH(g),体系中n(CO)随时间的变化如表:
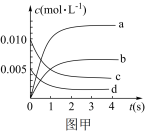
(1)图甲中表示CH3OH的变化的曲线是______ (填字母)。
(2)下列措施不能提高反应速率的有_______ (填字母,下同)。
a.升高温度 b.加入催化剂
c.减小压强 d.及时分离出CH3OH
(3)下列叙述能说明反应达到平衡状态的是_______ 。
a.CO和H2的浓度保持不变
b.v(H2)=2v(CO)
c.CO的物质的量分数保持不变
d.容器内气体密度保持不变
e.每生成1molCH3OH的同时有2molH-H断裂
(4)现有如下两个反应:A.NaOH+HCl=NaCl+H2O,B.Cu+2Ag+=2Ag+Cu2+。
①根据上述两反应的本质,能设计成原电池的是_______ (填字母)。
②将上述反应中能设计成原电池的反应设计成原电池。
I.写出负极的电极反应式________ ,反应类型为________ 。
II.画出装置图并标明电极材料与名称、电解质溶液、电子流向________ 。

 CH3OH(g),体系中n(CO)随时间的变化如表:
CH3OH(g),体系中n(CO)随时间的变化如表:| 时间/s | 0 | 1 | 2 | 3 | 5 |
| n(CO)/mol | 0.020 | 0.011 | 0.008 | 0.007 | 0.007 |
(1)图甲中表示CH3OH的变化的曲线是

(2)下列措施不能提高反应速率的有
a.升高温度 b.加入催化剂
c.减小压强 d.及时分离出CH3OH
(3)下列叙述能说明反应达到平衡状态的是
a.CO和H2的浓度保持不变
b.v(H2)=2v(CO)
c.CO的物质的量分数保持不变
d.容器内气体密度保持不变
e.每生成1molCH3OH的同时有2molH-H断裂
(4)现有如下两个反应:A.NaOH+HCl=NaCl+H2O,B.Cu+2Ag+=2Ag+Cu2+。
①根据上述两反应的本质,能设计成原电池的是
②将上述反应中能设计成原电池的反应设计成原电池。
I.写出负极的电极反应式
II.画出装置图并标明电极材料与名称、电解质溶液、电子流向

您最近一年使用:0次
2010·全国·一模
名校
解题方法
6 . 碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为Zn(s)+2MnO2(s)+2H2O(l)=Zn(OH)2(s)+2MnOOH(s),下列说法错误的是
| A.电池工作时,锌失去电子 |
| B.电池正极的电极反应式为2MnO2(s)+2H2O(l)+2e-=2MnOOH(s)+2OH-(aq) |
| C.电池工作时,电子由正极通过外电路流向负极 |
| D.外电路中每通过0.2mol电子,锌的质量理论上减小6.5g |
您最近一年使用:0次
2023-08-27更新
|
778次组卷
|
98卷引用:广西桂林市第十八中学2019-2020学年高一下学期开学考试化学试题
广西桂林市第十八中学2019-2020学年高一下学期开学考试化学试题(已下线)2010年春季武汉睿升学校高一期中考试化学卷(已下线)09~10年大连23中高一下学期期末考试化学卷(已下线)2010-2011学年江西省安福中学高一下学期期中考试化学试卷(已下线)2010-2011学年江西省上饶市第五中学高一下学期期中考试化学试卷(已下线)2010-2011学年江西省泰和中学高一下学期期末化学模拟试卷(已下线)2011-2012学年甘肃省金昌市第一中学高一期中考试(理)化学试卷 (已下线)2011-2012学年河北省衡水中学高一下学期期末考试化学试卷(已下线)2012年人教版高中化学必修二2.2 化学能与电能练习卷(已下线)2012-2013学年吉林省白山市第一中学高一下学期期末考试化学试卷(已下线)2013-2014湖北省黄石市三中高一下学期期中考试化学试卷2014-2015辽宁省实验中学分校高一下学期期中考试化学试卷2014-2015广西桂林市第十八中学高一下学期期中考试化学试卷2014-2015学年北京市房山区周口店中学高一下期中考试化学试卷2014-2015学年浙江省杭州第二中学高一下期中考试化学试卷2015-2016湖南浏阳市第一中学高二上入学考试化学试卷2015-2016学年河南省周口市商水一中高一下学期期中考试化学试卷2015-2016学年内蒙古平煤高中高一实验班下期中化学卷2015-2016学年辽宁省大连二十中高一6月月考化学试卷2015-2016学年河北省石家庄市辛集中学高一下第一次段考化学试卷2015-2016学年河北省永年二中高一下学期期末化学试卷2015-2016学年辽宁省庄河高中高一下期末化学试卷2016-2017学年河南师范大学附属中学高一3月月考化学试卷2016-2017学年广西桂林第18中学高一下学期期中模拟化学试卷2016-2017学年浙江省温州市“十五校联合体”高一下学期期中联考化学试卷湖南省邵阳市第二中学2016-2017学年高一下学期第三次月考化学试题广西河池市高级中学2016-2017学年高一下学期第二次月考化学试题高中化学人教版 选修四 第四章 电化学基础 第二节 化学电源 化学电源湖南省浏阳市第一中学2016-2017学年高二上学期入学考试化学试题安徽省定远重点中学2017-2018学年高一下学期教学段考化学试题【全国百强校】新疆维吾尔自治区乌鲁木齐八一中学2018-2019学年高一下学期期中考试化学试题黑龙江省牡丹江市第一高级中学2018-2019学年高一下学期期末考试化学试题陕西省黄陵中学高新部2018-2019学年高一下学期期末考试化学试题江西省南昌市第二中学2019-2020学年高一下学期第一次月考化学试题河南省鹤壁市外国语中学2019-2020学年高一下学期段考化学试题云南省玉溪市新平彝族傣自治县第一中学2020-2021学年高三上学期开学考试化学试题(已下线)江苏省江阴市第一中学2018-2019高一下学期期中考试化学试卷(已下线)【镇江新东方】高一下第一次月考一中镇中联考江苏省射阳中学2022-2023学年高一下学期3月月考化学试题山西省朔州市怀仁县阳高一中2023-2024学年高二上学期11月化学试卷宁夏石嘴山市第三中学2023-2024学年高一下学期3月月考化学试题(已下线)高考第一轮复习化学反应与能量变化单元测试(已下线)2010年广东省广州市番禹区高二下学期期中考试化学试题(已下线)2009—2010学年成都市玉林中学高二(下期)摸底测试化学(已下线)2010—2011年江苏盐城中学高二上学期期末考试化学卷(选修)(已下线)2011-2012学年甘肃省天水市一中高二上学期期末考试化学试卷(已下线)2012-2013学年陕西省三原县北城中学高二第四次月考化学试卷(已下线)2013届北京市大兴区高三上学期期末考试化学试卷(已下线)2014-2015河北省石家庄第二实验中学高二上学期期中化学(理)试卷2014-2015四川省雅安中学高二上学期期末模拟化学试卷2015-2016学年河北成安一中、永年二中高二上期中联考化学试卷2015-2016学年福建省龙海市程溪中学高二上学期期中测试化学试卷2016届辽宁省大连八中高三上学期期中测试化学试卷2015-2016学年四川阆中中学校高二上第二次段考化学试卷2015-2016学年黑龙江省海林林业局一中高二上期末考试化学试卷2015-2016学年甘肃省甘谷一中高二上期末化学试卷(已下线)同步君 选修4 第4章 第2节 化学电源2016-2017学年山东省济南市长清一中高二上第一次质检化学卷2016-2017学年西藏拉萨中学高二上月考三化学卷云南省峨山彝族自治县第一中学2017-2018学年高二上学期期末市统测模拟考化学试题广西陆川县中学2017-2018学年高二12月月考化学试题广东省深圳高中联考联盟2017-2018学年高二上学期期末考试化学试题福建省厦门市湖滨中学2017-2018学年高二下学期第一次月考化学试题吉林省辽源市田家炳高级中学2018-2019学年高二9月月考化学试题陕西省黄陵中学2018-2019学年高二(重点班)上学期期中考试化学试题黑龙江省哈尔滨市呼兰区第一中学2019届高三上学期第三次(12月)月考化学试题陕西省黄陵中学2018-2019学年高二上学期期末考试化学试题江西省分宜中学2018-2019学年高二下学期第一次月考化学试题【校级联考】黑龙江省龙东南七校2018-2019学年高二上学期期末联考化学试题四川省成都市七中实验学校2018-2019学年高二5月月考化学试题广西蒙山县第一中学2017-2018学年高二上学期期末考试化学试题(已下线)1.2.2 化学电源 练习《新教材同步备课》(鲁科版选择性必修1)福建省福清西山学校高中部2020-2021学年高二9月月考化学试题安徽省涡阳县育萃中学2020-2021学年高二上学期第一次月考化学试题鲁科版(2019)高二选择性必修第一册第1章 化学反应与能量变化 第2节 化学能转化为电能——电池 课时2 化学电源人教版(2019)高二化学选择性必修1第四章 化学反应与电能 第一节 原电池 课时2 化学电源(已下线)专题4.2 化学电源-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)福建省莆田第十五中学2018-2019学年高二上学期期中考试化学试题黑龙江省伊春市伊美区第二中学2018-2019学年高二上学期期末考试化学试题天津市第八中学2020-2021学年高二上学期第三次统练化学试题(已下线)练习8 原电池 化学电源-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)(已下线)第四章 电化学基础(基础过关)-2020-2021学年高二化学单元测试定心卷(人教版选修4)(已下线)4.2 化学电源(基础练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)吉林省白城市第一中学2020-2021学年高二下学期3月月考化学试题(已下线)1.2.2 化学电源(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)(已下线)第4章 化学反应与电能(章末检测)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)第4章 电化学基础(选拔卷)-【单元测试】2021-2022学年高二化学尖子生选拔卷(人教版选修4)四川省西充中学 2021-2022 学年高二上学期期中考试化学试题江苏省淮安市2021-2022学年高二上学期期末调研测试化学试题福建省福州市协作体四校2021-2022学年高二上学期期中联考化学试题四川省南充市2021-2022学年高二下学期期末考试化学试题第一节 原电池 第2课时 化学电源河北省石家庄市第四十二中学2022-2023高二上学期10月月考化学试题宁夏吴忠中学2022-2023学年高二上学期期中考试化学试题作业(五) 化学电源内蒙古呼伦贝尔市满洲里市第一中学2022-2023学年高二下学期期中考试化学试题第四章 化学反应与电能 第一节 原电池 第2课时 化学电源(已下线)BBWYhjhx1110.pdf
名校
解题方法
7 . 新冠肺炎最明显的症状就是出现发热,体温枪能快速检测人体体温。该体温枪所用的银锌电池是一种常见化学电源,反应原理为: ,其工作示意图如下图。下列说法正确的是
,其工作示意图如下图。下列说法正确的是
 ,其工作示意图如下图。下列说法正确的是
,其工作示意图如下图。下列说法正确的是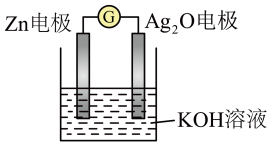
A. 向Zn电极移动 向Zn电极移动 |
B. 做正极,发生氧化反应 做正极,发生氧化反应 |
C.电子由Zn电极经外电路向 电极移动,再经电解质溶液回到Zn电极 电极移动,再经电解质溶液回到Zn电极 |
D. 电极的电极反应式: 电极的电极反应式: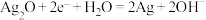 |
您最近一年使用:0次
2023-07-13更新
|
161次组卷
|
2卷引用:甘肃省兰州市第五十五中学2023-2024学年高一上学期开学考试化学试题
名校
8 . 通过如图装置进行能量转化。下列分析不正确的是
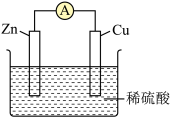
| A.该装置能将化学能转化为电能 |
| B.电子从锌片流向铜片,电流表指针偏转 |
C.Cu片;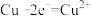 ;Zn片: ;Zn片: |
| D.氧化反应和还原反应可在两个不同的区域进行 |
您最近一年使用:0次
2023-07-13更新
|
233次组卷
|
4卷引用:甘肃省兰州市第五十五中学2023-2024学年高一上学期开学考试化学试题
名校
解题方法
9 . 我国高铁技术全球领先。CRH380B型动车组使用是镍镉(Ni-Cd)可充电电池,它作为原电池时,发生的反应为:Cd+2NiO(OH)+2H2O=Cd(OH)2+2Ni(OH)2。由此推断,该电池负极材料是
| A.Cd(OH)2 | B.Cd | C.Ni(OH)2 | D.NiO(OH) |
您最近一年使用:0次
2023-07-12更新
|
80次组卷
|
3卷引用:甘肃省兰州市第五十五中学2023-2024学年高一上学期开学考试化学试题
名校
解题方法
10 . 人们常常利用化学反应中的能量变化为人类服务。
(1)下列化学反应在理论上可以设计成原电池的是___________(填字母)。
(2)如图是某兴趣小组设计的原电池示意图,实验结束后,在实验报告上记录信息如下。
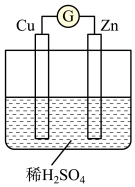
①实验报告中记录合理的是___________ (填字母)。
②请写出该电池的负极反应式:___________ 。
③将稀 换成
换成 溶液,电极质量增加的是
溶液,电极质量增加的是___________ (填“锌极”或“铜极”,下同),溶液中 移向
移向___________ 。
(1)下列化学反应在理论上可以设计成原电池的是___________(填字母)。
A.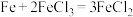 | B. |
C.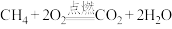 | D.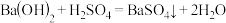 |

| a.电流计指针偏转 |
b.Cu极有 产生 产生 |
c. 向负极移动 向负极移动 |
| d.电流由Zn经导线流向Cu |
②请写出该电池的负极反应式:
③将稀
 换成
换成 溶液,电极质量增加的是
溶液,电极质量增加的是 移向
移向
您最近一年使用:0次
2023-07-12更新
|
301次组卷
|
2卷引用:甘肃省兰州市第五十五中学2023-2024学年高一上学期开学考试化学试题



