名校
1 . A、B、C、W、X、Y、Z均为短周期主族元素。其中A、B、C的原子序数依次增大,A原子最外层电子数比次外层多3,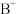 的离子与
的离子与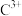 离子具有相同的电子层结构。其余元素在周期表中的位置如图所示,Z单质常用于自来水消毒。请按要求
离子具有相同的电子层结构。其余元素在周期表中的位置如图所示,Z单质常用于自来水消毒。请按要求用化学用语 回答下列问题:
(1) A、B、C原子半径由大到小的顺序为___________ ; 分子的空间构型为
分子的空间构型为___________ 。
(2)W、X、Z的最高价氧化物的水化物中酸性最强的为___________ ;A、W、Y的最简单氢化物中,沸点最高的是___________ 。
(3)2011年日本发生了9级大地震,福岛核电站遭到严重破坏,造成多种放射性物质的泄漏。其中放射性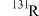 (中子数为78)与Z同主族,则R在周期表中的位置为
(中子数为78)与Z同主族,则R在周期表中的位置为___________ 。
(4)甲是W的一种气态氢化物,属于10电子分子。甲可用于制作燃料电池(原理如图所示)。则a为___________ (填“正”或“负”)极;a极的电极反应式为___________ 。___________ 。不同浓度的 与铁反应的还原产物很复杂,写出稀硝酸与过量的铁反应时生成
与铁反应的还原产物很复杂,写出稀硝酸与过量的铁反应时生成 的离子方程式
的离子方程式___________ 。
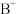 的离子与
的离子与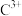 离子具有相同的电子层结构。其余元素在周期表中的位置如图所示,Z单质常用于自来水消毒。请按要求
离子具有相同的电子层结构。其余元素在周期表中的位置如图所示,Z单质常用于自来水消毒。请按要求| W | Y | ||
| X | Z |
(1) A、B、C原子半径由大到小的顺序为
 分子的空间构型为
分子的空间构型为(2)W、X、Z的最高价氧化物的水化物中酸性最强的为
(3)2011年日本发生了9级大地震,福岛核电站遭到严重破坏,造成多种放射性物质的泄漏。其中放射性
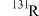 (中子数为78)与Z同主族,则R在周期表中的位置为
(中子数为78)与Z同主族,则R在周期表中的位置为(4)甲是W的一种气态氢化物,属于10电子分子。甲可用于制作燃料电池(原理如图所示)。则a为

 与铁反应的还原产物很复杂,写出稀硝酸与过量的铁反应时生成
与铁反应的还原产物很复杂,写出稀硝酸与过量的铁反应时生成 的离子方程式
的离子方程式
您最近一年使用:0次
2 . 为有效降低含氮化物的排放量,又能充分利用化学能,合作小组设计如图所示电池,将含氮化合物转化为无毒气体。下列说法错误的是
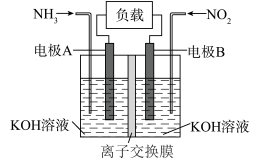
A.该电池的总反应为: |
| B.电池工作一段时间后,右侧电极室溶液的碱性增强 |
| C.同温同压时,左右两侧电极室中产生的气体体积比为4∶3 |
D.若离子交换膜为阴离子交换膜(只允许阴离子通过),电池工作时 从左侧电极室通过交换膜移向右侧 从左侧电极室通过交换膜移向右侧 |
您最近一年使用:0次
名校
解题方法
3 . 下列关于下图所示装置的叙述,错误的是

| A.锌是负极,其质量逐渐减小 | B.氢离子在铜表面被还原,产生气泡 |
C.溶液中 移向铜片 移向铜片 | D.电子从锌片经导线流向铜片 |
您最近一年使用:0次
名校
4 . 下列说法中不正确的是
| A.化学电池的反应原理是自发的氧化还原反应 |
| B.充电电池不能无限制地反复充电、放电 |
| C.铅酸蓄电池和锌锰酸性干电池都是可充电电池 |
| D.燃料电池是一种高效且对环境友好的新型电池 |
您最近一年使用:0次
名校
解题方法
5 . 某化学兴趣小组为了探究铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
根据表中记录的实验现象,回答下列问题。
(1)实验1、2中Al电极的作用是否相同______ (填“相同”或“不相同”)。
(2)实验3中Al为______ 极,电极反应式为______ ;
石墨为______ 极,电极反应式为______ ;
电池总反应为(离子方程式)______ 。
| 编号 | 电极材料 | 电解质溶液 | 电流表指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、石墨 | 稀盐酸 | 偏向石墨 |
(1)实验1、2中Al电极的作用是否相同
(2)实验3中Al为
石墨为
电池总反应为(离子方程式)
您最近一年使用:0次
名校
6 . 一种铁-空气电池的电池反应为: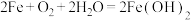 ,原理如图所示,下列有关该电池的说法正确的是
,原理如图所示,下列有关该电池的说法正确的是
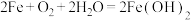 ,原理如图所示,下列有关该电池的说法正确的是
,原理如图所示,下列有关该电池的说法正确的是
A.a极的电极反应式为: |
B.当电路中转移0.2mol电子时,消耗1.12L  |
| C.b极为电池正极,发生氧化反应 |
| D.电子由a极经负载流向b极,再经NaOH溶液回到a极 |
您最近一年使用:0次
名校
7 . Ⅰ.汽车尾气中含有CO、NO等有害气体,某新型催化剂能促使NO、CO转化为两种无毒气体。一定温度下,在体积为2L的恒容密闭容器中加入等物质的量的NO和CO,测得部分物质的物质的量随时间的变化如图所示。___________ 逆反应速率(填“>”“<”或“=”)。
(2)该反应的化学方程式为___________ 。
(3)从反应开始到达到平衡,
___________  ;该条件下,设起始压强为P,平衡时压强为
;该条件下,设起始压强为P,平衡时压强为 ,则
,则 的值为
的值为___________ 。
(4) 、
、 和熔融
和熔融 可制作燃料电池,其原理如图所示。该电池在放电过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用,则正极反应式为
可制作燃料电池,其原理如图所示。该电池在放电过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用,则正极反应式为___________ 。 ,反应过程中的能量变化如图所示。
,反应过程中的能量变化如图所示。___________ (填“放热”或“吸热”)反应,生成1mol  吸收或放出的热量为
吸收或放出的热量为___________ kJ(用a,b表示)。
(6)在恒容条件下进行该反应,下列叙述能说明反应达到平衡状态的是___________ (请用相应字母填空);
a.CO和 的浓度保持不变
的浓度保持不变
b.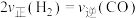
c.每生成1mol 的同时有2mol H-H键形成
的同时有2mol H-H键形成
d.容器内气体密度保持不变
e.容器内质量保持不变

(2)该反应的化学方程式为
(3)从反应开始到达到平衡,

 ;该条件下,设起始压强为P,平衡时压强为
;该条件下,设起始压强为P,平衡时压强为 ,则
,则 的值为
的值为(4)
 、
、 和熔融
和熔融 可制作燃料电池,其原理如图所示。该电池在放电过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用,则正极反应式为
可制作燃料电池,其原理如图所示。该电池在放电过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用,则正极反应式为
 ,反应过程中的能量变化如图所示。
,反应过程中的能量变化如图所示。
 吸收或放出的热量为
吸收或放出的热量为(6)在恒容条件下进行该反应,下列叙述能说明反应达到平衡状态的是
a.CO和
 的浓度保持不变
的浓度保持不变b.

c.每生成1mol
 的同时有2mol H-H键形成
的同时有2mol H-H键形成d.容器内气体密度保持不变
e.容器内质量保持不变
您最近一年使用:0次
名校
8 . 化学反应过程不仅发生了物质变化,还存在能量的变化,最主要的能量形式为热能和电能,根据题目要求回答以下问题:
(1)工业合成氨的反应 是一个可逆反应,反应条件是高温、高压,并且需要合适的催化剂,已知断裂1mol相应化学键需要的能量如下,若反应生成1.5mol
是一个可逆反应,反应条件是高温、高压,并且需要合适的催化剂,已知断裂1mol相应化学键需要的能量如下,若反应生成1.5mol  (g),可
(g),可___________ (填“吸收”或“放出”)热量___________ kJ。
(2)在100℃时,将0.4mol  放入2L的真空容器中发生反应:
放入2L的真空容器中发生反应: 。测得容器内气体的物质的量随时间变化如下表:
。测得容器内气体的物质的量随时间变化如下表:
①上述条件下。前20s内以 表示的平均化学反应速率为
表示的平均化学反应速率为___________ ;达到平衡状态时, 的转化率是
的转化率是___________ 。
②
___________ 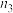 (填“>”、=”、“<”)。
(填“>”、=”、“<”)。
(3)铅蓄电池是常用的化学电源。汽车中的电瓶使用的就是铅酸电池,工作时电池总反应为 ,下列说法正确的是___________(请用相应字母填空)
,下列说法正确的是___________(请用相应字母填空)
(4)甲醇( )—空气燃料电池是一种高效能、轻污染的车载电池,以KOH为电解质溶液。通入氧气的电极为感料电池的
)—空气燃料电池是一种高效能、轻污染的车载电池,以KOH为电解质溶液。通入氧气的电极为感料电池的___________ (填“正”或“负”)极,负极发生的电极反应式为___________ 。
(1)工业合成氨的反应
 是一个可逆反应,反应条件是高温、高压,并且需要合适的催化剂,已知断裂1mol相应化学键需要的能量如下,若反应生成1.5mol
是一个可逆反应,反应条件是高温、高压,并且需要合适的催化剂,已知断裂1mol相应化学键需要的能量如下,若反应生成1.5mol  (g),可
(g),可| 化学键 | H—H | N—H | N≡N |
| 能量 | 436kJ | 391kJ | 946kJ |
 放入2L的真空容器中发生反应:
放入2L的真空容器中发生反应: 。测得容器内气体的物质的量随时间变化如下表:
。测得容器内气体的物质的量随时间变化如下表:| 时间/s | 0 | 20 | 40 | 60 | 80 |
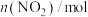 | 0.4 |  | 0.26 | 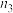 | 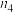 |
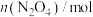 | 0 | 0.05 |  | 0.08 | 0.08 |
 表示的平均化学反应速率为
表示的平均化学反应速率为 的转化率是
的转化率是②

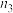 (填“>”、=”、“<”)。
(填“>”、=”、“<”)。(3)铅蓄电池是常用的化学电源。汽车中的电瓶使用的就是铅酸电池,工作时电池总反应为
 ,下列说法正确的是___________(请用相应字母填空)
,下列说法正确的是___________(请用相应字母填空)A.放电时,负极的电极反应式为: |
| B.放电时,正极附近溶液pH增大 |
| C.充电时,理论上每消耗30.3g硫酸铅,外电路中转移的电子为0.2mol |
| D.放电时,电池两电极的质量均增加 |
 )—空气燃料电池是一种高效能、轻污染的车载电池,以KOH为电解质溶液。通入氧气的电极为感料电池的
)—空气燃料电池是一种高效能、轻污染的车载电池,以KOH为电解质溶液。通入氧气的电极为感料电池的
您最近一年使用:0次
名校
解题方法
9 . I.化学反应中伴随着能量变化,根据相关知识回答下列问题:
(1)下列过程吸热的是___________ (填序号)。
a.生石灰溶于水 b.浓硫酸稀释 c.硝酸铵溶于水 d.铜溶于浓硝酸
e.氯化铵固体与氢氧化钡晶体混合搅拌
(2)已知H2和O2反应放热, 且断开1molH-H键、1molO=O键、1molO-H键需吸收的能量分别为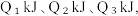 由此可以推知下列关系正确的是
由此可以推知下列关系正确的是___________ (填序号)。
①.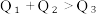 ②.
②. 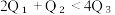 ③.
③. 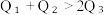 ④.
④. 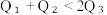
Ⅱ.某同学用导线将电流表与Zn片、Cu片相连接,插入盛有稀硫酸的烧杯中进行实验,如图所示。___________ 。
(4)从构成原电池的基本要素来看,稀硫酸的作用是(选填以下序号)___________ 。
a.反应物 b.电极材料 c.离子导体 d.电子导体
(5)该原电池的负极反应式为___________ ,___________ (填“电子”或“电流”)是由锌片经导线流向铜片。标准状况下,若反应过程中溶解了6.5g锌,则生成的氢气的体积为___________ L。
(6)某同学想利用反应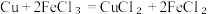 设计一个原电池请在下图
设计一个原电池请在下图___________ (共2处)标出使用的用品。
(1)下列过程吸热的是
a.生石灰溶于水 b.浓硫酸稀释 c.硝酸铵溶于水 d.铜溶于浓硝酸
e.氯化铵固体与氢氧化钡晶体混合搅拌
(2)已知H2和O2反应放热, 且断开1molH-H键、1molO=O键、1molO-H键需吸收的能量分别为
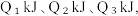 由此可以推知下列关系正确的是
由此可以推知下列关系正确的是①.
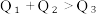 ②.
②. 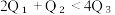 ③.
③. 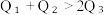 ④.
④. 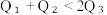
Ⅱ.某同学用导线将电流表与Zn片、Cu片相连接,插入盛有稀硫酸的烧杯中进行实验,如图所示。
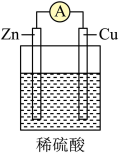
(4)从构成原电池的基本要素来看,稀硫酸的作用是(选填以下序号)
a.反应物 b.电极材料 c.离子导体 d.电子导体
(5)该原电池的负极反应式为
(6)某同学想利用反应
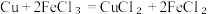 设计一个原电池请在下图
设计一个原电池请在下图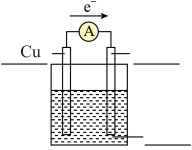
您最近一年使用:0次
解题方法
10 . 在2L恒温恒容密闭容器中投入2molSO2和1molO2在一定条件下充分反应,如图是SO2和SO3随时间的变化曲线。___________ ;平衡时,SO2的转化率为___________ 。
(2)下列叙述能判断该反应达到平衡状态的是___________ (填序号)。
①容器中压强不再改变
②容器中气体密度不再改变
③SO3的质量不再改变
④O2的物质的量浓度不再改变
⑤SO2的消耗速率和SO3的生成速率相等
(3)以下操作会引起化学反应速率变快的是___________ (填字母)。
A.向容器中通入氦气 B.升高温度 C.扩大容器的容积 D.向容器中通入O2 E.使用催化剂
(4)25min时,正反应速率___________ 逆反应速率(填“>”“<”或“=”)。
(5)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:___________ 。(填“正极”或“负极”)
②电解质溶液中OH-离子向___________ 移动(填“电极a”或“电极b”)。
③电极b的电极反应式为___________ 。

(2)下列叙述能判断该反应达到平衡状态的是
①容器中压强不再改变
②容器中气体密度不再改变
③SO3的质量不再改变
④O2的物质的量浓度不再改变
⑤SO2的消耗速率和SO3的生成速率相等
(3)以下操作会引起化学反应速率变快的是
A.向容器中通入氦气 B.升高温度 C.扩大容器的容积 D.向容器中通入O2 E.使用催化剂
(4)25min时,正反应速率
(5)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:
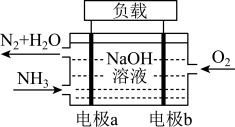
②电解质溶液中OH-离子向
③电极b的电极反应式为
您最近一年使用:0次



