1 . 海水电池在海洋能源领域备受关注,一种锂-海水电池构造示意图如下。下列说法错误的是

| A.海水起电解质溶液作用 |
B.N极仅发生的电极反应: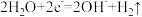 |
| C.玻璃陶瓷具有传导离子和防水的功能 |
| D.该锂-海水电池属于一次电池 |
您最近一年使用:0次
2022-06-10更新
|
13270次组卷
|
40卷引用:2022年湖南卷高考真题变式题(1-10)
(已下线)2022年湖南卷高考真题变式题(1-10)2022年新高考湖南化学高考真题(已下线)专题08 电化学及其应用-2022年高考真题模拟题分项汇编(已下线)专题08 电化学及其应用-三年(2020-2022)高考真题分项汇编(已下线)考点18 原电池 化学电源-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第15练 化学反应与能量变化-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第18讲 原电池 化学电源(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)易错点19 电化学基础-备战2023年高考化学考试易错题(已下线)热点情景汇编-专题八 化学反应中的电能(已下线)专题05 化学能与电能的转化(讲)-2023年高考化学二轮复习讲练测(新高考专用)湖南省株洲市九方中学2022-2023学年高三上学期第一次月考化学试题湖南省株洲市九方中学2022-2023学年高三上学期第二次月考化学试题(已下线)专题16 新型电化学装置分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第一部分 二轮专题突破 专题11 新型电池和电解原理的应用(已下线)题型20 两室膜电解装置及其应用(已下线)专题一 原电池的工作原理及其应用(练习)(已下线)专题卷14 新型化学电源装置-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)题型16 锂电池和锂离子电池的应用(已下线)题型15 金属–空气电池的应用(已下线)专题12 电化学的综合应用(已下线)专题12 电化学的综合应用(已下线)专题07 电化学及其应用-2023年高考化学真题题源解密(新高考专用)(已下线)考点19 电解池(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)热点题型训练 新型化学电源及其应用(已下线)第3讲 原电池 化学电源(已下线)题型11 新型电化学装置分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)第08练 以新型化学电源及电极反应式的书写突破原电池原理-2022年【暑假分层作业】高二化学(2023届一轮复习通用)黑龙江省双鸭山市第一中学2021-2022学年高一下学期期末考试化学试题黑龙江省鹤岗市第一中学2021-2022学年高一下学期期末考试化学试题山东省威海乳山市银滩高级中学2022-2023学年高二9月月考化学试题广东省深圳市高级中学2022-2023学年高二上学期期中考试化学试题江苏省苏州市2022-2023学年高一下学期期末应考化学试题(已下线)第16练 原电池 新型电池 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)作业(二十六) 金属的腐蚀与防护黑龙江省哈尔滨市第四中学校2022-2023学年高一下学期期末考试化学试题第四章 化学反应与电能 第一节 原电池 第2课时 化学电源浙江省杭州第十四中学2023-2024学年高二上学期 期中考试化学试卷10-2023新东方高二上期中考化学广东省佛山市顺德区桂洲中学2023-2024学年高一下学期第二次联考化学模拟试题2(已下线)重难点02 化学反应与能量-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(江苏专用)
解题方法
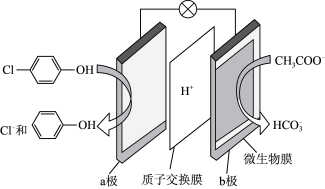
2 . 通过膜电池可除去废水中的乙酸钠和对氯苯酚(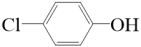 ),其原理如图所示,下列说法错误的是
),其原理如图所示,下列说法错误的是
 ),其原理如图所示,下列说法错误的是
),其原理如图所示,下列说法错误的是
| A.环境温度对该电池会有影响 |
| B.每消耗1molCH3COO-,电路中通过的电子数为8NA |
C. 、 、 均能与氯化铁溶液发生显色反应 均能与氯化铁溶液发生显色反应 |
| D.该电池工作时,外电路中的电流由b极流向a极 |
您最近一年使用:0次
3 . 丙烯是重要的有机化工原料,丙烷脱氢是工业生产丙烯的重要途径。回答下列相关问题:
(1)已知:Ⅰ.2C3H8(g)+O2(g) 2C3H6(g)+2H2O(g) △H1=-238kJ•mol-1
2C3H6(g)+2H2O(g) △H1=-238kJ•mol-1
Ⅱ.2H2(g)+O2(g) 2H2O(g) △H2=-484kJ•mol-1
2H2O(g) △H2=-484kJ•mol-1
则丙烷脱氢制丙烯反应C3H8(g) C3H6(g)+H2(g)的△H为
C3H6(g)+H2(g)的△H为_______ kJ•mol-1
(2)一定温度下,向1L的密闭容器中充入1mol C3H8发生脱氢反应,经过10min达到平衡状态,测得平衡时气体压强是开始的1.5倍。
①0~10min丙烷的化学反应速率v(C3H8)=_______ mol•L-1•min-1。
②下列情况能说明该反应达到平衡状态的是_______ 。
A.△H不变 B.C3H8与H2的物质的量之比保持不变
C.混合气体密度不变 D.混合气体的总压强不变
(3)一定温度下,向恒容密闭容器中充入1mol C3H8,开始压强为pkPa,C3H8的气体体积分数与反应时间的关系如图所示:
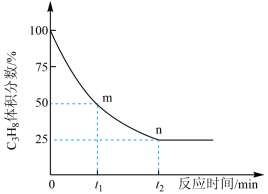
①此温度下该反应的平衡常数Kp=_______ (用含字母p的代数式表示,Kp是用反应体系中气体物质的分压表示的平衡常数,平衡分压=总压×体积分数)。
②已知该反应过程中,v正=k正p(C3H8),v逆=k逆p(C3H6)p(H2),其中k正、k逆为速率常数,只与温度有关,则图中m点处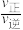 =
=_______ 。
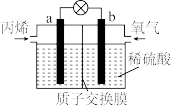
(4)某丙烯燃料电池的工作原理如图所示,质子交换膜(只有质子能够通过)左右两侧的溶液均为1L 2mol/L H2SO4溶液。a极的电极反应式为_______ ;当导线中有1.8mol e-发生转移时,左右两侧溶液的质量差为_______ g ( 假设反应物耗尽,忽略气体的溶解)。
(1)已知:Ⅰ.2C3H8(g)+O2(g)
 2C3H6(g)+2H2O(g) △H1=-238kJ•mol-1
2C3H6(g)+2H2O(g) △H1=-238kJ•mol-1Ⅱ.2H2(g)+O2(g)
 2H2O(g) △H2=-484kJ•mol-1
2H2O(g) △H2=-484kJ•mol-1则丙烷脱氢制丙烯反应C3H8(g)
 C3H6(g)+H2(g)的△H为
C3H6(g)+H2(g)的△H为(2)一定温度下,向1L的密闭容器中充入1mol C3H8发生脱氢反应,经过10min达到平衡状态,测得平衡时气体压强是开始的1.5倍。
①0~10min丙烷的化学反应速率v(C3H8)=
②下列情况能说明该反应达到平衡状态的是
A.△H不变 B.C3H8与H2的物质的量之比保持不变
C.混合气体密度不变 D.混合气体的总压强不变
(3)一定温度下,向恒容密闭容器中充入1mol C3H8,开始压强为pkPa,C3H8的气体体积分数与反应时间的关系如图所示:

①此温度下该反应的平衡常数Kp=
②已知该反应过程中,v正=k正p(C3H8),v逆=k逆p(C3H6)p(H2),其中k正、k逆为速率常数,只与温度有关,则图中m点处
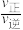 =
=(4)某丙烯燃料电池的工作原理如图所示,质子交换膜(只有质子能够通过)左右两侧的溶液均为1L 2mol/L H2SO4溶液。a极的电极反应式为

您最近一年使用:0次
2022-04-26更新
|
1013次组卷
|
3卷引用:2022年湖南卷高考真题变式题(15-19)
名校
4 . 《Science》杂志报道了王浩天教授团队发明的制取H2O2的绿色方法,原理如图所示。下列说法正确的是
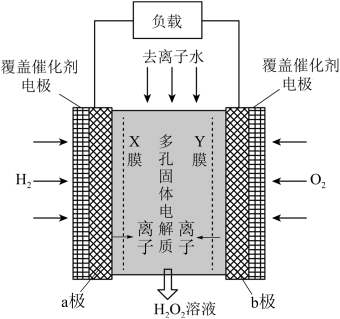

| A.a极为正极,发生还原反应 |
| B.X膜为阳离子交换膜 |
| C.当外电路通过2mol e-时,消耗22.4L O2 |
| D.该装置可实现化学能与电能间的完全转化 |
您最近一年使用:0次
2022-04-14更新
|
2141次组卷
|
14卷引用:2022年湖南卷高考真题变式题(1-10)
(已下线)2022年湖南卷高考真题变式题(1-10)(已下线)押全国卷理综第11题 电化学基础-备战2022年高考化学临考题号押题(课标全国卷)(已下线)2022年全国甲卷高考真题变式题(选择题)湖南省株洲市九方中学2022-2023学年高三上学期第一次月考化学试题湖南省攸县第一中学2022-2023学年高三第六次月考化学试题湖南省涟源市第一中学2023届高三第五次月考化学试题湖南省永州市第一中学2023届高三下学期第五次月考化学试题湖南省永州市第一中学2022-2023学年高三第七次月考化学试题广东省梅州市 2022届高三二模(4月)化学试题(已下线)化学-2022年高考考前押题密卷(湖北卷)福建省莆田第一中学2021-2022学年高二下学期期中考试化学试题福建省福州第八中学2021-2022学年高二下学期期末考试化学试题安徽省舒城中学2022-2023学年高二上学期第二次月考化学试题河北省唐山市遵化市第一中学2023-2024学年高三上学期月考2 化学试题
名校
解题方法
5 . 氮及其化合物的利用是科学家们一直在探究的问题,它们在工农业生产和生命活动中起着重要的作用。
(1)已知:2C(s)+O2(g)=2CO(g) ΔH=-221kJ·mol-1
C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1
N2(g)+O2(g)=2NO(g) ΔH=+181kJ·mol-1
若某反应的平衡常数表达式为K= ,请写出此反应的热化学方程式:
,请写出此反应的热化学方程式:_______ 。
(2)汽车尾气中的NO和CO在一定条件下可发生反应生成无毒的N2和CO2。将NO和CO以一定的流速通过两种不同的催化剂(cat1、cat2)进行反应,相同时间内测得的脱氮率(脱氮率即NO的转化率)如图所示。M点_______ (填“是”或“不是”)对应温度下的平衡脱氮率,理由是_______ 。

(3)通过NOx传感器可监测NOx的含量,其工作原理如图。

①Pt电极上发生的是_______ 反应(填“氧化”或“还原”)。
②写出NiO电极上的电极反应式:_______ 。
(4)某温度下,在一密闭容器中充入一定量NO(g)发生反应4NO(g)⇌N2(g)+2NO2(g) ΔH<0,其正反应速率表达式为v正=k正·cn(NO)(k正为速率常数,只与温度有关),测得反应速率和NO浓度的数据如表所示。
则k正=_______ mol-3·L3·s-1;下列对于该反应的说法正确的是_______ (填标号)。
A.当混合气体颜色保持不变时,反应达到化学平衡状态
B.当 的比值保持不变时,反应达到化学平衡状态
的比值保持不变时,反应达到化学平衡状态
C.反应达到化学平衡状态时,每消耗0.1molNO就会消耗0.05molNO2
D.反应达到平衡状态后,若降低温度,则混合气体的颜色变浅
E.反应达到平衡状态后,若减小压强,则混合气体的平均相对分子质量减小
(1)已知:2C(s)+O2(g)=2CO(g) ΔH=-221kJ·mol-1
C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1
N2(g)+O2(g)=2NO(g) ΔH=+181kJ·mol-1
若某反应的平衡常数表达式为K=
 ,请写出此反应的热化学方程式:
,请写出此反应的热化学方程式:(2)汽车尾气中的NO和CO在一定条件下可发生反应生成无毒的N2和CO2。将NO和CO以一定的流速通过两种不同的催化剂(cat1、cat2)进行反应,相同时间内测得的脱氮率(脱氮率即NO的转化率)如图所示。M点

(3)通过NOx传感器可监测NOx的含量,其工作原理如图。

①Pt电极上发生的是
②写出NiO电极上的电极反应式:
(4)某温度下,在一密闭容器中充入一定量NO(g)发生反应4NO(g)⇌N2(g)+2NO2(g) ΔH<0,其正反应速率表达式为v正=k正·cn(NO)(k正为速率常数,只与温度有关),测得反应速率和NO浓度的数据如表所示。
| 序号 | c(NO)/(mol·L-1) | v正/(mol·L-1·s-1) |
| ① | 0.10 | 4.00×10-9 |
| ② | 0.20 | 6.40×10-8 |
| ③ | 0.30 | 3.24×10-7 |
A.当混合气体颜色保持不变时,反应达到化学平衡状态
B.当
 的比值保持不变时,反应达到化学平衡状态
的比值保持不变时,反应达到化学平衡状态C.反应达到化学平衡状态时,每消耗0.1molNO就会消耗0.05molNO2
D.反应达到平衡状态后,若降低温度,则混合气体的颜色变浅
E.反应达到平衡状态后,若减小压强,则混合气体的平均相对分子质量减小
您最近一年使用:0次
2022-04-07更新
|
1034次组卷
|
11卷引用:2022年湖南卷高考真题变式题(15-19)
(已下线)2022年湖南卷高考真题变式题(15-19)(已下线)专项16 化学反应原理综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)湖南省长沙市麓山国际实验学校2022-2023学年高三上学期入学考试化学试题湖南省隆回县第二中学2022-2023学年高二上学期线上课程摸底(期中)考试化学试题湖南省株洲市第四中学2022-2023学年高二上学期期中考试化学试题湖南省株洲市南方中学2023届高三第六次月考化学试题湖南省永州市第一中学2023届高三下学期第五次月考化学试题陕西省西安中学2021-2022学年高三下学期第四次模拟考试理科综合化学试题(已下线)化学(辽宁B卷)-学易金卷:2023年高考第一次模拟考试卷辽宁省本溪市高级中学2022-2023学年高三上学期期中测试化学试题湖北省武汉市武钢三中2023-2024学年高三上学期7月月考化学试题
名校
6 . 金属(M)—空气电池的工作原理如图所示。下列说法正确的是
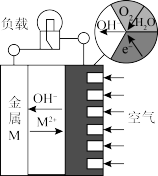

| A.金属M作电池正极,发生氧化反应 |
| B.工作时电子通过负载向负极移动 |
| C.正极的电极反应O2+4H++4e−=2H2O |
| D.电池反应为2M+O2+2H2O=2M(OH)2 |
您最近一年使用:0次
7 . 微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得电能,同时可实现海水淡化。现以NaCl溶液模拟海水,采用惰性电极,用下图装置处理有机废水(以含 CH3COO-的溶液为例)。下列说法错误的是
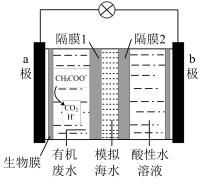
A.负极反应为 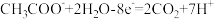 |
| B.隔膜1为阳离子交换膜,隔膜2为阴离子交换膜 |
| C.当电路中转移1mol电子时,模拟海水理论上除盐58.5g |
| D.电池工作一段时间后,正、负极产生气体的物质的量之比为2:1 |
您最近一年使用:0次
2020-07-11更新
|
14609次组卷
|
80卷引用:2022年湖南卷高考真题变式题(1-10)
(已下线)2022年湖南卷高考真题变式题(1-10)(已下线)专题08 电化学及其应用-2020年高考真题和模拟题化学分项汇编(已下线)专题讲座(六)新型电源及电极反应式的书写(精讲)——2021年高考化学一轮复习讲练测(已下线)第21讲 电解池 金属的电化学腐蚀与防护 (精讲)——2021年高考化学一轮复习讲练测湖南师范大学附属中学2020-2021学年高二上学期期中考试化学试题(已下线)小题必刷25 原电池及化学电源——2021年高考化学一轮复习小题必刷(通用版本)(已下线)小题必刷26 电解池原理及其应用——2021年高考化学一轮复习小题必刷(通用版本)(已下线)专题05 化学反应与能量——备战2021年高考化学纠错笔记(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)热点9 化学能与电能-2021年高考化学【热点·重点·难点】专练(新高考)(已下线)小题16 新型原电池装置——备战2021年高考化学经典小题考前必刷(全国通用)(已下线)押山东卷第10题 原电池选择题-备战2021年高考化学临考题号押题(山东卷)(已下线)第19讲 电解池 金属的电化学腐蚀与防护(精讲)-2022年一轮复习讲练测(已下线)课时33 多池多室带膜电化学装置-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点21 原电池 化学电源-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点21 原电池 化学电源-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题讲座(四)新型电源及电极反应式的书写 (讲) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)专题08 电化学及其应用-备战2022年高考化学真题及地市好题专项集训【山东专用】(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)卷08 电化学及其应用-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)押新高考卷12题 电化学基础-备战2022年高考化学临考题号押题(新高考通版)(已下线)2022年全国甲卷高考真题变式题(选择题)(已下线)考点18 原电池 化学电源-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)专题讲座(六) 电解质介质和隔膜在电化学的作用(练)-2023年高考化学一轮复习讲练测(全国通用)湖南省衡阳县第四中学 2022-2023学年高二下学期开学摸底考试(平行班)化学试题(已下线)第六章 化学反应与能量 第36讲 新型化学电源(已下线)专题一 原电池的工作原理及其应用(已下线)专题一 原电池的工作原理及其应用(练习)(已下线)专题八 电化学的相关计算(练习)(已下线)题型18 微生物电池的应用(已下线)专题12 电化学的综合应用(已下线)第25讲电解池与金属的电化学腐蚀(已下线)第24讲原电池与化学电源(已下线)第3讲 原电池 化学电源湖南省邵阳市邵东市创新高级中学2023-2024学年高三上学期第四次月考化学试题2020年山东省高考化学试卷(新高考)四川省成都市双流棠湖中学2021届高三上学期开学考试理综化学试题安徽省蚌埠市2021届高三上学期第一次质量监测化学试题山东省滨州渤海中学2020-2021学年高二上学期10月月考化学试题黑龙江省哈尔滨市第六中学2021届高三12月月考化学试题西藏拉萨中学2021届高三上学期第三次月考理综化学试题甘肃省静宁县第一中学2021届高三上学期第四次模拟考试化学试题河南省豫南九校2020-2021学年高二上学期第四次联考化学试题江苏省南京市高淳高级中学2021届高三10月阶段性检测化学试题湖北省宜昌市夷陵中学2020-2021学年高二下学期3月份阶段性检测化学试题河南省鹤壁高中2020-2021学年高二下学期第一次段考化学试题河南省驻马店市2020-2021学年高一下学期期末考试化学试题选择性必修1(SJ)专题1专题培优专练选择性必修1 专题1 素养检测河北省张家口市第一中学2020-2021学年高二上学期10月月考(衔接班)化学 试题江苏省昆山市周市高级中学2021-2022学年高三上学期暑期自主学习测试化学试题江苏省徐州市第三中学2021-2022学年高二上学期10月月考化学试题山东省济南市第一中学2021-2022学年高二上学期期中考试化学试题河南省信阳市2021-2022学年高二上学期期末考试化学试题山东省济宁邹城市第二中学2021-2022学年高二12月月考化学试题北京市第二中学2021-2022学年高三12月月考化学试题(已下线)必刷卷01-2022年高考化学考前信息必刷卷(辽宁地区专用)(已下线)化学-2022年高考押题预测卷02(广东卷)西藏自治区拉萨市拉萨中学2022届高三第八次月考理综化学试题(已下线)2020年山东卷化学高考真题变式题11-15第四章 综合拔高练山西省长治市上党区一中2021-2022学年高二上学期10月月考化学试题福建省莆田第二十五中学2022-2023学年高二上学期月考(一)化学试题福建省福州第十五中学2022-2023学年高二上学期10月月考化学试题河南省洛阳市新安县第一高级中学2022-2023学年高三上学期入学测试(实验小班)化学试题福建省福州市第一中学2022-2023学年高二上学期10月月考化学试题福建省泉州市石狮市石光中学2022-2023学年高二上学期期中考试化学试题福建省石狮市第一中学2022-2023学年高二上学期第一次月考化学试题山东烟台2022-2023学年高一下学期3月月考化学试题山东省菏泽市2022-2023学年高一下学期期末考试化学试题黑龙江省七台河市勃利县高级中学2022-2023学年高三上学期11月期中考试化学试题四川省成都市石室中学2023-2024学年高二上学期开学考试化学试题河北省石家庄市新乐市第一中学2023-2024学年高三上学期开学测试化学试题福建省福州市连江尚德中学2023-2024学年高二上学期第一次诊断性测试化学试题福建省福州市闽侯县第一中学2023-2024学年高二上学期10月月考化学试题吉林省通化市辉南县第六中学2023-2024学年高二上学期11月半月考化学试卷 河北省沧州市泊头市第一中学2023-2024学年高二上学期12月月考化学试题福建省福建师范大学附属中学2023-2024学年高三上学期开学考化学试题



