名校
解题方法
1 . 全固态锂金属电池具有更高比能和更高安全性。我国科研团队设计了基于LLZ-TO@Ag复合层负极改性的硫化物全固态锂电池,结构如图,放电时电池反应: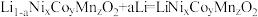 。下列说法不正确的是
。下列说法不正确的是
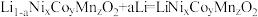 。下列说法不正确的是
。下列说法不正确的是
| A.充电时,电流流向为电源→b极→固态电解质→a极 |
B.放电时, 流向为a极→复合层→固态电解质→b极 流向为a极→复合层→固态电解质→b极 |
C.充电时,b极的电极反应为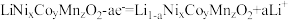 |
D.放电前两电极质量相等,放电过程中,当两电极质量差值为1.4g时,电路中转移0.2mol  |
您最近一年使用:0次
解题方法
2 . 某锂离子聚合物电池的原理如图所示,下列说法正确的是

| A.充电时,A与电源正极相连 |
B.放电时,B极发生反应为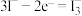 |
| C.充放电过程中,有2种元素化合价发生变化 |
D.每 有机物参加反应,有 有机物参加反应,有 离子通过交换膜 离子通过交换膜 |
您最近一年使用:0次
3 . 氢能是一种重要的绿色能源,在实现“碳中和”与“碳达峰”目标中起到重要作用。
Ⅰ.甲醇―水催化重整可获得氢气。
(1)表中数据是该反应中相关物质的标准摩尔生成焓(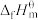 )数据(标准摩尔生成焓是指在298.15K、100kPa下由稳定态单质生成1mol化合物时的焓变)。
)数据(标准摩尔生成焓是指在298.15K、100kPa下由稳定态单质生成1mol化合物时的焓变)。
则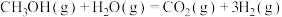 △H=
△H=___________ kJ∙mol-1,该反应在___________ (填“高温”“低温”或“任意温度”)下能自发进行。
Ⅱ.乙醇―水催化重整亦可获得,主要反应如下:
反应①:
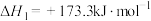
反应②:

(2)向恒容密闭容器中充入1mol 和3mol
和3mol 发生上述反应①和②,初始时体系压强为100kPa.平衡时
发生上述反应①和②,初始时体系压强为100kPa.平衡时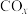 的分布分数
的分布分数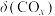 、
、 的产率随温度的变化曲线如图所示。
的产率随温度的变化曲线如图所示。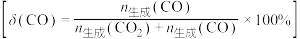
___________ (写出2条)。
②200℃以后,解释曲线a随温度变化趋势的原因:___________ 。
③温度为500℃时,反应经10min达到平衡,此时乙醇的转化率为60%,则0~10min内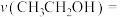
___________ kPa∙min-1,该温度下,反应②的Kp=___________ (保留小数点后两位)。
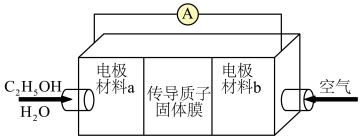
(3)乙醇燃料电池(电极材料a和b均为惰性电极)广泛应用于微型电源、能源汽车、家用电源、国防等领域,工作原理如图所示,写出负极的电极反应式:___________ ,当转移1.2mol电子时,正极消耗的氧气的体积为___________ L(标准状况下)。
Ⅰ.甲醇―水催化重整可获得氢气。
(1)表中数据是该反应中相关物质的标准摩尔生成焓(
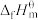 )数据(标准摩尔生成焓是指在298.15K、100kPa下由稳定态单质生成1mol化合物时的焓变)。
)数据(标准摩尔生成焓是指在298.15K、100kPa下由稳定态单质生成1mol化合物时的焓变)。| 物质 |  |  |  |  |
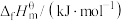 | 0 | ―393.5 | ―241.8 | ―200.7 |
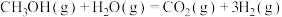 △H=
△H=Ⅱ.乙醇―水催化重整亦可获得,主要反应如下:
反应①:

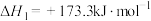
反应②:


(2)向恒容密闭容器中充入1mol
 和3mol
和3mol 发生上述反应①和②,初始时体系压强为100kPa.平衡时
发生上述反应①和②,初始时体系压强为100kPa.平衡时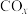 的分布分数
的分布分数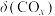 、
、 的产率随温度的变化曲线如图所示。
的产率随温度的变化曲线如图所示。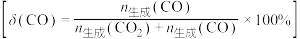
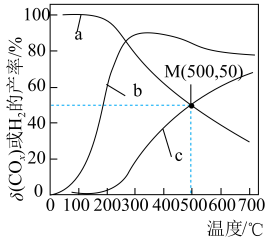
②200℃以后,解释曲线a随温度变化趋势的原因:
③温度为500℃时,反应经10min达到平衡,此时乙醇的转化率为60%,则0~10min内
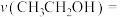
(3)乙醇燃料电池(电极材料a和b均为惰性电极)广泛应用于微型电源、能源汽车、家用电源、国防等领域,工作原理如图所示,写出负极的电极反应式:
您最近一年使用:0次
2024-05-19更新
|
107次组卷
|
4卷引用:T29-原理综合题
解题方法
4 . 某科研团队开发出一种高能量和转化效率的二次电池,其放电原理如图所示,其中电极M的材料为多孔石墨,充放电过程中,电极N上完成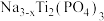 和
和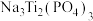 之间的转化。下列说法错误的是
之间的转化。下列说法错误的是
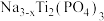 和
和 之间的转化。下列说法错误的是
之间的转化。下列说法错误的是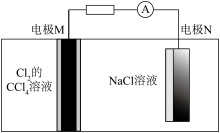
| A.放电时,电极M作正极 |
B.放电时, 从电极M向电极N迁移 从电极M向电极N迁移 |
C.充电时,导线中流过1mol ,NaCl溶液的质量减小35.5g ,NaCl溶液的质量减小35.5g |
| D.充、放电时,电极N上均为Ti元素的化合价发生变化 |
您最近一年使用:0次
名校
5 . 镁锂双盐电池是新型二次离子电池,其放电时的工作原理如图所示。
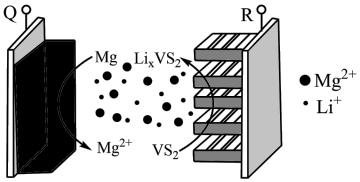
A.充电时, 和 和 均向Q极区移动 均向Q极区移动 |
B.充电时,阴极的电极反应式为 |
| C.放电时,Q电极Mg失去电子,电子经导线流向R电极 |
D.电池工作时,若外电路中转移电子的物质的量为 ,则两极的质量变化值相差0.5g ,则两极的质量变化值相差0.5g |
您最近一年使用:0次
2024-04-04更新
|
634次组卷
|
6卷引用:T12-电化学基础
(已下线)T12-电化学基础河南省濮阳市2024届高三下学期第二次模拟考试理科综合化学试题河南省濮阳市2024届高三第一次模拟考试理综-化学试题河南省漯河市高级中学2023-2024学年高三下学期4月月考化学试题(已下线)压轴题06?电化学原理综合分析(6大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)山西省晋中市2024届高三第二次优生测试理综合化学试题-
6 . 人类利用二氧化碳合成淀粉对社会的发展起着重要作用,合成过程首先是利用二氧化碳制备甲醇,合成甲醇的反应为
 。回答下列问题:
。回答下列问题:
(1)已知:
①
 ;
;
②
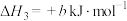 ;
;
③a、b均为大于零的数,且a>b。

_______ (用含a、b的式子表示) 。某研究小组设计合成
。某研究小组设计合成 的路线及
的路线及 的部分应用如图所示,图中熔融碳酸盐燃料电池的正极电极反应式为
的部分应用如图所示,图中熔融碳酸盐燃料电池的正极电极反应式为__________________ 。________________ 。 的产率。为了研究水分子对该反应机制的内在影响,我国学者利用计算机模拟,研究添加适量水蒸气前后对能垒较大的反应历程能量变化的影响(如图所示,吸附在催化剂表面的物种用*标注)。
的产率。为了研究水分子对该反应机制的内在影响,我国学者利用计算机模拟,研究添加适量水蒸气前后对能垒较大的反应历程能量变化的影响(如图所示,吸附在催化剂表面的物种用*标注)。___________________ 。
②结合图3及学过的知识推测,有水参与的历程,反应速率加快的原因是_____________________ 。
(4)在T℃时,将6mol (g)和12mol
(g)和12mol  (g)充入容积为10L的恒容容器中,只发生
(g)充入容积为10L的恒容容器中,只发生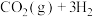
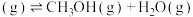 ,初始压强为
,初始压强为 kPa,测得体系中剩余
kPa,测得体系中剩余 (g)的物质的量随时间变化如图中状态Ⅰ所示。
(g)的物质的量随时间变化如图中状态Ⅰ所示。
__________  ,该反应的平衡常数
,该反应的平衡常数
_________  。(用平衡分压代替平衡浓度计算,列出计算式)
。(用平衡分压代替平衡浓度计算,列出计算式)
②保持投料量不变,仅改变某一个条件后,测得 随时间变化如图中状态Ⅲ所示,与状态Ⅰ相比,状态Ⅲ改变的条件可能是
随时间变化如图中状态Ⅲ所示,与状态Ⅰ相比,状态Ⅲ改变的条件可能是___________________ 。

 。回答下列问题:
。回答下列问题:(1)已知:
①

 ;
;②

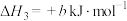 ;
;③a、b均为大于零的数,且a>b。

 。某研究小组设计合成
。某研究小组设计合成 的路线及
的路线及 的部分应用如图所示,图中熔融碳酸盐燃料电池的正极电极反应式为
的部分应用如图所示,图中熔融碳酸盐燃料电池的正极电极反应式为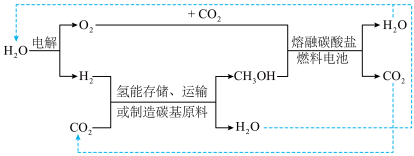
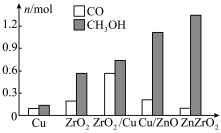
 的产率。为了研究水分子对该反应机制的内在影响,我国学者利用计算机模拟,研究添加适量水蒸气前后对能垒较大的反应历程能量变化的影响(如图所示,吸附在催化剂表面的物种用*标注)。
的产率。为了研究水分子对该反应机制的内在影响,我国学者利用计算机模拟,研究添加适量水蒸气前后对能垒较大的反应历程能量变化的影响(如图所示,吸附在催化剂表面的物种用*标注)。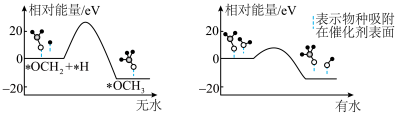
②结合图3及学过的知识推测,有水参与的历程,反应速率加快的原因是
(4)在T℃时,将6mol
 (g)和12mol
(g)和12mol  (g)充入容积为10L的恒容容器中,只发生
(g)充入容积为10L的恒容容器中,只发生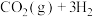
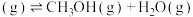 ,初始压强为
,初始压强为 kPa,测得体系中剩余
kPa,测得体系中剩余 (g)的物质的量随时间变化如图中状态Ⅰ所示。
(g)的物质的量随时间变化如图中状态Ⅰ所示。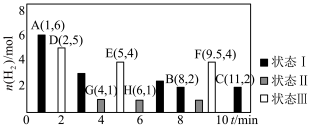
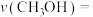
 ,该反应的平衡常数
,该反应的平衡常数
 。(用平衡分压代替平衡浓度计算,列出计算式)
。(用平衡分压代替平衡浓度计算,列出计算式)②保持投料量不变,仅改变某一个条件后,测得
 随时间变化如图中状态Ⅲ所示,与状态Ⅰ相比,状态Ⅲ改变的条件可能是
随时间变化如图中状态Ⅲ所示,与状态Ⅰ相比,状态Ⅲ改变的条件可能是
您最近一年使用:0次
2024-03-22更新
|
746次组卷
|
6卷引用:T29-原理综合题
(已下线)T29-原理综合题河南省新乡市2024届高三第二次模拟考试理综-化学试题2024届青海省百所名校高三下学期二模理科综合试题-高中化学(已下线)化学(全国卷旧教材)-2024年高考押题预测卷2024届四川省绵阳市东辰中学高三下学期模拟考试(一)理科综合试题-高中化学2024届宁夏回族自治区石嘴山市平罗县平罗中学高三下学期模拟预测理综试题-高中化学
7 . 某品牌全电动汽车使用的是钴酸锂电池,该新型锂电池的工作原理如图所示,其电池总反应为 .下列有关说法错误的是
.下列有关说法错误的是
 .下列有关说法错误的是
.下列有关说法错误的是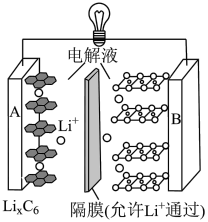
A.放电时, 电极为正极,电极反应式为 电极为正极,电极反应式为 |
B.放电时, 从负极脱嵌,经电解液和隔膜嵌入正极 从负极脱嵌,经电解液和隔膜嵌入正极 |
C.充电时, 电极为阳极,电极反应式为 电极为阳极,电极反应式为 |
D.放电时,若转移 电子,B电极将增重 电子,B电极将增重 |
您最近一年使用:0次
8 . 电解苯酚的乙腈(CH3CN)水溶液可在电极上直接合成扑热息痛(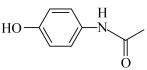 )。装置如图,其中电极材料均为石墨。下列说法
)。装置如图,其中电极材料均为石墨。下列说法

| A.电极a为负极 |
B.c电极反应式为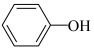 +CH3CN+H2O-2e- +CH3CN+H2O-2e-  +2H+ +2H+ |
| C.装置工作时,乙室溶液pH减小 |
| D.合成1mol扑热息痛,理论上甲室质量增重64g |
您最近一年使用:0次
2024-03-09更新
|
518次组卷
|
10卷引用:河南省湘豫名校2023届高三下学期第一次模拟化学试题变式题(选择题11-13)
(已下线)河南省湘豫名校2023届高三下学期第一次模拟化学试题变式题(选择题11-13)(已下线)专题12 电化学的综合应用山东省烟台市、德州市、滨州市2023届高三一模考试化学试题(已下线)先机卷 05 -【热题狂飙】2023年高考化学样卷(全国卷专用)山西省2023-2024学年高三上学期10月月考化学试题山东省部分学校2024届高三上学期10月大联考化学试题山西省运城市金科大联考2023-2024学年高三上学期10月质量检测化学试题北京大学附属中学预科部2023-2024学年高三下学期3月阶段练习化学试题福建省厦门双十中学2024届高三模拟预测化学试题黑龙江省大庆市实验中学实验二部2023-2024学年高三下学期得分训练化学试题(四)
名校
解题方法
9 . 纳基-海水可充电电池总反应为 ,其工作原理如图所示。
,其工作原理如图所示。

下列说法错误的是
 ,其工作原理如图所示。
,其工作原理如图所示。
下列说法错误的是
| A.充电时,钠基材料连接电源的负极 | B.充放电时,固体电解质都只允许 通过 通过 |
C.充电时,空气电极能促进海水中的 放电 放电 | D.放电时,正极反应式为 |
您最近一年使用:0次
名校
10 . 科学家设计了一种具有石墨正极的高容量可充电 电池,原理如图所示。氯化铝(
电池,原理如图所示。氯化铝( )溶解在亚硫酰氯(
)溶解在亚硫酰氯( )中,以氟化物(LiFSI)为溶剂。下列叙述正确的是
)中,以氟化物(LiFSI)为溶剂。下列叙述正确的是
 电池,原理如图所示。氯化铝(
电池,原理如图所示。氯化铝( )溶解在亚硫酰氯(
)溶解在亚硫酰氯( )中,以氟化物(LiFSI)为溶剂。下列叙述正确的是
)中,以氟化物(LiFSI)为溶剂。下列叙述正确的是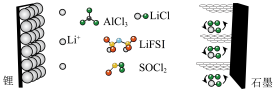
A.放电时,电解质溶液可以是 水溶液 水溶液 |
B.放电时,石墨极的电极反应式为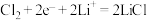 |
| C.充电时,石墨极与电源负极连接 |
D.充电时,转移 个电子时锂电极理论上消耗14g锂 个电子时锂电极理论上消耗14g锂 |
您最近一年使用:0次
2024-02-25更新
|
192次组卷
|
6卷引用:T12-电化学基础



