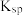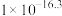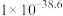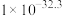解题方法
1 . 四氧化三锰( )广泛应用于软磁材料、电池材料等制备领域。一种以低品位锰矿(含
)广泛应用于软磁材料、电池材料等制备领域。一种以低品位锰矿(含 、
、 、MnOOH及少量
、MnOOH及少量 、
、 、
、 )为原料生产
)为原料生产 的工艺流程如下:
的工艺流程如下:
①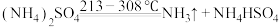
②已知:25℃时相关物质的 见表
见表
③当 时,
时, 开始溶解
开始溶解
回答下列问题:
(1)Mn元素在周期表中的______ 区,从核外电子排布的角度,稳定性Mn(Ⅱ)______ Mn(Ⅲ)(填“>”或“<”)。
(2)“溶浸”过程中, 可用
可用______ (填标号)代替,理由是______ 。
A.盐酸 B.硫酸 C.硝酸
(3)加入 调节
调节 时,杂质离子是否能完全沉淀
时,杂质离子是否能完全沉淀______ (填“是”或“否”),此时“滤渣2”的主要成分是______ 。(溶液中离子浓度 视为完全沉淀)
视为完全沉淀)
(4)“沉锰”步骤中,杂质含量直接影响 的品位,实验测得温度对
的品位,实验测得温度对 中硫酸根含量的影响如图所示,实际生产中综合考虑选择50℃为宜,不选择更高温度的原因是
中硫酸根含量的影响如图所示,实际生产中综合考虑选择50℃为宜,不选择更高温度的原因是______ 。“母液”中,能转换成可循环利用的物质是______ 。 是制备电池正极材料
是制备电池正极材料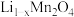 的优质原料,该电极在电池放电过程中转化为
的优质原料,该电极在电池放电过程中转化为 ,写出正极放电时的电极反应式
,写出正极放电时的电极反应式______ 。
 )广泛应用于软磁材料、电池材料等制备领域。一种以低品位锰矿(含
)广泛应用于软磁材料、电池材料等制备领域。一种以低品位锰矿(含 、
、 、MnOOH及少量
、MnOOH及少量 、
、 、
、 )为原料生产
)为原料生产 的工艺流程如下:
的工艺流程如下: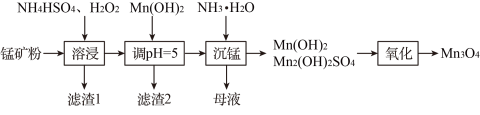
①
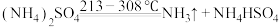
②已知:25℃时相关物质的
 见表
见表③当
 时,
时, 开始溶解
开始溶解物质 |
|
|
|
|
|
|
|
|
|
(1)Mn元素在周期表中的
(2)“溶浸”过程中,
 可用
可用A.盐酸 B.硫酸 C.硝酸
(3)加入
 调节
调节 时,杂质离子是否能完全沉淀
时,杂质离子是否能完全沉淀 视为完全沉淀)
视为完全沉淀)(4)“沉锰”步骤中,杂质含量直接影响
 的品位,实验测得温度对
的品位,实验测得温度对 中硫酸根含量的影响如图所示,实际生产中综合考虑选择50℃为宜,不选择更高温度的原因是
中硫酸根含量的影响如图所示,实际生产中综合考虑选择50℃为宜,不选择更高温度的原因是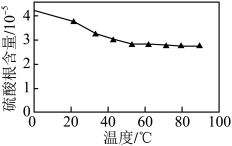
 是制备电池正极材料
是制备电池正极材料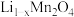 的优质原料,该电极在电池放电过程中转化为
的优质原料,该电极在电池放电过程中转化为 ,写出正极放电时的电极反应式
,写出正极放电时的电极反应式
您最近一年使用:0次
名校
2 . 一次性纸电池加水就可以激活,可用来驱动低功率电子器件,其基本结构如图所示,下列说法错误的是

| A.用乙醇代替水也可以激活该电池 |
| B.“油墨混有锌粉”为电池的负极 |
C.正极电极反应式: |
| D.激活时水用量过多浸没电池,可能造成电源无法正常工作 |
您最近一年使用:0次
2024-03-05更新
|
555次组卷
|
3卷引用:选择题1-5
名校
3 . 一种新型短路膜电池分离CO2装置如下图所示。下列说法中正确的是
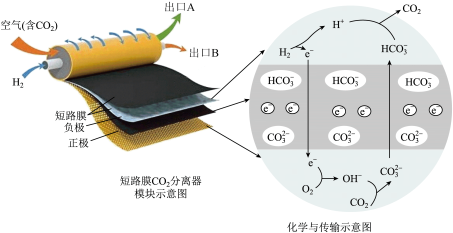

| A.负极反应为:H2−2e−+2OH−=H2O |
| B.正极反应消耗22.4LO2,理论上需要转移4mol电子 |
| C.短路膜和常见的离子交换膜不同,它既能传递离子,还可以传递电子 |
| D.该装置用于空气中CO2的捕获,CO2最终由出口A流出 |
您最近一年使用:0次
解题方法
4 .  转化利用对化解全球环境生态危机助力全球“碳达峰、碳中和”目标的实现具有重要意义。化学工作者致力于将
转化利用对化解全球环境生态危机助力全球“碳达峰、碳中和”目标的实现具有重要意义。化学工作者致力于将 转化为各种化工原料。
转化为各种化工原料。
Ⅰ.早在二十世纪初,工业上以 和
和 为原料在一定温度和压强下合成尿素。反应分两步:①
为原料在一定温度和压强下合成尿素。反应分两步:① 和
和 生成
生成 ;②
;② 分解生成尿素。
分解生成尿素。
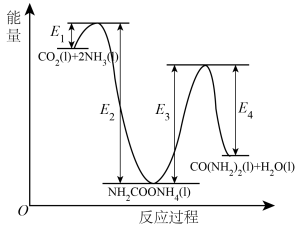
(1)活化能:反应①反应___________ ②(填“>”、“<”或“=”);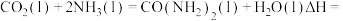
___________ (用含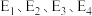 的式子表示)。
的式子表示)。
II.我国科学家研究 电池,取得了重大科研成果。
电池,取得了重大科研成果。 电池中,反应产物为
电池中,反应产物为 ;和单质碳,正极
;和单质碳,正极 电还原后与锂离子结合形成
电还原后与锂离子结合形成 按以下4个步骤进行:
按以下4个步骤进行:
① ;
;
②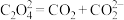 ;
;
③___________;
④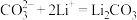
(2)写出步骤③中 与
与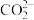 反应的离子方程式
反应的离子方程式___________ 。
III.利用 和重整技术可获得合成气(主要成分为
和重整技术可获得合成气(主要成分为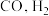 ),重整过程中反应的热化学方程式如下:
),重整过程中反应的热化学方程式如下:
反应i: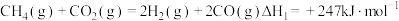
反应ii: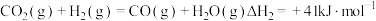
不同配比随温度变化对出口合成气中 的影响如下图所示
的影响如下图所示
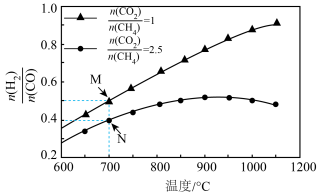
(3)对于反应 ,试比较
,试比较 点和
点和 点
点 的转化率:
的转化率:
___________  (填“>”、“<”或“=”下同);平衡常数
(填“>”、“<”或“=”下同);平衡常数
___________  ,当
,当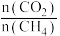 一定,有利于提高
一定,有利于提高 平衡转化率的反应条件是
平衡转化率的反应条件是___________ (填序号)。
A.高温高压 B.高温低压 C.低温高压 D.低温低压
(4)当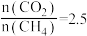 ,温度高于
,温度高于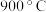 ,
, 减小的原因可能是
减小的原因可能是___________ 。
 转化利用对化解全球环境生态危机助力全球“碳达峰、碳中和”目标的实现具有重要意义。化学工作者致力于将
转化利用对化解全球环境生态危机助力全球“碳达峰、碳中和”目标的实现具有重要意义。化学工作者致力于将 转化为各种化工原料。
转化为各种化工原料。Ⅰ.早在二十世纪初,工业上以
 和
和 为原料在一定温度和压强下合成尿素。反应分两步:①
为原料在一定温度和压强下合成尿素。反应分两步:① 和
和 生成
生成 ;②
;② 分解生成尿素。
分解生成尿素。
(1)活化能:反应①反应
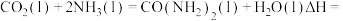
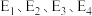 的式子表示)。
的式子表示)。II.我国科学家研究
 电池,取得了重大科研成果。
电池,取得了重大科研成果。 电池中,反应产物为
电池中,反应产物为 ;和单质碳,正极
;和单质碳,正极 电还原后与锂离子结合形成
电还原后与锂离子结合形成 按以下4个步骤进行:
按以下4个步骤进行:①
 ;
;②
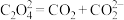 ;
;③___________;
④
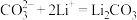
(2)写出步骤③中
 与
与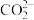 反应的离子方程式
反应的离子方程式III.利用
 和重整技术可获得合成气(主要成分为
和重整技术可获得合成气(主要成分为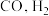 ),重整过程中反应的热化学方程式如下:
),重整过程中反应的热化学方程式如下:反应i:
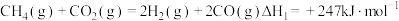
反应ii:
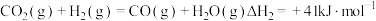
不同配比随温度变化对出口合成气中
 的影响如下图所示
的影响如下图所示
(3)对于反应
 ,试比较
,试比较 点和
点和 点
点 的转化率:
的转化率:
 (填“>”、“<”或“=”下同);平衡常数
(填“>”、“<”或“=”下同);平衡常数
 ,当
,当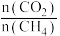 一定,有利于提高
一定,有利于提高 平衡转化率的反应条件是
平衡转化率的反应条件是A.高温高压 B.高温低压 C.低温高压 D.低温低压
(4)当
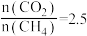 ,温度高于
,温度高于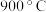 ,
, 减小的原因可能是
减小的原因可能是
您最近一年使用:0次
解题方法
5 . 钾—氧气电池的工作原理如图。关于该电池,下列说法正确的是


A.电解质 可能是 可能是 的水溶液 的水溶液 |
B.放电时电流由 电极沿导线流向多孔碳纸 电极沿导线流向多孔碳纸 |
C.放电时多孔碳纸上发生反应: |
D.为铅酸蓄电池充电时, 电极应与其正极相连 电极应与其正极相连 |
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
6 . 中科院研究者研发出世界首例室温条件以氢负离子为导体的新型电池,如以氢化镧(LaHx)为电解质的电池的工作原理如图所示:
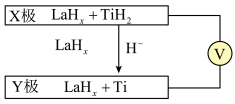
下列说法正确 的是

下列说法
| A.电势:Y>X | B.电池要保持无水干燥环境 |
| C.总反应式为Ti+H2=TiH2 | D.X极的电极反应式为2H--2e-=H2↑ |
您最近一年使用:0次
名校
解题方法
7 . 火星大气中含有大量 ,一种有
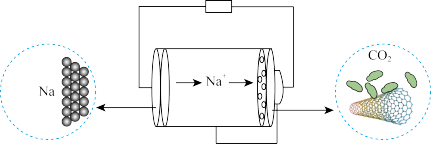
,一种有 参加反应的新型全固态电池有望为火星探测器供电。该电池以金属钠和碳纳米管作为两极(如图所示),放电的总反应为
参加反应的新型全固态电池有望为火星探测器供电。该电池以金属钠和碳纳米管作为两极(如图所示),放电的总反应为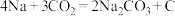 ,下列说法不正确的是
,下列说法不正确的是
 ,一种有
,一种有 参加反应的新型全固态电池有望为火星探测器供电。该电池以金属钠和碳纳米管作为两极(如图所示),放电的总反应为
参加反应的新型全固态电池有望为火星探测器供电。该电池以金属钠和碳纳米管作为两极(如图所示),放电的总反应为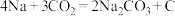 ,下列说法不正确的是
,下列说法不正确的是
A.该电池的介质可以选择 溶液 溶液 |
| B.金属Na作负极,发生氧化反应 |
C.正极反应式: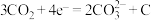 |
| D.工作时电子从Na电极经导线流向碳纳米管电极 |
您最近一年使用:0次
2023-11-16更新
|
930次组卷
|
4卷引用:选择题1-5
名校
解题方法
8 . 电化学原理在工农业生产中有重要应用。已知N2H4是一种重要的清洁高能燃料,产物无污染。根据如图所示装置回答下列问题(C1~C6均为石墨电极,假设各装置在工作过程中溶液体积不变)

(1)甲装置C2电极为___________ 极,C1电极上的电极反应为 ___________
(2)装置中Ag电极上的电极反应为___________ ,若乙装置中溶液体积为400mL,开始时溶液pH为6,当电极上通过0.04mol电子时溶液pH约为___________ 。
(3)丙装置用于处理含高浓度硫酸钠的废水,同时获得硫酸、烧碱及氢气,膜X为___________ (填“阳离子”“阴离子”或“质子”)交换膜,当电极上通过0.04mol电子时,中间硫酸钠废水的质量改变___________ g(假定水分子不能通过膜X和膜Y)。
(4)电解一段时间后,丁装置中能观察到的现象是___________ ,丁装置中电解反应的总化学方程式为___________ 。

(1)甲装置C2电极为
(2)装置中Ag电极上的电极反应为
(3)丙装置用于处理含高浓度硫酸钠的废水,同时获得硫酸、烧碱及氢气,膜X为
(4)电解一段时间后,丁装置中能观察到的现象是
您最近一年使用:0次
2023-11-07更新
|
598次组卷
|
4卷引用:电化学原理及应用
9 . 我国科学家设计的“海泥电池”,既可用于深海水下仪器的电源补给,又有利于海洋环境污染治理,其中微生物代谢产物显酸性,电池工作原理如图所示。下列说法正确的是
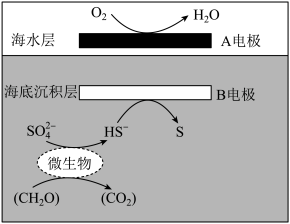

| A.B电极为正极 |
| B.微生物代谢反应中,氧化剂与还原剂的物质的量之比为1:2 |
| C.B电极的电极反应式为HS-+2e- = S↓+H+ |
| D.质子从海水层通过交接面向海底沉积层移动 |
您最近一年使用:0次
名校
解题方法
10 . 党的二十大报告提出,加强基础研究,突出原创,鼓励自由探索。一氧化氮-空气质子交换膜燃料电池将化学能转化为电能,实现了制硝酸、发电环保三位一体的结合。如图所示,某同学设计用该电池探究将雾霾中的SO2、NO转化为(NH4)2SO4的原理和粗铜的精炼原理。

(1)燃料电池放电过程中负极的电极反应式___________ 。
(2)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,CuSO4溶液的浓度将___________ (填“增大”、“减小”或“不变”)。
(3)乙装置中物质A是___________ (填化学式);阴极的电极反应式是___________ 。
(4)若在标准状况下,甲装置有11.2LO2参加反应,则乙装置中转化SO2和NO的物质的量共有___________ mol;丙装置中阴极析出铜的质量为___________ g。

(1)燃料电池放电过程中负极的电极反应式
(2)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,CuSO4溶液的浓度将
(3)乙装置中物质A是
(4)若在标准状况下,甲装置有11.2LO2参加反应,则乙装置中转化SO2和NO的物质的量共有
您最近一年使用:0次