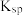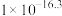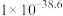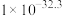2024·河北邯郸·一模
解题方法
1 . 硫脲(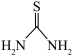 )可用作橡胶的硫化促进剂、金属矿物的浮选剂。已知硫脲易溶于水,易被氧化,受热时部分发生异构化反应而生成硫氰化铵。实验室制备硫脲的装置如图所示(夹持和加热装置略)。
)可用作橡胶的硫化促进剂、金属矿物的浮选剂。已知硫脲易溶于水,易被氧化,受热时部分发生异构化反应而生成硫氰化铵。实验室制备硫脲的装置如图所示(夹持和加热装置略)。

(1)仪器a的名称是
(2)反应开始时,先打开
 ,当观察到
,当观察到 ,这样操作的目的是
,这样操作的目的是(3)装置B中除生成硫脲外,还生成一种碱,写出装置B中发生反应的化学方程式:
(4)装置B反应后的液体经分离、提纯、烘干可得产品。测定产品的纯度:
称取m g产品,加水溶解配成250 mL溶液,取25 mL于锥形瓶中,加入稀硫酸酸化,用
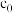 mol⋅L
mol⋅L 酸性
酸性 标准溶液滴定,滴定至终点时消耗标准溶液V mL(已知滴定时,硫脲转化为
标准溶液滴定,滴定至终点时消耗标准溶液V mL(已知滴定时,硫脲转化为 、
、 和
和 ,假设杂质不参与反应)。
,假设杂质不参与反应)。①该实验中滴加酸性
 标准溶液的正确操作是
标准溶液的正确操作是
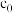 、V的代数式表示)。
、V的代数式表示)。③若滴定前平视酸性
 标准溶液液面读数,滴定后俯视液面读数,计算得到的待测产品纯度比实际纯度
标准溶液液面读数,滴定后俯视液面读数,计算得到的待测产品纯度比实际纯度
您最近一年使用:0次
2024·重庆·模拟预测
解题方法
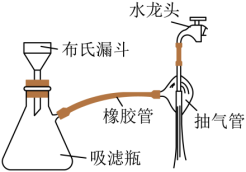
2 . 实验室制备三氯化六氨合钴(Ⅲ){[ Co(NH3)6]Cl3 }的装置如图1所示。
实验步骤:在三颈烧瓶中加入活性炭(作催化剂)、CoCl2和NH4Cl混合溶液,滴入浓氨水,充分反应后,再滴入双氧水,且水浴控温在55℃左右,反应结束后,将反应混合物趁热过滤,待滤液冷却后加入适量浓盐酸,冰水冷却抽滤、乙醇洗涤、干燥,得到[ Co(NH3)6]Cl3晶体。已知:[ Co(NH3)6]2+具有CoCl2和NH4Cl较强还原性,Co2+不易被氧化, 。
。
(1)仪器a的名称是_______________ ,仪器c中无水CaCl2的作用是_______________ 。
(2)先加入浓氨水的目的是_______________ ,水浴控制温度为55℃的原因是_______________ 。
(3)CoCl2制备[ Co(NH3)6]Cl3的化学方程式为_______________ 。
(4)待滤液冷却后加入适量浓盐酸的作用是_______________ ,抽滤采用如图2的装置,抽滤的优点是_______________ 。
(5)为测定产品中钴的含量,进行下列实验:
I.称取4.0g产品,加入足量NaOH溶液蒸出NH3,再加入稀硫酸,使[ Co(NH3)6]Cl3全部转化为Co3+,然后将溶液配制成250mL,取25.00mL于锥形瓶,加入过量KI溶液(将Co3+还原成Co2+),用0.1000mol.L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液13.10mL。(已知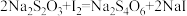 )
)
Ⅱ.另取与步骤I中等量的KI溶液于锥形瓶中,用上述标准溶液进行滴定,消耗Na2S2O3标准溶液1.10mL。
①样品中钴元素的质量分数为_______________ %。
②若步骤Ⅱ滴定前读数准确,滴定后的俯视读数,测定结果将_______________ (填“偏大”“偏小”或“不变”)。
实验步骤:在三颈烧瓶中加入活性炭(作催化剂)、CoCl2和NH4Cl混合溶液,滴入浓氨水,充分反应后,再滴入双氧水,且水浴控温在55℃左右,反应结束后,将反应混合物趁热过滤,待滤液冷却后加入适量浓盐酸,冰水冷却抽滤、乙醇洗涤、干燥,得到[ Co(NH3)6]Cl3晶体。已知:[ Co(NH3)6]2+具有CoCl2和NH4Cl较强还原性,Co2+不易被氧化,
 。
。
(1)仪器a的名称是
(2)先加入浓氨水的目的是
(3)CoCl2制备[ Co(NH3)6]Cl3的化学方程式为
(4)待滤液冷却后加入适量浓盐酸的作用是
(5)为测定产品中钴的含量,进行下列实验:
I.称取4.0g产品,加入足量NaOH溶液蒸出NH3,再加入稀硫酸,使[ Co(NH3)6]Cl3全部转化为Co3+,然后将溶液配制成250mL,取25.00mL于锥形瓶,加入过量KI溶液(将Co3+还原成Co2+),用0.1000mol.L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液13.10mL。(已知
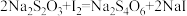 )
)Ⅱ.另取与步骤I中等量的KI溶液于锥形瓶中,用上述标准溶液进行滴定,消耗Na2S2O3标准溶液1.10mL。
①样品中钴元素的质量分数为
②若步骤Ⅱ滴定前读数准确,滴定后的俯视读数,测定结果将
您最近一年使用:0次
2024·河北邯郸·一模
3 . 有机物Ⅰ是合成二萜化合物的中间体,其合成路线如图所示(-Ph表示苯基,部分反应条件省略):
(1)化合物A的化学名称为______ ;C+E→F的反应类型为______ 。
(2)G→H的反应条件为______ ;F的结构简式为______ 。
(3)H→I的化学方程式为____________ 。
(4)化合物E有多种同分异构体,写出符合下列条件的同分异构体的结构简式:______ (任填一种)。
③其水解产物遇FeCl3溶液显色
④核磁共振氢谱显示只有3种不同化学环境的氢原子
(5)设计以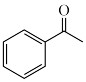 、HCHO、NH(CH3)2为原料制备
、HCHO、NH(CH3)2为原料制备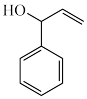 的合成路线:
的合成路线:____________ (无机试剂任选)。
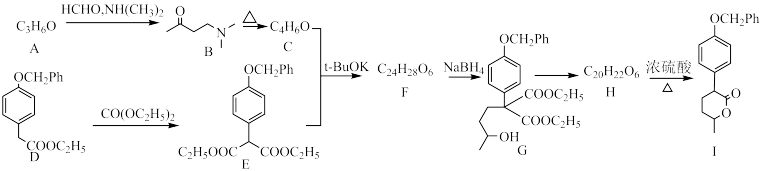
已知:ⅰ.
ⅱ.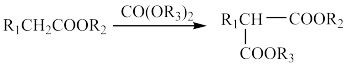
ⅲ.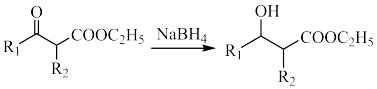
ⅳ.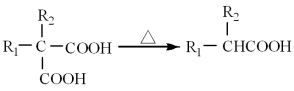
(1)化合物A的化学名称为
(2)G→H的反应条件为
(3)H→I的化学方程式为
(4)化合物E有多种同分异构体,写出符合下列条件的同分异构体的结构简式:
①含有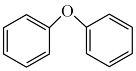 结构
结构
③其水解产物遇FeCl3溶液显色
④核磁共振氢谱显示只有3种不同化学环境的氢原子
(5)设计以
 、HCHO、NH(CH3)2为原料制备
、HCHO、NH(CH3)2为原料制备 的合成路线:
的合成路线:
您最近一年使用:0次
2024·广西南宁·一模
4 . 甲烷水蒸气催化重整是制备高纯氢的方法之一。
甲烷水蒸气催化重整发生如下反应:
反应i.
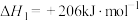
反应ⅱ.

(1)已知反应ⅱ中相关的化学键键能数据如下:
由此计算
______  。
。
(2)为了提高反应中甲烷的平衡转化率,理论上可采取的措施是______。
(3)把甲烷和水蒸气按物质的量之比1∶3通入反应器中,其他条件不变,在不同温度下探究CaO对平衡时干燥出口气中 物质的量分数的影响,结果如下:
物质的量分数的影响,结果如下:______ K(700℃)(填“大于”、“等于”或“小于”)。
②在400~600℃范围内,反应器中有CaO能大幅提高 物质的量分数,原因是
物质的量分数,原因是______ (用化学方程式表示)。
(4)某温度下,在体积为1L的容器中加入1mol 、3mol水蒸气进行催化重整反应,达到平衡时
、3mol水蒸气进行催化重整反应,达到平衡时 的总转化率为80%,CO的浓度为
的总转化率为80%,CO的浓度为 。
。 的平衡浓度为
的平衡浓度为______  ,反应i的平衡常数为
,反应i的平衡常数为______  (保留一位小数)。
(保留一位小数)。
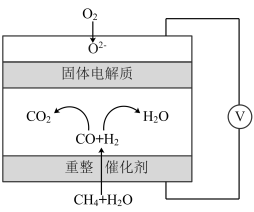
(5)一种高性能甲烷燃料电池的工作原理如图所示。理论上当正极消耗气体的体积为44.8L(标准状况)时,电路中转移的电子数为______  。
。
甲烷水蒸气催化重整发生如下反应:
反应i.

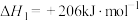
反应ⅱ.


(1)已知反应ⅱ中相关的化学键键能数据如下:
化学键 | H―H | H―O | C―H | C=O |
E/( | 436 | 465 | 413 | 745 |

 。
。(2)为了提高反应中甲烷的平衡转化率,理论上可采取的措施是______。
| A.恒容时通入氮气 | B.升高温度 | C.及时分离氢气 | D.选择合适的催化剂 |
(3)把甲烷和水蒸气按物质的量之比1∶3通入反应器中,其他条件不变,在不同温度下探究CaO对平衡时干燥出口气中
 物质的量分数的影响,结果如下:
物质的量分数的影响,结果如下: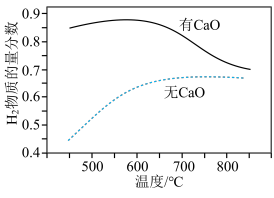
②在400~600℃范围内,反应器中有CaO能大幅提高
 物质的量分数,原因是
物质的量分数,原因是(4)某温度下,在体积为1L的容器中加入1mol
 、3mol水蒸气进行催化重整反应,达到平衡时
、3mol水蒸气进行催化重整反应,达到平衡时 的总转化率为80%,CO的浓度为
的总转化率为80%,CO的浓度为 。
。 的平衡浓度为
的平衡浓度为 ,反应i的平衡常数为
,反应i的平衡常数为 (保留一位小数)。
(保留一位小数)。(5)一种高性能甲烷燃料电池的工作原理如图所示。理论上当正极消耗气体的体积为44.8L(标准状况)时,电路中转移的电子数为
 。
。
您最近一年使用:0次
23-24高三下·四川绵阳·阶段练习
名校
解题方法
5 . 水仙环素是一种植物生长调节剂,具有抗毒性等作用,化合物H是水仙环素合成的中间产物。其合成路线如图: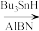 R-H
R-H
回答下列问题:
(1)B中官能团的名称为________ 。
(2)B→C的化学反应方程式为________ 。
(3)A→B,F→H分别的反应类型为_______ 、________ 。
(4)E的结构简式为_______ 。
(5)F与G的反应为最理想的“原子经济性反应”,则G的名称为_______ 。
(6)H有_______ 个手性碳原子。
(7)芳香族化合物K比D多了2个碳原子和2个氢原子,且K能与碳酸氢钠放CO2,则满足条件的K有_______ 种结构。
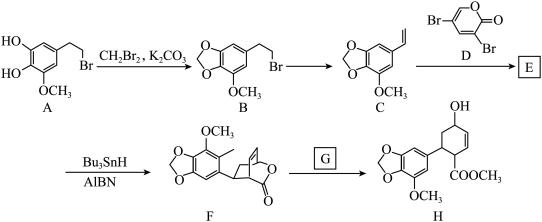
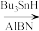 R-H
R-H回答下列问题:
(1)B中官能团的名称为
(2)B→C的化学反应方程式为
(3)A→B,F→H分别的反应类型为
(4)E的结构简式为
(5)F与G的反应为最理想的“原子经济性反应”,则G的名称为
(6)H有
(7)芳香族化合物K比D多了2个碳原子和2个氢原子,且K能与碳酸氢钠放CO2,则满足条件的K有
您最近一年使用:0次
2024·广西南宁·一模
解题方法
6 . 四氧化三锰( )广泛应用于软磁材料、电池材料等制备领域。一种以低品位锰矿(含
)广泛应用于软磁材料、电池材料等制备领域。一种以低品位锰矿(含 、
、 、MnOOH及少量
、MnOOH及少量 、
、 、
、 )为原料生产
)为原料生产 的工艺流程如下:
的工艺流程如下:
①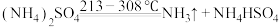
②已知:25℃时相关物质的 见表
见表
③当 时,
时, 开始溶解
开始溶解
回答下列问题:
(1)Mn元素在周期表中的______ 区,从核外电子排布的角度,稳定性Mn(Ⅱ)______ Mn(Ⅲ)(填“>”或“<”)。
(2)“溶浸”过程中, 可用
可用______ (填标号)代替,理由是______ 。
A.盐酸 B.硫酸 C.硝酸
(3)加入 调节
调节 时,杂质离子是否能完全沉淀
时,杂质离子是否能完全沉淀______ (填“是”或“否”),此时“滤渣2”的主要成分是______ 。(溶液中离子浓度 视为完全沉淀)
视为完全沉淀)
(4)“沉锰”步骤中,杂质含量直接影响 的品位,实验测得温度对
的品位,实验测得温度对 中硫酸根含量的影响如图所示,实际生产中综合考虑选择50℃为宜,不选择更高温度的原因是
中硫酸根含量的影响如图所示,实际生产中综合考虑选择50℃为宜,不选择更高温度的原因是______ 。“母液”中,能转换成可循环利用的物质是______ 。 是制备电池正极材料
是制备电池正极材料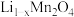 的优质原料,该电极在电池放电过程中转化为
的优质原料,该电极在电池放电过程中转化为 ,写出正极放电时的电极反应式
,写出正极放电时的电极反应式______ 。
 )广泛应用于软磁材料、电池材料等制备领域。一种以低品位锰矿(含
)广泛应用于软磁材料、电池材料等制备领域。一种以低品位锰矿(含 、
、 、MnOOH及少量
、MnOOH及少量 、
、 、
、 )为原料生产
)为原料生产 的工艺流程如下:
的工艺流程如下: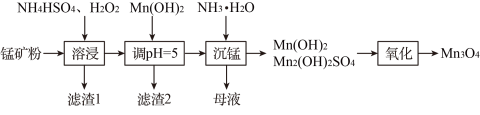
①
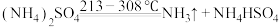
②已知:25℃时相关物质的
 见表
见表③当
 时,
时, 开始溶解
开始溶解物质 |
|
|
|
|
|
|
|
|
|
(1)Mn元素在周期表中的
(2)“溶浸”过程中,
 可用
可用A.盐酸 B.硫酸 C.硝酸
(3)加入
 调节
调节 时,杂质离子是否能完全沉淀
时,杂质离子是否能完全沉淀 视为完全沉淀)
视为完全沉淀)(4)“沉锰”步骤中,杂质含量直接影响
 的品位,实验测得温度对
的品位,实验测得温度对 中硫酸根含量的影响如图所示,实际生产中综合考虑选择50℃为宜,不选择更高温度的原因是
中硫酸根含量的影响如图所示,实际生产中综合考虑选择50℃为宜,不选择更高温度的原因是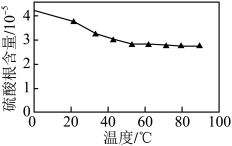
 是制备电池正极材料
是制备电池正极材料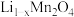 的优质原料,该电极在电池放电过程中转化为
的优质原料,该电极在电池放电过程中转化为 ,写出正极放电时的电极反应式
,写出正极放电时的电极反应式
您最近一年使用:0次
2024·黑龙江吉林·一模
7 . 艾氟康唑(化合物K)是一种用于治疗甲癣的三唑类抗真菌药物。K的一种路线如下(部分试剂和条件略去)。
(1)A的化学名称为________ 。
(2)D的结构简式为________ 。
(3)F中含氧官能团有羟基和________ 。
(4)F→G的反应包括两步,第二步为取代反应,则第一步的反应条件应选择________ 。
a.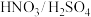 b.
b. c.
c.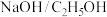 d.
d.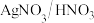
(5) 反应的化学方程式为
反应的化学方程式为________ 。
(6) 的同分异构体能同时满足以下三个条件的有
的同分异构体能同时满足以下三个条件的有________ 种(不考虑立体异构),其中能与碳酸氢钠浴液反应放出 ,核磁共振氢普有5组峰,且峰面积比为2∶1∶1∶1∶1的结构简式为
,核磁共振氢普有5组峰,且峰面积比为2∶1∶1∶1∶1的结构简式为________ (任写一种)。
①含有手性碳
②氟原子与苯环直接相连
③苯环上有3个取代基且不含其它环状结构

已知:①Boc为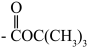
②
(1)A的化学名称为
(2)D的结构简式为
(3)F中含氧官能团有羟基和
(4)F→G的反应包括两步,第二步为取代反应,则第一步的反应条件应选择
a.
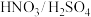 b.
b. c.
c.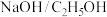 d.
d.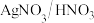
(5)
 反应的化学方程式为
反应的化学方程式为(6)
 的同分异构体能同时满足以下三个条件的有
的同分异构体能同时满足以下三个条件的有 ,核磁共振氢普有5组峰,且峰面积比为2∶1∶1∶1∶1的结构简式为
,核磁共振氢普有5组峰,且峰面积比为2∶1∶1∶1∶1的结构简式为①含有手性碳
②氟原子与苯环直接相连
③苯环上有3个取代基且不含其它环状结构
您最近一年使用:0次
23-24高三下·北京·开学考试
名校
解题方法
8 . 下列化学用语或图示表达正确的是
A.NaOH的电子式: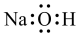 |
B.基态Cr的价层电子排布式: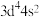 |
C.基态硅原子的价层电子轨道表示式: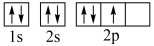 |
D. 的空间结构模型 的空间结构模型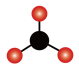 |
您最近一年使用:0次
2024-03-22更新
|
304次组卷
|
3卷引用:选择题1-5
2024·贵州贵阳·一模
解题方法
9 . 氯乙酸(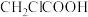 )是重要的分析试剂和有机合成中间体。一种制备氯乙酸的方法为
)是重要的分析试剂和有机合成中间体。一种制备氯乙酸的方法为 。下列说法正确的是
。下列说法正确的是
A. 分子中 分子中 键数 键数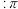 键数 键数 |
B. 键比 键比 键的键长更短、键能更小 键的键长更短、键能更小 |
C. 的酸性比 的酸性比 更强 更强 |
D.标准状况下, 是一种液态物质 是一种液态物质 |
您最近一年使用:0次
2024·广东深圳·一模
10 . 用“氧化-萃取法”可从卤水中提取碘,其方法为向酸化的卤水中加入 溶液,再加入萃取剂(R)进行萃取。该过程涉及以下反应:
溶液,再加入萃取剂(R)进行萃取。该过程涉及以下反应:
(ⅰ)

(ⅱ)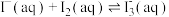
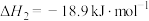
(ⅲ)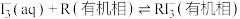
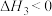
(1)根据盖斯定律,反应

________ 。
(2)基态碘原子价层电子的轨道表示式为________ 。
(3)①反应条件会影响碘的萃取率。其他条件不变时,不同温度下达平衡时碘萃取率
[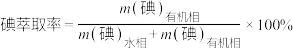 ]曲线如图所示:
]曲线如图所示:_______________ (忽略萃取剂的挥发、 的挥发及
的挥发及 分解产生的影响)。当萃取温度超过320 K时,
分解产生的影响)。当萃取温度超过320 K时, 的分解导致碘萃取率明显下降。
的分解导致碘萃取率明显下降。
②下列说法不正确的是________ (填标号)。
A.增大溶液的pH,碘萃取率降低 B.增大萃取剂用量,碘萃取率升高
C.萃取体系平衡后加水稀释, 变小 D.增大
变小 D.增大 的浓度,反应(ⅰ)的速率增大
的浓度,反应(ⅰ)的速率增大
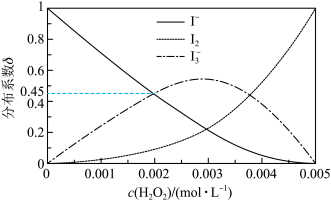
(4)未加萃取剂时,固定总碘浓度为 ,平衡时溶液中的
,平衡时溶液中的 、
、 、
、 分布系数
分布系数 与溶液中初始
与溶液中初始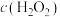 关系如图所示。[总碘浓度
关系如图所示。[总碘浓度 各组分折合为
各组分折合为 后的浓度之和,
后的浓度之和, ,如
,如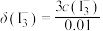 ]
] 、
、 、
、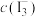 分别为
分别为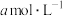 、
、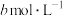 、
、 ,则
,则 、
、 、
、 之间的关系式为
之间的关系式为________ 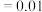 。
。
②计算反应 的平衡常数
的平衡常数
________ (结果保留3位有效数字)。
(5)测定卤水中的 方法:取
方法:取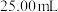 卤水于锥形瓶中,加适量氧化剂恰好将
卤水于锥形瓶中,加适量氧化剂恰好将 全部氧化为
全部氧化为 ;加
;加 溶液酸化后,再加入适量
溶液酸化后,再加入适量 溶液,密闭静置后,用
溶液,密闭静置后,用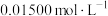
 标准溶液滴定至溶液呈微黄色,加入淀粉指示剂,继续滴定至终点;平行测定3次,平均消耗
标准溶液滴定至溶液呈微黄色,加入淀粉指示剂,继续滴定至终点;平行测定3次,平均消耗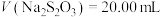 ,则卤水中
,则卤水中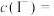
________  。(已知:
。(已知: )
)
 溶液,再加入萃取剂(R)进行萃取。该过程涉及以下反应:
溶液,再加入萃取剂(R)进行萃取。该过程涉及以下反应:(ⅰ)


(ⅱ)
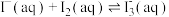
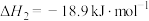
(ⅲ)
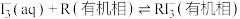
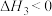
(1)根据盖斯定律,反应


(2)基态碘原子价层电子的轨道表示式为
(3)①反应条件会影响碘的萃取率。其他条件不变时,不同温度下达平衡时碘萃取率
[
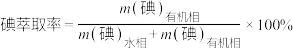 ]曲线如图所示:
]曲线如图所示: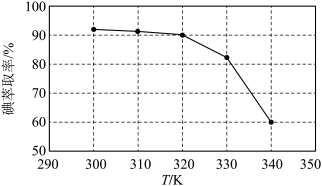
 的挥发及
的挥发及 分解产生的影响)。当萃取温度超过320 K时,
分解产生的影响)。当萃取温度超过320 K时, 的分解导致碘萃取率明显下降。
的分解导致碘萃取率明显下降。②下列说法不正确的是
A.增大溶液的pH,碘萃取率降低 B.增大萃取剂用量,碘萃取率升高
C.萃取体系平衡后加水稀释,
 变小 D.增大
变小 D.增大 的浓度,反应(ⅰ)的速率增大
的浓度,反应(ⅰ)的速率增大(4)未加萃取剂时,固定总碘浓度为
 ,平衡时溶液中的
,平衡时溶液中的 、
、 、
、 分布系数
分布系数 与溶液中初始
与溶液中初始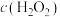 关系如图所示。[总碘浓度
关系如图所示。[总碘浓度 各组分折合为
各组分折合为 后的浓度之和,
后的浓度之和, ,如
,如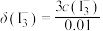 ]
]
 、
、 、
、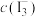 分别为
分别为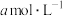 、
、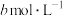 、
、 ,则
,则 、
、 、
、 之间的关系式为
之间的关系式为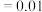 。
。②计算反应
 的平衡常数
的平衡常数
(5)测定卤水中的
 方法:取
方法:取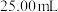 卤水于锥形瓶中,加适量氧化剂恰好将
卤水于锥形瓶中,加适量氧化剂恰好将 全部氧化为
全部氧化为 ;加
;加 溶液酸化后,再加入适量
溶液酸化后,再加入适量 溶液,密闭静置后,用
溶液,密闭静置后,用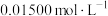
 标准溶液滴定至溶液呈微黄色,加入淀粉指示剂,继续滴定至终点;平行测定3次,平均消耗
标准溶液滴定至溶液呈微黄色,加入淀粉指示剂,继续滴定至终点;平行测定3次,平均消耗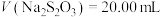 ,则卤水中
,则卤水中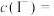
 。(已知:
。(已知: )
)
您最近一年使用:0次