名校
解题方法
1 . 硝酸生产的尾气中NO和 等氮氧化物以及酸性废水中
等氮氧化物以及酸性废水中 均须处理达标后再排放。
均须处理达标后再排放。
Ⅰ.硝酸生产的尾气中NO和 的处理。
的处理。
(1)硝酸尾气可用NaOH溶液吸收,主要反应为 ;
;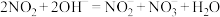 ;
;
①吸收后的溶液经浓缩、结晶、过滤,得到 晶体,该晶体中的主要杂质是
晶体,该晶体中的主要杂质是___________ (填化学式);
②吸收后排放的尾气中含量较高的氮氧化物是___________ (填化学式)。
(2)用NaClO溶液也能除去尾气中NO。其他条件相同,NO去除为 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。 的离子方程式为
的离子方程式为___________ ;NaClO溶液的初始pH越大,NO转化率越低。其原因是___________ 。
(3)利用 也能够还原氮氧化物(
也能够还原氮氧化物( )实现氮污染的治理。将硝酸尾气与
)实现氮污染的治理。将硝酸尾气与 的混合气体通入
的混合气体通入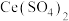 与
与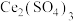 的混合溶液中实现无害化处理,其转化过程如图所示。
的混合溶液中实现无害化处理,其转化过程如图所示。 参与的离子方程式为
参与的离子方程式为___________ 。
②若该过程中,每转移3.6mol电子消耗1mol氮氧化物( ),则x为
),则x为___________ 。
Ⅱ.酸性废水中 的处理
的处理
(4)在45℃、惰性气体氛围中金属或合金可以将溶液废水中的 还原为
还原为 ,从而实现脱氨。量取三份50mL含
,从而实现脱氨。量取三份50mL含 的废水,分别用金属铝、金属铁和铝铁合金进行处理,溶液中
的废水,分别用金属铝、金属铁和铝铁合金进行处理,溶液中 的残留率(残留率=
的残留率(残留率=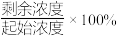 )与反应时间的关系如图所示。0~2h内,铝铁合金的脱氮效率比金属铝、金属铁要高得多,其可能原因是
)与反应时间的关系如图所示。0~2h内,铝铁合金的脱氮效率比金属铝、金属铁要高得多,其可能原因是___________ 。 ,废水中的
,废水中的 在水处理剂表面的变化如图所示,该电池正极上的电极反应式为
在水处理剂表面的变化如图所示,该电池正极上的电极反应式为___________ 。
 等氮氧化物以及酸性废水中
等氮氧化物以及酸性废水中 均须处理达标后再排放。
均须处理达标后再排放。Ⅰ.硝酸生产的尾气中NO和
 的处理。
的处理。(1)硝酸尾气可用NaOH溶液吸收,主要反应为
 ;
;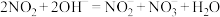 ;
;①吸收后的溶液经浓缩、结晶、过滤,得到
 晶体,该晶体中的主要杂质是
晶体,该晶体中的主要杂质是②吸收后排放的尾气中含量较高的氮氧化物是
(2)用NaClO溶液也能除去尾气中NO。其他条件相同,NO去除为
 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。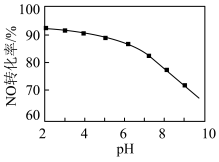
 的离子方程式为
的离子方程式为(3)利用
 也能够还原氮氧化物(
也能够还原氮氧化物( )实现氮污染的治理。将硝酸尾气与
)实现氮污染的治理。将硝酸尾气与 的混合气体通入
的混合气体通入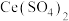 与
与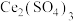 的混合溶液中实现无害化处理,其转化过程如图所示。
的混合溶液中实现无害化处理,其转化过程如图所示。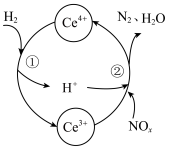
 参与的离子方程式为
参与的离子方程式为②若该过程中,每转移3.6mol电子消耗1mol氮氧化物(
 ),则x为
),则x为Ⅱ.酸性废水中
 的处理
的处理(4)在45℃、惰性气体氛围中金属或合金可以将溶液废水中的
 还原为
还原为 ,从而实现脱氨。量取三份50mL含
,从而实现脱氨。量取三份50mL含 的废水,分别用金属铝、金属铁和铝铁合金进行处理,溶液中
的废水,分别用金属铝、金属铁和铝铁合金进行处理,溶液中 的残留率(残留率=
的残留率(残留率=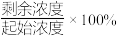 )与反应时间的关系如图所示。0~2h内,铝铁合金的脱氮效率比金属铝、金属铁要高得多,其可能原因是
)与反应时间的关系如图所示。0~2h内,铝铁合金的脱氮效率比金属铝、金属铁要高得多,其可能原因是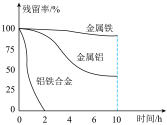
 ,废水中的
,废水中的 在水处理剂表面的变化如图所示,该电池正极上的电极反应式为
在水处理剂表面的变化如图所示,该电池正极上的电极反应式为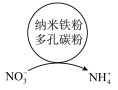
您最近半年使用:0次
2 . 按要求回答问题。
(1)制作印刷电路板的过程中常用FeCl3溶液与铜反应2Fe3++Cu=2Fe2++Cu2+,把该反应设计成原电池,可用___________ 作正极材料,正极反应的电极方程式为___________ 。
(2)氢氧燃料电池的构造如图所示,由此判断OH-向___________ (填“正”或“负”)极定向移动,Y极的电极反应式为___________ 。 Pb+PbO2+2H2SO4。铅蓄电池放电时正极电极质量
Pb+PbO2+2H2SO4。铅蓄电池放电时正极电极质量___________ (填“增大”或“减小”)。放电过程中,外电路中转移2.5 mol e-,消耗硫酸___________ mol。
(4)某电解池装置如图所示,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则___________ 。
②Y电极上的电极反应式为___________ ,检验该电极反应产物的方法及现象是___________ 。
(1)制作印刷电路板的过程中常用FeCl3溶液与铜反应2Fe3++Cu=2Fe2++Cu2+,把该反应设计成原电池,可用
(2)氢氧燃料电池的构造如图所示,由此判断OH-向

 Pb+PbO2+2H2SO4。铅蓄电池放电时正极电极质量
Pb+PbO2+2H2SO4。铅蓄电池放电时正极电极质量(4)某电解池装置如图所示,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
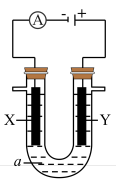
②Y电极上的电极反应式为
您最近半年使用:0次
名校
解题方法
3 . 一种新型微生物燃料电池可用于污水净化、海水淡化,其工作原理如图所示,下列说法正确的是。
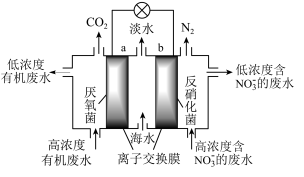
| A.该电池能在高温下工作 |
| B.a极为电池的正极 |
| C.有机废水处理后pH降低 |
D.处理 的电极反应为 的电极反应为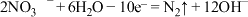 |
您最近半年使用:0次
名校
解题方法
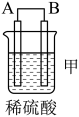
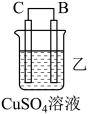
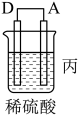
4 . 化学能还可以转化为电能,由A、B、C、D四种金属按表中装置图进行实验。
根据实验现象回答下列问题:
(1)装置甲中作正极的是_______ (填“A”或“B”)。
(2)外电路中电流由_______ (填“C极向B极移动”或“B极向C极移动”)。
(3)装置丙中金属A上电极反应属于_______ (填“氧化反应”或“还原反应”)。
(4)四种金属活动性由强到弱的顺序是_______ 。
| 装置 |
|
|
|
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
(1)装置甲中作正极的是
(2)外电路中电流由
(3)装置丙中金属A上电极反应属于
(4)四种金属活动性由强到弱的顺序是
您最近半年使用:0次
5 . 某化学小组为了探究铝电极在原电池中的作用,进行了下列实验,实验结果记录如表。下列说法正确的是
编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
① | Mg、Al | 稀盐酸 | 偏向Al |
② | Al、Cu | 稀盐酸 | 偏向Cu |
③ | Al、石墨 | 稀盐酸 | 偏向________ |
④ | Mg、Al | NaOH溶液 | 偏向Mg |
| A.实验①和②中,Al电极的作用相同 |
| B.实验③中,电流表指针偏向A1 |
C.实验④中,Mg为负极,电极反应式为: |
| D.以上实验说明,铝在原电池中的作用,与另一个电极材料和电解质溶液有关 |
您最近半年使用:0次
解题方法
6 . 用过量铁片与稀硫酸反应制备氢气,下列方法能增大反应速率而不影响氢气生成量的是
| A.稀硫酸改为浓硫酸 | B.加入 固体 固体 |
C.滴加少量 溶液 溶液 | D.加入 固体 固体 |
您最近半年使用:0次
解题方法
7 . 下列反应的离子方程式书写正确的是
| A.铜和硫酸溶液反应:Cu + 2H+ = Cu2++H2↑ |
| B.氯化铁溶液与氢氧化钡溶液反应:Fe3++ 3OH-= Fe(OH)3↓ |
| C.铁与稀盐酸反应:Fe+2H+=Fe3++H2↑ |
| D.醋酸除水垢:2CH3COOH+CaCO3=2CH3COO﹣+Ca2++CO2↑+H2O |
您最近半年使用:0次
名校
解题方法
8 . LiH是制备有机合成的重要还原剂LiAlH4的反应物,氢化锂遇水蒸气剧烈反应。某小组设计如图所示装置制备LiH:
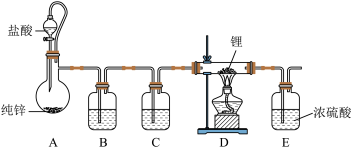
| A.装置B中盛装浓硫酸 |
| B.装置A中加入少量硫酸铜,可加快反应速率 |
| C.装置E用于吸收尾气,避免污染环境 |
| D.实验中,先点燃酒精灯,再通入H2 |
您最近半年使用:0次
名校
9 . 少量锌粉与100mL 的稀盐酸反应,为了加快此反应速率且不改变生成
的稀盐酸反应,为了加快此反应速率且不改变生成 的总量,以下方法可行的是
的总量,以下方法可行的是
①适当升高温度;②再加入100mL 的稀盐酸;③加少量
的稀盐酸;③加少量 固体;④加入少量醋酸钠固体;⑤加几滴浓硫酸;⑥滴入几滴硫酸铜溶液。
固体;④加入少量醋酸钠固体;⑤加几滴浓硫酸;⑥滴入几滴硫酸铜溶液。
 的稀盐酸反应,为了加快此反应速率且不改变生成
的稀盐酸反应,为了加快此反应速率且不改变生成 的总量,以下方法可行的是
的总量,以下方法可行的是①适当升高温度;②再加入100mL
 的稀盐酸;③加少量
的稀盐酸;③加少量 固体;④加入少量醋酸钠固体;⑤加几滴浓硫酸;⑥滴入几滴硫酸铜溶液。
固体;④加入少量醋酸钠固体;⑤加几滴浓硫酸;⑥滴入几滴硫酸铜溶液。| A.①⑤ | B.②③ | C.①⑥ | D.②④ |
您最近半年使用:0次
名校
解题方法
10 . 某学习小组在做氢气的制备实验时,用高纯锌粒和稀硫酸为反应物,结果发现反应速率较慢。下列措施不能加快制氢气速率的是
| A.将稀硫酸换成质量分数为98%的浓硫酸 | B.向反应液中加入适量的碳粉 |
| C.改换合适的装置并适当加热 | D.将锌粒换成质量相等的锌粉 |
您最近半年使用:0次