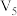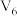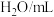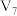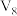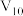解题方法
1 . 利用下图所示的电化学装置可消除污水中的氮污染,下列叙述正确的是

| A.电极电势:A>B |
B.负极上电极反应式: |
C.好氧反应器中反应式为 |
D.X离子为 ,交换膜Y是阴离子交换膜 ,交换膜Y是阴离子交换膜 |
您最近一年使用:0次
解题方法
2 . 下列装置能达到实验目的的是
|
|
A.制备 | B.探究硫价态(+6、+4、0)转化 |
|
|
| C.验证镁比铝活泼 | D.测定甲烷体积 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
昨日更新
|
37次组卷
|
3卷引用:2024届河南省百所名校仿真模拟大联考三模考试理综试题-高中化学
解题方法
3 . 在醋杆菌(最适生长温度为25~30℃)作用下,将酸性废水中有机物( )转化成
)转化成 ,同时电还原硝酸盐,实现地下水厌氧条件下修复,模拟原理如图所示,下列叙述正确的是
,同时电还原硝酸盐,实现地下水厌氧条件下修复,模拟原理如图所示,下列叙述正确的是
 )转化成
)转化成 ,同时电还原硝酸盐,实现地下水厌氧条件下修复,模拟原理如图所示,下列叙述正确的是
,同时电还原硝酸盐,实现地下水厌氧条件下修复,模拟原理如图所示,下列叙述正确的是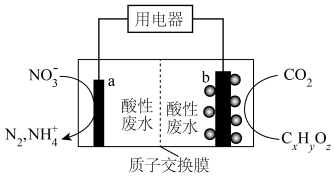
| A.放电时,电流由b极经外电路流向a极 |
| B.其他条件相同,70℃地下水修复效率高于40℃ |
C.若a极生成 和 和 共2mol,则理论上一定转移18mol电子 共2mol,则理论上一定转移18mol电子 |
D.b极反应式为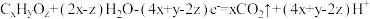 |
您最近一年使用:0次
名校
4 . 化学反应原理对指导实验和生产实际具有重要作用,请结合所学知识完成下列问题。
(1)某同学在用稀硫酸与铁块制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。
①硫酸铜溶液可以加快氢气生成速率的原因是____________________ 。
②为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量铁块的反应瓶中,收集产生的气体。记录获得相同体积的气体所需时间。
请完成此实验设计,其中: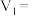
__________ ,
__________ ;该同学最后得出的结论为:当加入少量 溶液时,生成氢气的速率会大大提高。但当加入的
溶液时,生成氢气的速率会大大提高。但当加入的 溶液超过一定量时,生成氢气的速率反而会下降。
溶液超过一定量时,生成氢气的速率反而会下降。
请分析氢气生成速率下降的主要原因:______________________________ 。
(2)下图是以铂( )为电极的氢氧燃料电池示意图,电解质溶液为稀
)为电极的氢氧燃料电池示意图,电解质溶液为稀 。
。__________ (填“a”或“b”)极,电池工作时,溶液中 移向
移向__________ (填“a”或“b”)极。
②若有 参加反应,则理论上
参加反应,则理论上 在b极获得电子的物质的量为
在b极获得电子的物质的量为__________ 。
(3)已知合成氮反应: ,在一定温度下,向恒容的密闭容器中充入一定量的
,在一定温度下,向恒容的密闭容器中充入一定量的 和
和 发生反应,测得各组分浓度随时间变化如下图所示。
发生反应,测得各组分浓度随时间变化如下图所示。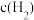 变化的曲线是
变化的曲线是__________ (填“曲线A”、“曲线B”或“曲线C”)。
②下列描述一定能表示上述反应体系达平衡状态的是__________ (填字母)。
A.单位时间内消耗 的
的 ,同时生成
,同时生成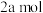 的
的
B. 的转化率不变
的转化率不变
C.容器内压强不再发生变化
D. 的百分含量不变
的百分含量不变
E.
(4)已知: ,不同温度(T)下,恒容容器中
,不同温度(T)下,恒容容器中 分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度
分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度 消耗一半时所需的相应时间),则
消耗一半时所需的相应时间),则
__________ (填“>”、“=”或“<”) ,当温度为
,当温度为 、起始压强为
、起始压强为 ,反应至
,反应至 时,此时体系压强
时,此时体系压强
__________ (用 表示)。
表示)。
(1)某同学在用稀硫酸与铁块制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。
①硫酸铜溶液可以加快氢气生成速率的原因是
②为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量铁块的反应瓶中,收集产生的气体。记录获得相同体积的气体所需时间。
实验编号 | A | B | C | D | E | F |
| 30 |
|
|
|
|
|
饱和 | 0 | 0.5 | 2.5 | 5 |
| 20 |
|
|
| 17.5 |
| 10 | 0 |
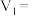

 溶液时,生成氢气的速率会大大提高。但当加入的
溶液时,生成氢气的速率会大大提高。但当加入的 溶液超过一定量时,生成氢气的速率反而会下降。
溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因:
(2)下图是以铂(
 )为电极的氢氧燃料电池示意图,电解质溶液为稀
)为电极的氢氧燃料电池示意图,电解质溶液为稀 。
。
 移向
移向②若有
 参加反应,则理论上
参加反应,则理论上 在b极获得电子的物质的量为
在b极获得电子的物质的量为(3)已知合成氮反应:
 ,在一定温度下,向恒容的密闭容器中充入一定量的
,在一定温度下,向恒容的密闭容器中充入一定量的 和
和 发生反应,测得各组分浓度随时间变化如下图所示。
发生反应,测得各组分浓度随时间变化如下图所示。
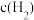 变化的曲线是
变化的曲线是②下列描述一定能表示上述反应体系达平衡状态的是
A.单位时间内消耗
 的
的 ,同时生成
,同时生成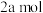 的
的
B.
 的转化率不变
的转化率不变C.容器内压强不再发生变化
D.
 的百分含量不变
的百分含量不变E.

(4)已知:
 ,不同温度(T)下,恒容容器中
,不同温度(T)下,恒容容器中 分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度
分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度 消耗一半时所需的相应时间),则
消耗一半时所需的相应时间),则
 ,当温度为
,当温度为 、起始压强为
、起始压强为 ,反应至
,反应至 时,此时体系压强
时,此时体系压强
 表示)。
表示)。
您最近一年使用:0次
5 . 一定温度下,在2L的密闭容器中,M、N两种气体的物质的量随时间变化的曲线如图所示:_______ 。
(2)反应达到化学平衡时,化学反应速率
______ ,N的转化率为______ 。
(3)下列可作为判断该反应达到平衡状态的依据是_______。
(4)能加快反应速率的措施是_____。
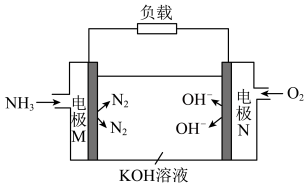
(5)潜艇中使用的液氨—液氧燃料电池工作原理如图所示: 离子向
离子向_____ (填“电极a”或“电极b”)移动。
②电极a的电极反应式为_____ 。
③可通过 与
与 反应来制得火箭燃料肼(
反应来制得火箭燃料肼( )。该反应的化学反应方程式是
)。该反应的化学反应方程式是_____ 。

(2)反应达到化学平衡时,化学反应速率

(3)下列可作为判断该反应达到平衡状态的依据是_______。
| A.该条件下,正、逆反应速率都为零 |
| B.该条件下,混合气体的密度不再发生变化 |
| C.该条件下,混合气体的压强不再发生变化 |
D.该条件下,单位时间内消耗 的同时,消耗 的同时,消耗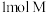 |
(4)能加快反应速率的措施是_____。
| A.升高温度 | B.容器容积不变,充入惰性气体 |
C.容器压强不变,充入惰性气体 | D.使用催化剂 |
(5)潜艇中使用的液氨—液氧燃料电池工作原理如图所示:

 离子向
离子向②电极a的电极反应式为
③可通过
 与
与 反应来制得火箭燃料肼(
反应来制得火箭燃料肼( )。该反应的化学反应方程式是
)。该反应的化学反应方程式是
您最近一年使用:0次
名校
6 . 镁锂双盐电池是新型二次离子电池,其放电时的工作原理如图所示。

A.充电时, 和 和 均向 均向 极区移动 极区移动 |
B.充电时,阴极的电极反应式为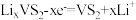 |
C.放电时, 电极发生氧化反应 电极发生氧化反应 |
D.电池工作时,若外电路中转移电子 ,则两极的质量变化值相差 ,则两极的质量变化值相差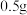 |
您最近一年使用:0次
名校
解题方法
7 . 研究化学能与热能、电能的转化具有重要价值。回答下列问题:
(1)下列化学反应过程中的能量变化符合图示的是___________ (填序号)。
①酸碱中和反应 ②碳酸钙分解 ③金属钠与水反应 ④酒精燃烧 ⑤灼热的碳与二氧化碳反应 ⑥ 与
与 反应
反应 的反应过程如图所示:
的反应过程如图所示: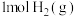 和
和 充分反应,则反应物中旧键断裂共吸收
充分反应,则反应物中旧键断裂共吸收___________ kJ能量,生成物中新键形成共放出___________ kJ能量,该反应为___________ (填“吸热”或“放热”)反应。
原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(3)现有如下两个反应:A ;B.
;B.  ,判断上述两个反应中能设计成原电池的是
,判断上述两个反应中能设计成原电池的是___________ (填“A”或“B”)。
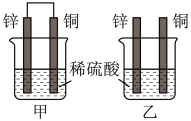
(4)将纯锌片和纯铜片按图中方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:___________ 。
A 甲、乙均为化学能转变为电能的装置 B. 乙中铜片上没有明显变化
C. 甲中铜片质量减少、乙中锌片质量减少 D. 两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲___________ 乙(填“>”“<”或“=”)。
③请写出图中构成原电池的负极电极反应式:___________ 。
(5)若利用反应 设计一个原电池,请完善实验装置,负极材料:
设计一个原电池,请完善实验装置,负极材料:___________ ;正极材料:___________ ;电解质溶液:___________ 。
__________________ ___________ 。
(1)下列化学反应过程中的能量变化符合图示的是
①酸碱中和反应 ②碳酸钙分解 ③金属钠与水反应 ④酒精燃烧 ⑤灼热的碳与二氧化碳反应 ⑥
 与
与 反应
反应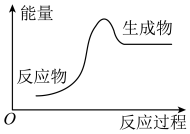
 的反应过程如图所示:
的反应过程如图所示: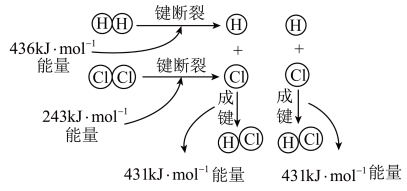
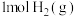 和
和 充分反应,则反应物中旧键断裂共吸收
充分反应,则反应物中旧键断裂共吸收原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(3)现有如下两个反应:A
 ;B.
;B.  ,判断上述两个反应中能设计成原电池的是
,判断上述两个反应中能设计成原电池的是(4)将纯锌片和纯铜片按图中方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:
A 甲、乙均为化学能转变为电能的装置 B. 乙中铜片上没有明显变化
C. 甲中铜片质量减少、乙中锌片质量减少 D. 两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲
③请写出图中构成原电池的负极电极反应式:
(5)若利用反应
 设计一个原电池,请完善实验装置,负极材料:
设计一个原电池,请完善实验装置,负极材料: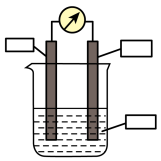
您最近一年使用:0次
8 . 根据实验目的设计方案并进行实验,观察到相关现象,其中方案设计或结论正确的是
| 实验目的 | 方案设计 | 现象 | 结论 | |
| A | 检验乙酰水杨酸中的酯基 | 将乙酰水杨酸溶液分装于两支试管中: 试管①中滴入几滴  溶液 溶液试管②中先滴入2滴稀硫酸,加热后滴入几滴  溶液,振荡后滴入几滴 溶液,振荡后滴入几滴 溶液 溶液 | 试管①中溶液未变紫色 试管②中溶液变紫色 | 乙酰水杨酸中存在酯基 |
| B | 探究金属的牺性阳极保护法 | 把琼脂溶液倒入培养皿中,滴入56滴酚酞溶液和 溶液混合均匀,将铁钉用锌片包裹只露出两端并放入培养皿中。 溶液混合均匀,将铁钉用锌片包裹只露出两端并放入培养皿中。 | 铁钉两端周围的溶液不变红,锌片周围溶液变红,未观察到蓝色沉淀 | 锌片被腐蚀,铁钉被保护 |
| C | 检验菠菜中是否含有铁元素 | 取新鲜菠菜叶剪碎研磨后加水搅拌,过滤得到滤液,取少量滤液于试管中,滴加几滴 溶液,振荡 溶液,振荡 | 试管中的滤液不变红 | 该种菠菜中不含铁元素 |
| D | 检验氨气中的水蒸气 | 将混合气体按一定流速通过盛放有硫酸铜粉末的硬质玻璃管 | 硫酸铜粉末变蓝 | 氨气中存在水蒸气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 下图是一种以丙酮和异丙醇为氧化/还原电对的热电化学电池的工作原理。下列说法错误的是
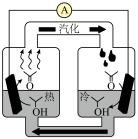
| A.热电化学电池能将热能转化为电能 |
| B.热端电极电势低于冷端电极电势 |
C.负极的电极反应: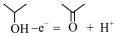 |
| D.温差使丙酮蒸发和冷凝,引起了丙酮的浓度差,可持续放电 |
您最近一年使用:0次
解题方法
10 . 下图是“海水-河水”浓差电池装置示意图(不考虑溶解氧的影响),其中a、b均为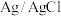 复合电极,下列说法不正确的是
复合电极,下列说法不正确的是
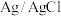 复合电极,下列说法不正确的是
复合电极,下列说法不正确的是
A.b的电极反应式为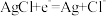 |
B.内电路中, 由a极区向b极区迁移 由a极区向b极区迁移 |
C.工作一段时间后,两极 溶液的浓度差减小 溶液的浓度差减小 |
D.电路中转移1  时,理论上a极区模拟海水的质量减少23g 时,理论上a极区模拟海水的质量减少23g |
您最近一年使用:0次