名校
解题方法
1 . 下列有关原电池装置的说法不正确的是
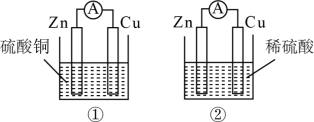

| A.①、②中,锌片都发生氧化反应 |
B.①、②中,SO 都向铜片移动 都向铜片移动 |
| C.②可将2H++Zn=H2↑+Zn2+释放的能量直接转化为电能 |
| D.当①、②中通过外电路的电子数相等时,正极生成物的质量比为32:1 |
您最近一年使用:0次
2022-07-10更新
|
682次组卷
|
3卷引用:陕西省韩城市2022-2023学年高一下学期期末考试化学试题
解题方法
2 . 根据信息填空
(1)用如图所示的装置进行铝热法炼铁实验,写出铝热法炼铁反应的化学方程式:_______ 。
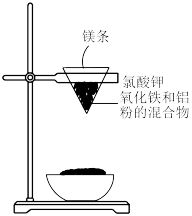
(2)已知:Fe+2FeCl3=3FeCl2,利用这一反应,设计一个原电池,画出示意图,标明电极材料名称,电解质溶液______ 。该原电池中,三价铁离子向_______ (填“正极”或“负极”)移动。负极的电极反应式为_______

(3)古代《药性论》中有关铅丹(Pb3O4)的描述是治惊悸狂走,呕逆,消渴,铅丹(Pb3O4)也可作为防锈用涂料,呈红褐色,又名红丹。
①铅丹可用PbO在空气中加热制备,请写出有关反应的化学方程式_______ 。
②铅丹曾用于铁制品防锈,请举例说明铁制品防锈的其它方法_______ (只填一种方法)。
(1)用如图所示的装置进行铝热法炼铁实验,写出铝热法炼铁反应的化学方程式:

(2)已知:Fe+2FeCl3=3FeCl2,利用这一反应,设计一个原电池,画出示意图,标明电极材料名称,电解质溶液

(3)古代《药性论》中有关铅丹(Pb3O4)的描述是治惊悸狂走,呕逆,消渴,铅丹(Pb3O4)也可作为防锈用涂料,呈红褐色,又名红丹。
①铅丹可用PbO在空气中加热制备,请写出有关反应的化学方程式
②铅丹曾用于铁制品防锈,请举例说明铁制品防锈的其它方法
您最近一年使用:0次
名校
3 . 乙醇(C2H5OH)是重要的工业原料,它的应用和制备方法是科研人员研究的热点,其在生产生活上用途很多。回答下列问题:
(1)乙醇汽油代替铅基汽油解决了铅基汽油燃烧对环境的污染。
①C2H5OH燃烧时将____ 能转化为____ 能。
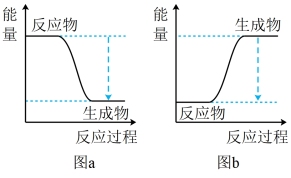
②C2H5OH完全燃烧的化学方程式为____ ,该反应过程中能量变化的图象符合____ (填“图a”或“图b”)。
(2)某碱性C2H5OH燃料电池工作原理如图c,总化学方程式C2H5OH+3O2+4KOH=2K2CO3+5H2O。
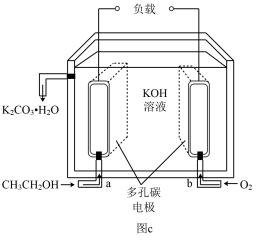
①该电池工作时,电子____ (填“由a极经外电路流向b极”或“由b极经外电路流向a极”)。
②负极电极反应式为____ 。
(3)工业上通过CO与H2反应制取C2H5OH(2CO+4H2 C2H5OH+H2O),温度为T时CO与C2H5OH的物质的量的浓度与时间的关系如图d(生成物、反应物均为气体)。
C2H5OH+H2O),温度为T时CO与C2H5OH的物质的量的浓度与时间的关系如图d(生成物、反应物均为气体)。
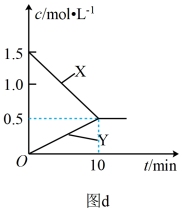
①X为____ (填化学式)。
②反应前10min,CO的转化率=_____ %(精确到小数点后一位)。
(1)乙醇汽油代替铅基汽油解决了铅基汽油燃烧对环境的污染。
①C2H5OH燃烧时将
②C2H5OH完全燃烧的化学方程式为

(2)某碱性C2H5OH燃料电池工作原理如图c,总化学方程式C2H5OH+3O2+4KOH=2K2CO3+5H2O。

①该电池工作时,电子
②负极电极反应式为
(3)工业上通过CO与H2反应制取C2H5OH(2CO+4H2
 C2H5OH+H2O),温度为T时CO与C2H5OH的物质的量的浓度与时间的关系如图d(生成物、反应物均为气体)。
C2H5OH+H2O),温度为T时CO与C2H5OH的物质的量的浓度与时间的关系如图d(生成物、反应物均为气体)。
①X为
②反应前10min,CO的转化率=
您最近一年使用:0次
解题方法
4 . 锌-空气电池具有蓄电量大、循环次数多等优点。下列说法正确的是
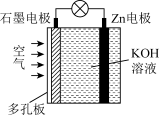

A.电池放电时, 电极逐渐溶解 电极逐渐溶解 |
| B.石墨为负极 |
C.电子由石墨经导线流向 片 片 |
| D.电池放电时,实现了电能向化学能的转化 |
您最近一年使用:0次
2022-06-02更新
|
44次组卷
|
2卷引用:陕西省宝鸡市陈仓区2021-2022学年高一下学期期末考试化学试题
名校
解题方法
5 . 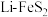 电池是目前电池中综合性能最好的一种电池,其原理示意图如图所示。已知电池放电时的反应为
电池是目前电池中综合性能最好的一种电池,其原理示意图如图所示。已知电池放电时的反应为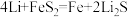 (S的化合价均为-1价)。下列说法正确的是
(S的化合价均为-1价)。下列说法正确的是

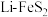 电池是目前电池中综合性能最好的一种电池,其原理示意图如图所示。已知电池放电时的反应为
电池是目前电池中综合性能最好的一种电池,其原理示意图如图所示。已知电池放电时的反应为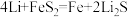 (S的化合价均为-1价)。下列说法正确的是
(S的化合价均为-1价)。下列说法正确的是
| A.Li为电池的正极,发生氧化反应 |
B.电流由Li经负载,流向 极 极 |
C.正极的电极反应式为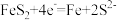 |
D.将熔融的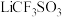 改为LiCl的水溶液,电池性能更好 改为LiCl的水溶液,电池性能更好 |
您最近一年使用:0次
2022-06-01更新
|
236次组卷
|
3卷引用:陕西省榆林市第一中学2021-2022学年高一下学期期末考试化学试题
名校
6 . I.回答下列问题:
(1)标准状况下, 、
、 、
、 的密度之比为
的密度之比为_______ ,同温同压下,1L 和
和 气体中所含的中子数之比为
气体中所含的中子数之比为_______ 。
(2)如图所示, 分子结构与白磷分子相似,呈正四面体结构。已知断裂1molN—N键吸收193kJ热量,断裂1mol
分子结构与白磷分子相似,呈正四面体结构。已知断裂1molN—N键吸收193kJ热量,断裂1mol 键吸收941kJ热量,则1mol
键吸收941kJ热量,则1mol 气体转化为
气体转化为 时要
时要_______ (填“吸收”或“放出”)热量_______ kJ。

II.某化学兴趣小组的几位同学探究原电池原理的应用时,做了如图的实验:原电池原理判断金属的活泼性。
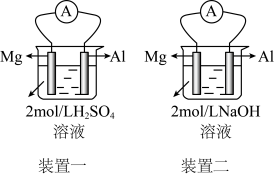
(3)实验前,甲同学认为“构成原电池的负极总是较活泼的金属材料”,若根据他的判断,两个装置中的Al都是_______ 极;实际实验时发现两个装置中的电流表偏转方向不同,以下的有关中判断正确的是_______ 。
A.利用原电池反应判断金属活动性顺序时应注意选择合适的电解质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动性顺序已过时,已没有实用价值
D.该实验说明化学研究对象复杂,反应受条件影响较大,故应具体问题具体分析
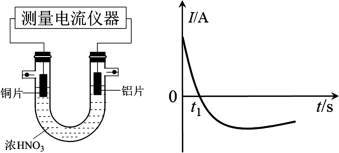
(4)乙同学利用打磨过的铜片和铝片设计了如图的实验装置,并测量和绘制了原电池的电流(I)随时间(t)的变化曲线(极短时间电流反转),则图中t1时刻之后阶段,负极材料是_______ 。
(1)标准状况下,
 、
、 、
、 的密度之比为
的密度之比为 和
和 气体中所含的中子数之比为
气体中所含的中子数之比为(2)如图所示,
 分子结构与白磷分子相似,呈正四面体结构。已知断裂1molN—N键吸收193kJ热量,断裂1mol
分子结构与白磷分子相似,呈正四面体结构。已知断裂1molN—N键吸收193kJ热量,断裂1mol 键吸收941kJ热量,则1mol
键吸收941kJ热量,则1mol 气体转化为
气体转化为 时要
时要
II.某化学兴趣小组的几位同学探究原电池原理的应用时,做了如图的实验:原电池原理判断金属的活泼性。

(3)实验前,甲同学认为“构成原电池的负极总是较活泼的金属材料”,若根据他的判断,两个装置中的Al都是
A.利用原电池反应判断金属活动性顺序时应注意选择合适的电解质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动性顺序已过时,已没有实用价值
D.该实验说明化学研究对象复杂,反应受条件影响较大,故应具体问题具体分析
(4)乙同学利用打磨过的铜片和铝片设计了如图的实验装置,并测量和绘制了原电池的电流(I)随时间(t)的变化曲线(极短时间电流反转),则图中t1时刻之后阶段,负极材料是

您最近一年使用:0次
名校
7 . 锌—铜原电池示意图如图所示。下列说法正确的是
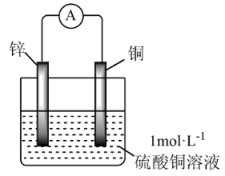

| A.电子由锌片流向硫酸铜溶液再流向铜片 | B.负极质量减少,正极质量增加 |
| C.锌电极发生还原反应 | D.该装置能将化学能完全转化为电能 |
您最近一年使用:0次
解题方法
8 . 原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
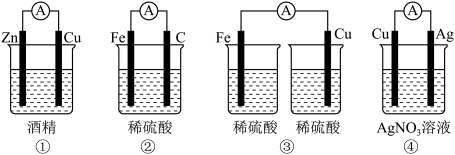
(1)如图装置中属于原电池的是____ (填序号)。
(2)依据氧化还原反应Fe+2Ag+=Fe2++2Ag设计的原电池如图1所示。
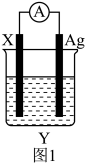
①电极X的材料是____ 。
②X电极的电极反应式为____ ;Ag电极上发生的是___ (填“氧化”或“还原”)反应。
③当有2.8 g铁溶解时,Ag电极增重____ g。
(3)以甲烷为燃料的新型电池得到广泛的研究,如图2是目前研究较多的一类燃料电池的工作原理示意图。
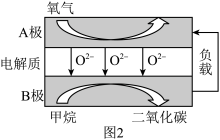
①A极为电池极____ (填“正”或“负”)。
②B极的电极反应式为____ ;若消耗标准状况下的CH411.2 L,则电路中转移____ mol电子。
(1)如图装置中属于原电池的是

(2)依据氧化还原反应Fe+2Ag+=Fe2++2Ag设计的原电池如图1所示。

①电极X的材料是
②X电极的电极反应式为
③当有2.8 g铁溶解时,Ag电极增重
(3)以甲烷为燃料的新型电池得到广泛的研究,如图2是目前研究较多的一类燃料电池的工作原理示意图。

①A极为电池极
②B极的电极反应式为
您最近一年使用:0次
21-22高一·全国·假期作业
名校
解题方法
9 . 图1是铜锌原电池示意图。图2中x轴表示实验时流入正极的电子的物质的量,则y轴表示

| A.溶液的质量 | B.c(Zn2+) | C.c(Cu2+) | D.锌棒的质量 |
您最近一年使用:0次
2022-05-12更新
|
217次组卷
|
5卷引用:陕西省咸阳市泾阳县2021-2022学年高一下学期期中质量检测化学试题
陕西省咸阳市泾阳县2021-2022学年高一下学期期中质量检测化学试题(已下线)综合测试卷-【寒假自学课】2022年高一化学寒假精品课(苏教版必修第二册)福建省厦门第一中学2021-2022学年高一下学期期中考试化学试题新疆生产建设兵团第二师八一中学2022-2023学年高一下学期期末考试化学试题福建省南平市福建省武夷山第一中学2023-2024学年高一下学期4月期中考试化学试题
解题方法
10 . 如图所示是两种常见的化学电源示意图,下列说法错误的是
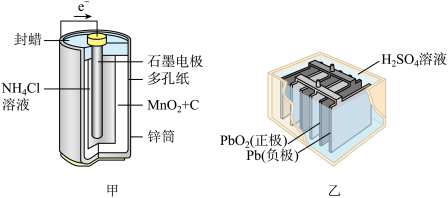

| A.化学电源是将化学能转化为电能的实用装置 |
| B.甲、乙分别属于一次电池和二次电池 |
| C.铅蓄电池可以无限制地反复放电、充电 |
| D.甲电池的负极反应式为Zn-2e-=Zn2+ |
您最近一年使用:0次



